Различните модели на бъбречна фиброза са показателни за увреждане на различни бъбречни отделения
Mar 20, 2022
Резюме:Фиброзата на бъбреците е често срещана проява и отличителен белег на голямо разнообразие от хроничнизаболяване на бъбреците(CKD), който се появява в различни морфологични модели, което предполага различни патогенни причини. Широките макроскопски видими белези са последствията от тежко фокално нараняване и пълна деструкция на паренхима, отразяващи реакцията на заздравяване на раната като последица от инфаркт. Вбъбрек,хроничното гломерулно увреждане води до атрофия на съответния тубул, дегенерация на този специфичен нефрон и накрая интерстициална фиброза/тубулна атрофия (IF/TA). В сравнение с този индуциран от гломерул фокален заместващ белег, дифузната фиброза, независима от тубулната атрофия, изглежда е различен патогенен процес.Бъбрекизглежда, че фиброзата се развива по специфичен за отделението начин, но дали фокалната и дифузната фифиброза има различни характеристики, свързани с други гломерулни или тубулоинтерстициални лезии, остава неуловим. В настоящото изследване ние имахме за цел да анализираме бъбречни фиброзни модели, свързани с бъбречни лезии, които пряко допринасят за бъбречната фиброгенеза, за да разкрием фиброзни модели и прояви при увреждане на отделни бъбречни отделения. Модели набъбрекфиброзата са анализирани в експериментални модели на ХБН и различни бъбречни патологии в корелация с хистопатологични и ултраструктурни находки. След индуцирането на изолиран сърповиден гломерулонефрит (GN) при нефротоксичен серумен нефрит (NTN), хроничното гломерулно увреждане води до предимно фокална фиброза в съседство с атрофични тубули. Обратно, използването на едностранна обструкция на уретера (UUO) като модел на първично увреждане на тубулоинтерстициалния компартмент разкрива дифузна фиброза като преобладаващ модел на хронични лезии. И накрая, индуцираната от фолиева киселина нефропатия (FAN) като модел на първично тубулно увреждане с последваща тубулна атрофия, независимо от хроничното гломерулно увреждане, също индуцира преобладаващ фокален IF/TA. Анализирайки няколко бъбречни патологии, нашите данни също предполагат, че фокалната и дифузната фифиброза изглежда допринасят като хронични лезии в по-голямата част от бъбречните заболявания при хора, като присъстват главно в свързания с антинеутрофилни цитоплазмени антитела (ANCA) GN, лупусен нефрит и IgA нефропатия ( IgAN). Фокалната IF/TA корелира с гломерулно увреждане и необратимо увреждане на нефроните, докато дифузната фиброза при ANCA GN е свързана изрично с интерстициално възпаление, независимо от гломерулно увреждане и загуба на нефрон. Ултраструктурен анализ на фокална IF/TA спрямо дифузна фиброза разкрива различни състави на матрицата, допълнително подкрепени от различни колагенови сигнатури в набори от данни за транскриптоми. По отношение на дългосрочния бъбречен резултат, само степента на фокална IF/TA корелира с развитието на краен стадийзаболяване на бъбреците(ESKD) в ANCA GN. За разлика от тях дифузенбъбрекфиброзата не се свързва с дългосрочния бъбречен резултат. В заключение, тук предоставяме доказателства, че фокусен модел набъбрекфиброзата изглежда е свързана със загуба на нефрони и заместващи белези. За разлика от тях, дифузен модел набъбрекфиброзата изглежда е резултат от първично интерстициално възпаление и нараняване.
Ключови думи:модел на фиброза; фиброза на бъбреците; увреждане на бъбреците; тубулна атрофия; възпаление; системен васкулит

CISTANCHE ЩЕ ПОДОБРИ БЪБРЕЧНА/БЪБРЕЧНА ИНФЕКЦИЯ
Въведение
Фиброзата на бъбреците е често срещана проява и отличителен белег на голямо разнообразие от хроничнибъбречни заболявания(CKD), водещ до краен стадийзаболяване на бъбреците(ESKD), независимо от подлежащата етиология [1]. Като цяло бъбречната фиброза (или тубулоинтерстициална фиброза) представлява хистоморфологията на отлагането на екстрацелуларен матрикс (ECM) във всички стадии на ХБН.Бъбрекфиброзата може да се появи в различни морфологични модели, което предполага други патогенни причини [2]. Широките макроскопски видими белези са последствията от тежко фокално нараняване и пълна деструкция на паренхима, отразяващи реакцията на зарастване на рани като последица от инфаркт [3]. Вбъбрекхроничното гломерулно увреждане води до атрофия на съответния тубул, дегенерация на този специфичен нефрон и накрая интерстициална фиброза/тубулна атрофия (IF/TA) [4,5]. В сравнение с този индуциран от гломерул фокален заместващ белег, фифиброзата, независима от тубулна атрофия (по-нататък наричана дифузна фиброза), изглежда е различен патогенен процес [6,7]. Тубулната атрофия се определя като загуба на специализиран транспортен и метаболитен капацитет и обикновено се характеризира с малки тубули, епителни клетки с бледа цитоплазма или разширени много тънки тубули. За разлика от нашето разбиране за фиброзата като белег, представляващ непълен процес на възстановяване на бъбреците, дифузната фиброза се счита за активен фактор за прогресията на ХБН, което основно се основава на наблюдението, че намаляването на бъбречната функция корелира по-тясно с тубулоинтерстициалната фиброза, отколкото с гломерулно увреждане [8–11]. Въз основа на концепциите по-горе,бъбрекфиброзата се обсъжда или като механизъм на непълнабъбреквъзстановяване или активен принос за прогресията на ХБН [12,13].Бъбрекизглежда, че фиброзата се развива по специфичен за компартмента начин, но остава неясно дали фокалната IF/TA или дифузната фиброза имат различни характеристики, свързани с други гломерулни или тубулоинтерстициални лезии. В настоящото изследване ние имахме за цел да анализираме бъбречни фиброзни модели, свързани с гореспоменатите бъбречни лезии (напр. гломерулни, тубулни и интерстициални лезии), които пряко допринасят за бъбречната фиброгенеза.
Материали и методи
2.1. ЖивотниВсички експериментални проучвания върху животни са извършени с одобрението на Комитета за институционална грижа и използване на животните към Медицинския център на Бет Израел Дяконес (BIDMC) и Университетския медицински център Гьотинген в съответствие с насоките на ARRIVE [14]. Експерименталните протоколи са описани подробно по-долу. Размерът на извадката от n=5 мишки във всяка група не беше официално захранван или предварително определен. 2.2. Нефротоксичен серумен нефрит (NTN) Всяка мишка първоначално беше предварително имунизирана с 200 µg овчи IgG (Capralogics, Gilbertville, IA, USA) в 200 µL пълен адювант на Freund (Sigma, St. Louis, MO, USA), инжектиран интравенозно с 40 µL нефротоксичен серум на дни 5, 6 и 7 след преимунизацията. Експериментите приключиха 63 дни след имунизацията [15,16]. 2.3. Едностранна уретерална обструкция (UUO) Мишки C57BL/6 на възраст от осем до дванадесет седмици бяха анестезирани с инхалация на изофлуран и аналгезията беше извършена чрез подкожно инжектиране на бупренорфин. Уретерът беше отделен от околните тъкани и две лигатури бяха поставени на около 5 mm една от друга в горните две трети на уретера на левия бъбрек, за да се получи надеждна обструкция. Експериментите приключиха десет дни след лигирането на уретера, както е описано по-рано [17].

CISTANCHE ЩЕ ПОДОБРИ БЪБРЕЧНО/БЪБРЕЧНО ЗАБОЛЯВАНЕ
2.4. Индуцирана от фолиева киселина нефропатия (FAN)Бъбречно увреждане се предизвиква с еднократно интраперитонеално инжектиране на фолиева киселина (250 mg/kg телесно тегло в PBS) в CD1 мишки. Експериментите приключиха 96 дни след инжектирането.
2.5. Изследвана популация Общ брой от 112 случая на различни бъбречни патологии, включително остър интерстициален нефрит (AIN), гломерулонефрит, свързан с антинеутрофилни цитоплазмени антитела (ANCA GN), мембранен GN, лупусен нефрит, хипертонична нефропатия, IgA нефропатия (IgAN), фокално-сегментна гломерулосклероза (FSGS) и диабетзаболяване на бъбреците(DKD) бяха включени. Въпреки че не се изисква официално одобрение за използването на рутинни клинични данни, е дадено положително становище от комисията по етика на Университетския медицински център Гьотинген (№ 22/2/14 и 28/9/17). Освен това всички пациенти се съгласиха да събират данни като част от обичайните си медицински грижи. 2.6. Дефиниции Изчислената скорост на гломерулна филтрация (GFR) се изчислява с помощта на хроничнатаЗаболяване на бъбрецитеУравнение за епидемиологично сътрудничество (CKD-EPI) [18]. За случаите на ANCA GN, оценката на активността на Бирмингамския васкулит (BVAS) версия 3 беше изчислена, както е описано по-горе [19]. BVAS се оценява по скала от 0 до 63, като 0 показва липсата на активност на заболяването, а по-високите резултати показват активно заболяване. 2.7. Masson's Trichrome Stain Фиксирани с формалин, вградени в парафин бъбреци бяха срязани на 3 µm и оцветяването беше извършено в BIDMC Histopathology Core и Университетския медицински център Гьотинген. 2.8. Бъбречна хистопатология Бъбречните патолози (LS, SH и PS) оцениха всички биопсии и бяха заслепени за събиране и анализ на клинични данни. Аналогично на точковата система на Banff, процентът на кортикалните области, засегнати от общотобъбрекфиброза и фокална интерстициална фиброза в зоната на тубулна атрофия (IF/TA) бяха оценени в целия образец. Дифузната фиброза, която не е свързана с тубулна атрофия, се изчислява чрез изваждане [20]. В допълнение, всеки гломерул се оценява отделно за наличието на некроза, полумесеци и глобална склероза. Следователно, процентът на гломерулите с някоя от тези характеристики се изчислява като част от общия брой гломерули във всяка бъбречна биопсия. Въз основа на тези точки, хистопатологичното подгрупиране според Berden et al. (фокален, полумесечен, смесен или склеротичен клас) и ARRS според Brix et al. (нисък, среден или висок риск) [21,22].
2.9. Терапия за индукция на ремисияГлюкокортикоидите (GCs) се прилагат или като интравенозна пулсова терапия, или перорално с постепенно намаляване. По време на индукционния период по преценка на лекуващите лекари се прилага плазмен обмен (PEX). Ритуксимаб (RTX) се прилага в четири интравенозни дози от 375 mg/m2 всяка седмица; RTX не е прилаган в рамките на 48 часа преди лечението с PEX. Циклофосфамид (CYC) се прилага в три интравенозни дози до 15 mg/kg на всеки две седмици и на всеки три седмици след това, коригирани спрямо възрастта и бъбречната функция. Приложена е комбинирана терапия в четири интравенозни дози при 375 mg/m2 RTX всяка седмица и две интравенозни дози при 15 mg/kg CYC на всеки две седмици. По преценка на лекуващите лекари, терапията за индукция на ремисия зависи от предишните схеми и индивидуалните фактори на пациента. RTX е предпочитан при по-млади пациенти, като токсичността е основната причина за този избор [23]. Профилактика за предотвратяване на инфекция с Pneumocystis jiroveci е дадена в съответствие с местната практика.

CISTANCHE ЩЕ ПОДОБРИ БЪБРЕЧНАТА/БЪБРЕЧНАТА НЕДОСТАТЪЧНОСТ
2.10. Анализи на публично достъпни масиви от данниПублично достъпните набори от данни бяха анализирани съгласно общи препоръки [24]. Данните за масив от човешки транскриптоми са показани като log2 медиано центрирани интензитети, извлечени от базата данни Nephroseq, включително Европейската бъбречна cDNA Biobank (ERCB) от 170 пациенти с ХБН и 31 здрави живи донори (номер за достъп GSE69438) [25].
2.11. Статистически методиПроменливите бяха тествани за нормално разпределение с помощта на теста на Shapiro-Wilk. Ненормално разпределените непрекъснати променливи се изразяват като медиана и интерквартилен диапазон (IQR), категориалните променливи се представят като честота и процент. Статистическите сравнения не са официално задвижвани или предварително определени. За сравнение между групите е използван тестът на Kruskal-Wallis. За групови сравнения беше използван U-тестът на Mann-Whitney за определяне на разликите в медианите. Непараметричните сравнения между групите бяха извършени с хи-квадрат теста на Pearson. Корелациите бяха анализирани с помощта на ранговия корелационен коефициент на Spear Man (ρ на Spearman) и анализите на данните бяха извършени с GraphPad Prism (версия 8.4.3 за macOS, GraphPad Software, Сан Диего, Калифорния, САЩ).
3. Резултати
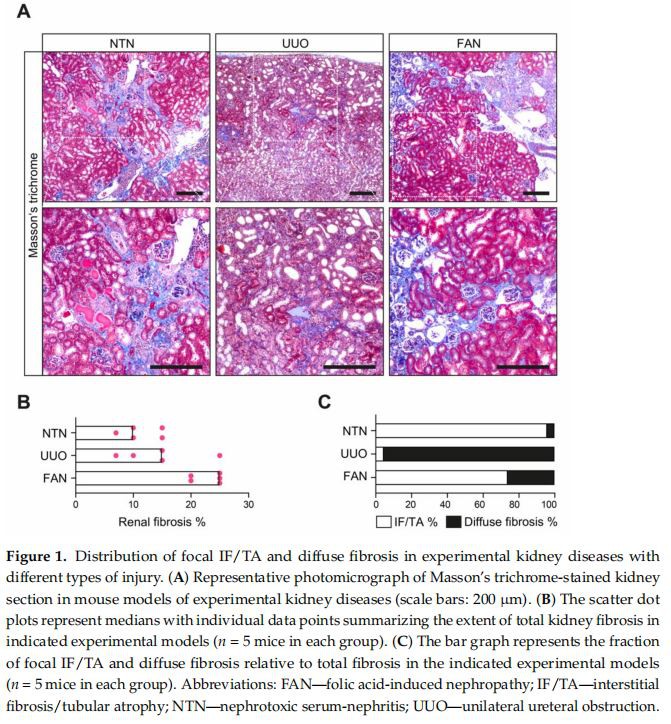
3.1. Увреждането на различни бъбречни отделения води до различни модели на бъбречна фиброзаЗа да изясним потенциалните механизми на основното заболяване при развитието на фокална IF/TA и дифузна фиброза в резултат на гломерулно или тубулно увреждане, първо предизвикахме мишки с експериментални модели на първично гломерулно увреждане, водещо до гломерулна склероза, индуцирана от нефротоксичен серумен нефрит (NTN) , дифузно тубулоинтерстициално увреждане, дължащо се на постренална недостатъчност с бъбречни хемодинамични и метаболитни промени, причинени от едностранна уретерална обструкция (UUO), и специфичен модел на тубулно увреждане, водещо до тубулна атрофия от индуцирана от фолиева киселина нефропатия (FAN, Фигура 1A) [26–28] ]. Бъбреците в тези експериментални модели наувреждане на бъбрецитебяха оценени чрез трихромно оцветяване на Masson, което разкрива, че хроничното гломерулно увреждане при NTN води до предимно фокален IF/TA в съседство с атрофични тубули (Фигура 1B,C и Таблица 1). За разлика от това, използването на UUO като модел на първично увреждане на тубулоинтерстициалното отделение със свързани възпалителни лезии разкрива дифузна фиброза като водещ модел на хронични лезии (Фигура 1B, C и Таблица 1). Интересно е, че FAN като модел на първично тубулно увреждане с последователна тубулна атрофия, независимо от хронично гломерулно увреждане, еднакво индуцира преобладаващо фокално IF/TA (Фигура 1B, C и Таблица 1), като по този начин подчертава ролята на тубулното увреждане и тубулната атрофия за развитието на този модел на фокална фиброза.

3.2. Разпространение на фокална IF/TA и дифузна фиброза при човешки патологииЗа да проверим дали различни модели на бъбречна фиброза са общи механизми за прогресиране на заболяването в отговор на хронично увреждане и наблюдавани при бъбречни патологии, след това анализирахме появата и разпространението на фокална IF/TA и дифузна фиброза при различни други хорабъбречни заболявания.В общ брой от 67 бъбречни биопсии с различни бъбречни патологии, включително гломерулонефрит, свързан с антинеутрофилни цитоплазмени антитела (ANCA GN), остър интерстициален нефрит (AIN), мембранозен GN, лупусен нефрит, хипертонична нефропатия, IgA нефропатия (IgAN), фокално-сегментна гломерулосклероза (FSGS) и диабетзаболяване на бъбреците(DKD), фокална IF/TA и дифузна фиброза могат да се наблюдават в различна степен (Фигура 2A–C и Таблица 2). Интересно е, че дифузната фиброза присъства предимно в случаи на ANCA GN, лупусен нефрит и IgAN катобъбречни заболяванияс гломерулно и интерстициално увреждане (Фигура 2C). Тези констатации предполагат, че различни модели на бъбречна фиброза присъстват при различни бъбречни патологии, включително ANCA GN, и че ANCA GN може да служи като модел на заболяване за изучаване на възпалителни и дегенеративни механизми на увреждане на различни бъбречни отделения [29].



3.3. Фокалната IF/TA и дифузната фиброза са показателни за увреждане на отделни бъбречни отделения при ANCA GNТъй като открихме, че различни модели на бъбречна фиброза присъстват при различни бъбречни патологии, включително ANCA GN като бъбречно заболяване с гломерулно и възпалително интерстициално увреждане с еднакво разпределение на фокална IF/TA и дифузна фиброза, ние анализирахме различни модели на бъбречна фиброза във връзка с клинични, лабораторни и хистопатологични находки в рамките на общ брой от 49 бъбречни биопсии с потвърден ANCA GN (Таблица 3) [30–36]. Степента на общата фиброза корелира с тежко влошаване на бъбречната функция, което се отразява чрез повишаване на серумния креатинин и загуба на скорост на гломерулна филтрация (GFR, Фигура 3B). Чрез систематично оценяване на ANCA GN, общата фиброза корелира с намалената фракция на нормалните гломерули, приписвана на ускорените полумесеци и глобалната гломерулна склероза (Фигура 3C). Сред възпалителните лезии, общата фифиброза корелира с общото възпаление при ANCA GN, което не е изрично приписано на интерстициално възпаление извън областите на IF/TA или възпаление в области на интерстициална фиброза и тубулна атрофия (i-IF/TA, Фигура 3C). След това разрязахме бъбречната фиброза на фокална IF/TA и дифузна фиброза, заобикаляща непокътнати тубули без видими признаци на тубулна атрофия за отделен анализ (Фигура 3D). Интересно е, че не наблюдавахме пряка корелация между фокална IF/TA и дифузна фиброза (Фигура 3E), което предполага различни характеристики на всяка лезия при ANCA GN. Както по-рано наблюдавахме за тотална фиброза, IF/TA корелира с намалена фракция на нормалните гломерули, което се дължи главно на глобалната гломерулна склероза (Фигура 3E), потвърждавайки установения механизъм, че хроничното гломерулно увреждане води до дегенерация на съответните тубули с тубулна атрофия и фокални фиброзни белези [4]. За разлика от това, дифузната фиброза не корелира с хронично гломерулно увреждане, а с полумесечни гломерули (Фигура 3E), което предполага, че дифузната фиброза (несвързана с тубулна атрофия) е в основата на все още неизвестни механизми, които са независими от хронично гломерулно увреждане и загуба на нефрон. Систематичното оценяване на бъбречното възпаление разкри, че дифузната фифиброза е специфично свързана с интерстициално възпаление в нефиброзни области (Фигура 3E), докато фокалното IF/TA корелира с общото кортикално възпаление, което не е специфично приписано на интерстициално възпаление или i-IF/TA ( Фигура 3E). Трябва да се отбележи, че и двете лезии корелират с по-тежко влошаване на бъбречната функция (Фигура 3F), което допълнително подкрепя наблюдението, че всяка лезия е съществен фактор за бъбречно увреждане и изход.


Фигура 3. Фокална IF/TA и дифузна фиброза са показателни за увреждане на различни бъбречни отделения при ANCA GN. (A) Представителна фотомикрография на оцветения с трихром бъбрек на Masson в ANCA GN (скала: 200 µm). (B) Връзката между общата бъбречна фиброза, клиничните и лабораторни находки при ANCA GN са показани чрез топлинна карта, отразяваща средните стойности на ρ на Spearman, звездичките показват p < 0.05.="" (c)="" връзката="" между="" общата="" бъбречна="" фиброза,="" гломерулните="" и="" възпалителните="" находки="" в="" anca="" gn="" са="" показани="" чрез="" топлинна="" карта,="" отразяваща="" средните="" стойности="" на="" ρ="" на="" spearman,="" звездичките="" показват="" p=""><0,05. (d)="" показана="" е="" представителна="" фотомикрография="" на="" трихромно="" оцветен="" бъбречен="" участък="" на="" masson="" в="" anca="" gn="" с="" фокална="" if/ta="" (горен="" панел)="" и="" дифузна="" фиброза="" (долен="" панел)="" (мащабни="" ленти:="" 40="" µm).="" (e)="" връзката="" между="" фокална="" if/ta="" и="" дифузна="" фиброза="" с="" гломерулни="" и="" възпалителни="" находки="" е="" илюстрирана="" чрез="" топлинна="" карта,="" отразяваща="" средните="" стойности="" на="" ρ="" на="" spearman,="" звездичките="" показват="" p=""><0,05. (f)="" връзката="" между="" фокална="" if/ta="" и="" дифузна="" фиброза="" с="" клинични="" и="" лабораторни="" находки="" в="" anca="" gn="" е="" показана="" чрез="" топлинна="" карта,="" отразяваща="" средните="" стойности="" на="" ρ="" на="" spearman,="" звездичките="" показват="" p=""><0,05. съкращения:="" anca="" gn—антинеутрофилно="" цитоплазмено="" антитяло="" гломерулонефрит;="" bvas—скор="" за="" активност="" на="" васкулит="" в="" бирмингам;="" crp—c="" реактивен="" протеин;="" gfr="" -="" скорост="" на="" гломерулна="" филтрация;="" if/ta—интерстициална="" фиброза/тубулна="" атрофия;="" iqr—интерквартилен="" диапазон;="" mpo-миелопероксидаза;="" acr—съотношение="" албумин/креатинин="" в="" урината;="" upcr="" -="" съотношение="" протеин/креатинин="" в="">
3.4. Анализът на фокална IF/TA спрямо дифузна фиброза разкрива различни състави на матрицатаСлед това анализирахме по-подробно морфологичните характеристики на фокалната IF/TA и дифузната фиброза в ANCA GN. Полутънките срезове разкриват, че фокалната IF/TA, заобикаляща атрофичните тубули, е по-кондензирана от рехаво подредената фиброзна тъкан, заобикаляща запазените интактни тубули (Фигура 4А). Трансмисионната електронна микроскопия (ТЕМ) изяснява колагенови снопове, вградени в гъсто опакован стромален матрикс (Фигура 4В). Обратно, ултраструктурният анализ на дифузната фиброза показва почти непокътнати тубули, заобиколени от разширена едематозна вътрешност с фокални колагенови снопове, разкриващи непълен вид фиброзна тъкан (Фигура 4B). Тези наблюдения предполагат, че фокалната IF/TA и дифузната бъбречна фиброза могат да се различават по отношение на състава и организацията на ECM.

3.5. Тубулоинтерстициален транскриптом във връзка с тубулна атрофия разкрива различни колагенови сигнатури при бъбречна фиброзаСлед това анализирахме състава на ECM, отразен от колагенови сигнатури в набори от данни за транскриптоми от микродисектирани тубулоинтерстициални компартменти при 170 пациенти с ХБН и 31 здрави живи донори (база данни Nephroseq) за връзка с установени маркери на тубулна атрофия, включително цитокератин -7 (кодиран от KRT7), -18 (KRT18) и -19 (KRT19) [25,37]. В тубулоинтерстициални компартменти с висока експресия на маркери за тубулно увреждане, колагените COL1A1, COL1A2, COL3A1, COL4A1, COL4A2, COL5A2, COL6A3, COL16A1 и COL18A1 бяха предимно експресирани (Фигура 5). Обратно, обратна корелация се наблюдава за COL2A1, COL5A3, COL6A1, COL8A2, COL11A1, COL11A2, COL17A1 и COL19A1 (Фигура 5). Тези резултати предполагат, че фиброзата на бъбреците може да има различни колагенови сигнатури в маркерите на тубулно увреждане.

3.6. Фокалното IF/TA е свързано с по-лош дългосрочен резултат при ANCA GNЗа да добием представа дали различни модели на бъбречна фиброза са свързани с дългосрочни бъбречни резултати, след това сравнихме общата, фокалната IF/TA и дифузната бъбречна фиброза при ANCA GN с развитието на ESKD. Тоталната бъбречна фиброза при ANCA GN корелира с по-лоши дългосрочни бъбречни резултати (Таблица 4). Интересно е, че само степента на фокална бъбречна фиброза корелира с бъбречните резултати (Таблица 4). За разлика от това, дифузната бъбречна фиброза не се свързва с дългосрочни бъбречни резултати (Таблица 4), което предполага, че различни модели на фиброза могат също да повлияят на прогресията на заболяването и потенциалния отговор на лечението.


Дискусия
Към днешна дата развитието на бъбречна фиброза може да се раздели на две концепции: от една страна, литературата предоставя солидни доказателства, че бъбречната фиброза е проста последица от необратимо увреждане на нефрона, поради хронично гломерулно или тубулно увреждане, като и двете са резултат при тубулна атрофия и фокална интерстициална фиброза около увредените нефрони [12,13]. По този начин фокалната IF/TA, свързана с тубулна атрофия, допринася за възстановяването на бъбреците, като служи като белези, като по този начин замества нефрони, които вече са загубени [12]. От друга страна, бъбречната фиброза може да се разглежда като активен, прогресиращ и увреждащ процес на ремоделиране на бъбречния интерстициум. В този процес фибробластите директно допринасят за увреждане на епитела, което предполага истински интерстициален механизъм на прогресиране на ХБН [13]. Доколкото ни е известно, това е първото проучване, което систематично разделя бъбречната фиброза на две различни и независими прояви с фокални или дифузни хистоморфологични модели, като по този начин изяснява два различни патогенни пътя на тези лезии. За да предоставим нови прозрения в областта на бъбречната фиброгенеза, развитието и съдбата на бъбречната фиброза, ние изследвахме три различни миши модела с известни образувания на бъбречна фиброза, за да разкрием фиброзни модели и прояви при увреждане на различни бъбречни отделения. Индуцирането на изолиран сърповиден GN в NTN и хроничното гломерулно увреждане води до предимно фокална фиброза в съседство с атрофични тубули [26]. Тези наблюдения подкрепят концепцията за необратимо увреждане на нефрона, което води до фокална IF/TA около увредените нефрони [12,13]. За разлика от това, използването на UUO като модел на първично увреждане на тубулоинтерстициалния компартмент със свързани възпалителни лезии разкрива дифузна фиброза като водещ модел на хронични лезии [27]. Бъбречната фиброза при UUO мишки се характеризира с деликатни колагенови влакна, обграждащи почти непокътнати тубули.
Интересно е, че интерстициумът на UUO мишки показва не само дифузна фиброза, но и изобилие от възпалителни клетки. Тъй като възпалението е отговор на нараняване, важно е да се обсъди дали интерстициалното възпаление е резултат от директно увреждане на интерстициалното отделение, независимо от съседния нефрон. Следователно дифузната фиброза е резултат от изолиран интерстициален нефрит без първично увреждане на бъбречния епителен паренхим, което може да възникне в по-късните етапи на прогресия на заболяването като тубулоинтерстициален нефрит и вероятно води до атрофични нефрони. Конгестията на урината в рамките на тубулната епителна система е основният виновник в UUO модела, което води до дифузна фиброза, бъбречна хемодинамика и метаболитни промени [27]. Тъй като всяко задръстване на паренхима води до оток на околния интерстициум, дифузното едематозно увреждане на бъбречния интерстициум може да обясни степента на възпалението и дифузната фиброза при UUO мишки. И накрая, FAN като модел на първично тубулно увреждане с последваща тубулна атрофия, независимо от хронично гломерулно увреждане, еднакво индуцира преобладаващ фокален IF/TA, като по този начин подчертава ролята на тубулното увреждане и тубулната атрофия за развитието на фокален IF/TA [28]. В този модел множество съседни нефрони изглежда са увредени от директна тубулна токсичност, което води до разширена тубулна атрофия без гломерулно увреждане.
След анализа на няколко бъбречни патологии, нашите данни също предполагат, че фокалната IF/TA и дифузната фиброза изглежда допринасят като хронични лезии при повечето бъбречни заболявания при хора. Фокалната IF/TA и дифузната фиброза присъстват главно в ANCA GN и подчертават постулирания механизъм на директно интерстициално увреждане като причина за дифузна фиброза. При ANCA GN като бъбречно заболяване с гломерулно увреждане (образуване на полумесец, гломерулна склероза и загуба на нефрон) и интерстициално увреждане (поради възпаление), ние тук предоставяме доказателства, че тубулоинтерстициалната фиброза е или свързана с увреждане на нефрона (зависимо или независимо от гломерулен белег) или първично интерстициално увреждане (водещо до дифузно фиброзно интерстициално ремоделиране) [22,38–41]. Освен това, нашите данни показват, че фокалната IF/TA при ANCA GN корелира с глобалната гломерулна склероза, което води до гломерулна склероза и загуба на нефрон [26]. Тук можем също така да разкрием, че фокалните бъбречни белези представляват централния модел на бъбречна фиброза, потвърждавайки голямо изобилие от литература, описваща, че хроничното гломерулно увреждане води до дегенерация на съответния тубул с тубулна атрофия, загуба на този специфичен нефрон и непълно възстановяване на бъбрека чрез фокален заместващ белег [12]. По този начин нашите данни потвърждават, че фокалната IF/TA е свързана с необратимо увреждане на нефроните, зависимо или независимо от гломерулно увреждане. Фокалните IF/TA модели в човешки биопсии изглеждат с подобен произход, отразявайки възстановяването на бъбреците. За разлика от това, дифузната фифиброза при ANCA GN е специфично свързана с интерстициално възпаление. Полутънки срезове разкриват фиброзна тъкан с рехаво подредени колагенови влакна, заобикалящи почти напълно непокътнати тубули без признаци на истинска атрофия. Трябва да се отбележи, че ТЕМ анализът показа много рядко подредени колагенови снопове в много слабо организиран интерстициум, което предполага едематозни интерстициални промени. Тъй като ANCA GN е васкулит, засягащ малки съдове, интерстициалното възпаление и дифузната фиброза могат да се обяснят поради интерстициален васкулит с придружено капилярно изтичане; по този начин отокът и интерстициалното възпаление влошават дифузната интерстициална фиброза [42].

CISTANCHE ЩЕ ПОДОБРИ БЪБРЕЧНАТА/БЪБРЕЧНАТА ДИАЛИЗА
Набори от транскриптомни данни от микродисектирани тубулоинтерстициални отделения разкриват различни колагенови сигнатури, свързани с фокална IF/TA, свързана с тубулна атрофия и дифузна фиброза, несвързана с тубулна атрофия, което предполага, че фокалната IF/TA и дифузната бъбречна фиброза могат да се различават в състава на ECM. Колагенът е основен изобилен фиброзен протеин в извънклетъчния матрикс. Колагените съставляват основния структурен елемент на ECM и осигуряват якост на опън, регулират клетъчната адхезия, поддържат хемотаксиса и миграцията и насочват развитието на тъканите [43]. Към днешна дата са описани 28 вида колаген. Основните типове колаген, открити в съединителната тъкан, са типове I, II, III, V и XI. В микродисектираните тубулоинтерстициални отделения, фокалната фифиброза, свързана с маркери на тубулна атрофия, съдържа предимно колаген типове I, III, IV и V. За разлика от това, ние идентифицирахме обратна корелация с колаген типове II и XI, което предполага, че фокалната IF/TA и дифузен бъбрек фиброзата може да се различава по различни колагенови подписи. И накрая, тук показваме, че общата бъбречна фиброза при ANCA GN корелира с по-лоши дългосрочни бъбречни резултати, както е описано по-рано [22]. Интересно е, че само степента на фокална бъбречна фиброза корелира с бъбречния резултат. За разлика от това, дифузната бъбречна фиброза не се свързва с дългосрочния бъбречен резултат. Тези наблюдения предполагат, че различни модели на фиброза могат също да повлияят върху прогресията на заболяването и потенциалния отговор на лечението.
Взети заедно, ние тук предоставяме доказателства, че по-голямата част от бъбречната фиброза изглежда е свързана със загуба на нефрони и заместващи белези, представляващи непълно възстановяване на тъканите. За разлика от това, дифузната фиброза изглежда е резултат от първично интерстициално възпаление и нараняване без увреждане на епителната част на бъбрека. Интересно е, че и двата модела на фиброза корелират с по-тежко влошаване на бъбречната функция, което предполага, че всяка интерстициална фиброзна лезия е съществен фактор за резултата. В същото време концепцията за загуба на функционален паренхим, водеща до фокална заместваща фиброза и дифузна фиброза, лежаща в основата на алтернативни механизми, все още не е систематично описана в бъбреците. Такива механизми обаче са докладвани при сърдечна фиброза. Заместителната фиброза (фиброзата на белега) е фокална и възниква след некроза на кардиомиоцитите, например след инфаркт на миокарда, и се счита за необратима, за да се предотврати разкъсване на сърдечния мускул след инфаркт [44]. От друга страна, дифузната фиброза е свързана с дифузно разпространение на извънклетъчен колаген без кардиомиоцитна некроза и се смята, че по принцип е обратима [45–48].
Основните ограничения на нашето проучване са ограниченият брой бъбречни биопсии при някои бъбречни патологии, неговият ретроспективен дизайн и ограничената възможност за прехвърляне на експериментални модели на бъбречно увреждане при хора. Въпреки това, нашата основна констатация, че фокалната IF/TA и дифузната фиброза са независими модели на бъбречна фиброза при ANCA GN (и други хронични бъбречни заболявания), предполага, че всяка лезия има различни характеристики и, вероятно, механизми при ANCA GN. Освен това, тези наблюдения допълнително разширяват настоящите ни познания за взаимодействието между възпаление, бъбречно увреждане и фиброза, като допринасят за по-точно разбиране на възпалителните реакции и потенциални нови терапевтични стратегии за модулиране на различни прояви на бъбречна фиброза
Изводи
В заключение, тук предоставяме доказателства, че фокалният модел на бъбречна фиброза изглежда е свързан със загуба на нефрон и заместващи белези. За разлика от дифузния модел на бъбреците фифиброзата изглежда е резултат от първично интерстициално възпаление и нараняване
