Хуморален имунитет срещу SARS-CoV-2 и въздействието върху патогенезата на COVID-19
Aug 23, 2023
Измина повече от година, откакто тежкият остър респираторен синдром коронавирус 2 (SARS-CoV-2) се появи за първи път. Много проучвания предоставиха представа за различните аспекти на имунния отговор на коронавирусната болест 2019 (COVID-19). Особено за лечение с антитела и разработване на ваксина, хуморалният имунитет към SARS-CoV-2 е изследван обстойно, въпреки че все още има много неизвестни и противоречиви неща. Тук въвеждаме ключови открития за хуморалните имунни отговори при COVID-19, включително имунната динамика на отговорите на антителата и корелациите с тежестта на заболяването, неутрализиращи антитела и тяхната кръстосана реактивност, колко време са антителата и отговорите на В-клетките на паметта последните, анормални автореактивни антитела, генерирани при пациенти с COVID{10}}, и ефикасността на наличните в момента терапевтични антитела и ваксини срещу циркулиращи варианти на SARSCoV-2 и подчертават пропуски в настоящите познания.
Ключови думи: COVID-19, хуморален имунитет, неутрализиращи антитела, варианти на SARS-CoV-2, SARS-CoV-2

cistanche tubulosa - подобряват имунната система
ВЪВЕДЕНИЕ
След първата поява на тежък остър респираторен синдром коронавирус 2 (SARS-CoV-2) през 2019 г. учените се опитаха да разкрият характеристиките на този вирус, който има опустошителни последици за човешкото здраве и икономиките по света. През изминалата година не само характеристиките на този нов вирус, но и патогенезата на коронавирусната болест 2019 (COVID-19) и имунните отговори, предизвикани в човешкото тяло, бяха обилно проучени, което доведе до разработването и прилагането на различни терапевтични възможности и ваксини. Въпреки че хуморалният имунитет е едно важно звено на защитния имунитет срещу вирусна инфекция, главно чрез производство на антитела, способни да неутрализират нахлуващите вируси, има много спорове относно ролята на хуморалните имунни отговори при COVID-19. В този мини-преглед представяме различни аспекти на хуморалния имунитет, които участват в защитата от или в патогенезата на COVID-19 и обсъждаме противоречивите открития, наблюдавани в различни групи, както и бъдещи насоки за текущи проблеми.

Cistanche ползи за мъжете - укрепване на имунната система
ХУМОРАЛЕН ИМУНИТЕТ КЪМ SARS-CoV-2 И ТЕЖЕСТ НА ЗАБОЛЯВАНЕТО
С тяхната способност за стерилизиращ имунитет, антителата са първата и най-осъществима цел за разработване на ваксина. За разлика от Т-клетъчния отговор, който е постоянно нарушен и броят на Т-клетките драстично намален при тежки пациенти с COVID{1}}, хуморалните отговори на SARS-CoV-2 и корелациите им с тежестта на заболяването са разнообразни. Няколко ранни доклада показват, че по-високите титри на антитела са свързани с тежки клинични прояви (Garcia-Beltran et al., 2021a; Hashem et al., 2020; Tan et al., 2020; Zhao et al., 2020). Проспективно проучване с 67 пациенти с COVID-19 показа, че анти-нуклеокапсиден протеин (NCP) IgM и IgG започват на ден 7 и ден 10 и достигат пик съответно на ден 28 и ден 49. В допълнение, тези антитела се появяват по-рано и техните титри са значително по-високи при тежки пациенти, отколкото при леки пациенти. Те също така установиха, че слабите отговорили за IgG имат значително по-висок процент на вирусен клирънс в сравнение с по-силните отговорили, което показва, че по-силният отговор на антитялото е свързан със забавен вирусен клирънс и тежест на заболяването (Tan et al., 2020). Друго проучване на 173 пациенти с инфекция със SARSCoV-2 също показа, че по-високият титър на антитялото е независимо свързан с по-лоша клинична класификация (Zhao et al., 2020). Тези проучвания повдигат възможността за патологичната роля на отговорите на антителата. Проучване на SARS-CoV инфекция при модел на макак показа влошаване на възпалението на белите дробове, предизвикано чрез антитяло-зависимо усилване (ADE) (Liu et al., 2019). Необходими са обаче всеобхватни проучвания, за да се обяснят клиничните корелати на отговорите на антителата и да се определи участието на ADE в тежки случаи на инфекция със SARS-CoV-2 (Arvin et al., 2020). С натрупването на всеобхватна кохорта от SARS-CoV-2 инфекции, динамиката на отговора на антителата и корелацията с тежестта изглеждат по-сложни. Анализът на функционалните хуморални траектории при хоспитализирани индивиди с умерено до тежко заболяване показа, че SARS-CoV-2 антиген-специфичните IgM и IgA са еволюирали почти еднакво във всички групи (Zohar et al., 2020). Развитието на S-специфичен IgG обаче се е случило по-рано и са наблюдавани по-високи титри на IgG при оцелели от тежко заболяване в сравнение с неоцелели, което показва, че бързото и мощно превключване на клас IgG е свързано с оцеляването (Zohar et al., 2020). Лукас и др. (2020) съобщават, че починалите пациенти не са имали по-високи общи хуморални отговори, включително анти-спайк IgG, анти-рецептор-свързващ домен (RBD) IgG и неутрализиращо антитяло (NAb), и са установили силен, но забавен отговор в сравнение с оцелелите . Те също предполагат, че генерирането на NAb преди 14 дни от началото на заболяването е ключов фактор за възстановяване (Lucas et al., 2020). Интересно е, че проучване, търсещо ранни фактори за предсказване на по-късни резултати от заболяването, разкрива, че специфичните за пика хуморални отговори са обогатени сред реконвалесцентни индивиди, докато функционалните отговори на антитела към нуклеокапсида са повишени при починали индивиди (Atyeo et al., 2020). Специфичните за пика фагоцитни и комплемент-фиксиращи дейности са обогатени рано при реконвалесценти, което показва, че тези специфични за шипа хуморални отговори може да са полезни за траекторията на SARS-CoV-2 инфекцията. Като цяло титрите на антитела, специфични за SARS-CoV-2, не просто корелират с тежестта на заболяването, но различните фактори, включително кинетиката на сероконверсията, изотипа на антителата и антигенната специфичност на антителата, трябва да се вземат предвид, за да се определи ефектът на хуморалния отговор върху тежестта на заболяването.

ползи от добавката Cistanche - повишава имунитета
НЕУТРАЛИЗИРАЩИ АНТИТЕЛА И КРЪСТОСАТА РЕАКТИВНОСТ
Неутрализирането е една от най-важните функции на антителата, предизвикващи стерилизиращ имунитет при вирусна инфекция. Повечето пациенти с положителен отговор на антитяло към SARSCoV-2 са показали неутрализираща активност, измерена чрез използване на псевдотипиран или автентичен SARS-CoV-2 вирус. Няколко проучвания са идентифицирали мощни NAbs срещу SARS-CoV-2 от реконвалесцентни пациенти с COVID-19 (Brouwer et al., 2020; Ju et al., 2020; Shi et al., 2020; Zost et al. , 2020 г.). NAb може да се свърже с нахлуващия вирус на мястото на RBD и други домейни на протеините на вирусния шип, предотвратявайки докинг на вируса към своя входен рецептор, ангиотензин-конвертиращ ензим 2 (ACE2). Проучване, изолиращо RBD-специфични моноклонални антитела от осем пациенти с COVID-19, разкрива връзка между неутрализиращата активност и конкуренцията с ACE2 за свързване на RBD (Ju et al., 2020). Анализът на кристалната структура на RBD-свързаното антитяло показа, че пространственото препятствие инхибира вирусното взаимодействие с ACE2. Това проучване установи също, че анти-SARS-CoV-2 антителата и заразената плазма не реагират кръстосано с RBDs на SARS-CoV или MERS-CoV, което предполага, че анти-RBD антителата са предимно специфични за вирусен вид инхибитори (Ju et al., 2020). Подобно проучване съобщава за изолирането на две специфични човешки моноклонални антитела от реконвалесцентен пациент, показващи мощна неутрализираща активност срещу SARS-CoV-2 in vitro и при маймуни резус (Shi et al., 2020). Структурният анализ разкрива, че моноклоналното антитяло се свързва с епитопите, съответстващи на частта, припокриваща се с ACE2-свързващите места в RBD, което пречи на взаимодействията вирус-рецептор чрез пространствено препятствие и директна конкуренция. За следващата стъпка много изследователски групи се опитаха да изолират голям брой човешки моноклонални антитела, способни да неутрализират SARS-CoV-2 и да идентифицират епитопи, взаимодействащи с тези моноклонални антитела, тъй като тези антитела ще бъдат обещаващи кандидати за COVID{{ 36}} лечение и профилактика. Те също така предоставят успешни стратегии за разработване на ваксина срещу SARS-CoV-2 (Barnes et al., 2020; Cao et al., 2020; Liu et al., 2020). Въпреки че са докладвани голям брой проучвания, изследващи хуморалните имунни отговори в серума, няколко проучвания са фокусирани върху отговора на антителата в респираторната лигавица, където навлиза SARS-CoV-2. Секреторният IgA е най-разпространеният изотип на антитяло в мукозните повърхности и е добре известен с това, че има мощна неутрализираща активност. Скорошно проучване измерва SARS-CoV-2-специфичните IgA антитела в серума, слюнката и бронхоалвеоларната течност на 159 пациенти с COVID-19 и установи, че IgA антителата преобладават в ранната фаза на SARS-CoV{ {49}} инфекция (Sterlin et al., 2021). Освен това, IgA от серумни и мукозни повърхности допринася за неутрализацията на вируса в по-голяма степен от IgG. По подобен начин, друго проучване установи, че IgA димерите, първичната форма на антитяло в мукозните повърхности, имат почти 15- пъти по-мощна неутрализация от IgA мономера, доминиращата форма в серума, и мономерът е 2-кратно по-малко мощен от IgG еквивалентите (Wang et al., 2021a). Друг момент, на който трябваше да се обърне внимание, беше дали плазмата или NAbs, получени от други коронавируси, имат неутрализираща активност срещу SARS-CoV-2, тъй като те могат да осигурят незабавна защита за тежки пациенти с COVID-19 и са друга възможност за разработване на универсални ваксини за силно вирулентен коронавирус (Pinto et al., 2020; Tian et al., 2020; Zhu et al., 2020). Няколко моноклонални антитела, идентифицирани от В-клетките на паметта на индивид, заразен със SARS-CoV през 2003 г., са насочени към шиповия протеин на SARS-CoV-2, който споделя 80% идентичност на аминокиселинната последователност с шиповия протеин на SARS-CoV ( Пинто и др., 2020 г.). Обратно, антитела с неутрализираща активност срещу SARS-CoV-2, изолирани от COVID-19 реконвалесцентни индивиди, също кръстосано неутрализират SARS-CoV и MERS-CoV (Zhang et al., 2021). Степента на кръстосана реактивност между човешки коронавируси (HCoVs) и SARS-CoV-2 е широко изследвана, но е довела до противоречиви констатации (Anderson et al., 2021; Ng et al., 2020; Nguyen-Contant et al. ., 2020 г.; Постън и др., 2020 г.; Сонг и др., 2020 г.). С помощта на метод, базиран на поточна цитометрия, SARSCoV-2 спайк протеин-реактивни антитела са открити в SARS-CoV-2-неинфектирани индивиди (Ng et al., 2020). SARS-CoV-2-неинфектирани донорски серуми, включително тези S2-насочени IgG клас антитела, показаха специфична неутрализираща активност срещу SARS-CoV-2 и SARS-CoV-2 S псевдотипове. Тези съществуващи антитела са по-чести при деца и юноши (Ng et al., 2020), което предполага възможност по-високите нива на инфекция с HCoV (коронавируси на обикновена настинка) при деца, отколкото при възрастни, да корелират с относително по-леки симптоми при деца с COVID{{ 98}} (Castagnoli et al., 2020). За разлика от това, други проучвания съобщават за ограничени вече съществуващи кръстосано реактивни антитела срещу SARS-CoV-2 при неизложени индивиди (Nguyen-Contant et al., 2020; Poston et al., 2020; Song et al., 2020 ). По-конкретно, само S{108}}насочено IgG антитяло беше открито и имаше известна неутрализираща активност, докато анти-RBD IgG антитялото липсваше при неекспонирани индивиди, въпреки че те откриха съществуващи кръстосано реактивни В клетки на паметта, които бяха активирани при SARS- CoV-2 инфекция. Освен това някои хора в група преди пандемия са имали кръстосано реактивни антитела срещу SARS-CoV-2, но те не са нито неутрализиращи, нито предпазващи срещу SARS-CoV-2 инфекция (Anderson et al., 2021) . Необходими са допълнителни проучвания, за да се разбере как кръстосаната реактивност между различни коронавируси влияе върху хода и патогенезата на инфекцията с друг коронавирус.

растение цистанче, повишаващо имунната система
ДЪЛГОЛЕТНОСТ НА ОТГОВОРА НА АНТИТЕЛАТА И В-КЛЕТКИТЕ НА ПАМЕТТА
Дълготрайността на отговора на имунната памет е от решаващо значение за защитата от повторно заразяване с патогени. Все още трябва да се натрупат повече данни за по-дълги периоди, но има няколко противоречиви доклада за това колко дълго могат да се поддържат отговорите на антитела срещу SARS-CoV-2 при пациенти с COVID-19 (Duysburgh et al., 2021 г. ; Gudbjartsson et al., 2020; Ibarrondo et al., 2020; Roltgen et al., 2020a; 2020b; Seow et al., 2020; Wajnberg et al., 2020). Някои проучвания показват, че повечето антитела срещу SARS-CoV-2 остават стабилни в продължение на няколко месеца след инфекцията, докато други проучвания установяват бързо намаляване на титрите на антителата в рамките на 3-4 месеца. Интересно е, че намаляването на анти-SARS-CoV-2 IgA антителата изглежда се влияе по-малко от други изотипове, включително IgM и IgG антитела (Gaebler et al., 2021). Предизвикателство е да се отговори на причината, поради която тези проучвания показват различни резултати. В някои проучвания е установено бързо намаляване на титрите на антителата срещу SARS-CoV-2 при пациенти с COVID-19 с леки симптоми или асимптоматични индивиди, което предполага, че дълготрайността на отговорите на антителата корелира с тежестта на заболяването (Roltgen et al., 2020a; 2020b; Seow et al., 2020). Тези констатации също предполагат, че е необходимо засилване на приложението на ваксината за дълготрайна защита. Въпреки че дълготрайността на антителата срещу SARS-CoV-2 все още не е ясна, беше установено, че специфичните за SARS-CoV-2- В-клетки на паметта персистират 3-6 месеца (Gaebler et al., 2021; Hartley et al., 2020; Rodda et al., 2021). В проучването на групата на Nussenzweig, въпреки че титрите на IgM и IgG анти-SARS-CoV-2 RBD антитела значително намаляват и капацитетът за неутрализиране намалява с времето, броят на RBD-специфичните В клетки на паметта не се променя до 6 месеца след инфекция (Gaebler et al., 2021). Освен това, хуморалният отговор в тази кохорта продължи да се развива, тъй като антителата от В клетките на паметта претърпяха голяма соматична хипермутация в съответствие с персистирането на SARS-CoV-2 в тънките черва (Gaebler et al., 2021). От 11 сдвоени проби от пациенти с COVID-19 между 4 и 242 дни след появата на симптомите, RBD и NCP-специфичните В клетки на паметта продължават да нарастват до 150 дни, а броят на RBD-специфичните IgG+ В клетки на паметта значително корелира с броя на циркулиращите фоликуларни хелперни Т клетки (Hartley et al., 2020). По-скорошно проучване изследва фенотипа на В-клетките на паметта при леки и тежки пациенти с COVID-19 до 6 месеца след инфекцията (Sokal et al., 2021). Използвайки надлъжен анализ на една клетка и репертоар, В-клетъчният отговор срещу SARS-CoV-2 показа временно превключване от екстрафоликуларна реакция към зависим от зародишния център отговор на паметта, генериращ анти-RBD NAbs. По-специално, кръстосано реактивните В-клетки на паметта срещу коронавирусите на обикновената настинка допринасят за ранния екстрафоликуларен отговор на антитела срещу SARS-CoV-2. Тези открития предполагат, че устойчивостта и еволюцията на В-клетките на паметта допринасят за функционалната имунологична памет, която осигурява защита при повторно излагане на вируса и осигурява основа за ефективна ваксинация.
ГЕНЕРИРАНЕ НА АВТОАНТИТЕЛА ПРИ COVID-19
Автоантитела, насочени срещу протеини на гостоприемника, могат да предизвикат смущение в имунната система на гостоприемника. Съобщава се, че тежки възпалителни състояния, като хронична вирусна инфекция, повишават разпространението на автоантитела. Няколко проучвания показват, че пациентите с COVID{{0}}, особено лицата с тежки симптоми, имат по-високо разпространение на автоантитела срещу различни протеини на гостоприемника (Bhadelia et al., 2021; Wang et al., 2020; Woodruff et др., 2020a; Zuniga и др., 2021). По-високи нива на анти-Анексин А2 антитела са открити сред хоспитализирани пациенти с COVID-19, които са починали, в сравнение с некритични хоспитализирани пациенти с COVID-19 (Zuniga et al., 2021). Използвайки техниката за откриване на автоантитела с висока производителност, Wang et al. (2020) установиха, че пациентите с COVID-19 имат драстично повишена реактивност на автоантитела в сравнение с неинфектираните контроли. Тези автоантитела са срещу имуносвързани протеини, включително цитокини, хемокини, компоненти на комплемента и протеини на клетъчната повърхност. Те също така показаха, че автоантителата, насочени към тъканно-свързаните антигени, корелират с тежестта на заболяването и клиничните характеристики на възпалението при пациенти с COVID-19. Друго проучване идентифицира активирането на екстрафоликуларни В-клетки при критично болни пациенти и тези В-клетки споделят характеристиките на В-клетъчния репертоар, описани по-рано в автоимунни настройки, като системен лупус еритематозус (SLE) (Woodruff et al., 2020b). Автоантитела срещу интерферони тип I (IFN) са докладвани при най-малко 101 от 987 (10,2%) пациенти с животозастрашаваща COVID-19 пневмония, докато нито един от индивидите с асимптоматичен или лек SARS-CoV-2 инфекция и само 4 от 1227 (0,33%) здрави индивиди преди пандемията са имали автоантитела срещу тип I IFNs (Bastard et al., 2020). Тези автоантитела имаха неутрализираща активност срещу тип I IFN и тяхната способност да блокират SARS-CoV-2 инфекция in vitro. Трябва да се отбележи, че 94% от пациентите с тези автоантитела са мъже. Като цяло изглежда, че наличието на автоантитела срещу протеини на гостоприемника при SARS-CoV-2 инфекция корелира с тежестта на COVID-19, но дали тези автоантитела ще доведат до автоимунно заболяване и как влияят върху естествения ход на SARS-CoV-2 инфекция остава неизвестна.

Ползи от добавката Cistanche - как да подсилим имунната система
Щракнете тук, за да видите продуктите Cistanche Enhance Imunity
【Попитайте за повече】 Имейл:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Полизахаридите на Cistanche tubulosa могат да стимулират пролиферацията на Т и В лимфоцити, но пролиферативният ефект на В лимфоцитите е значително по-силен от този на Т лимфоцитите. Полизахаридите на Cistanche deserticola насърчават освобождаването на цитокин IL22 от лимфоцитите, което е свързано с насърчаване на пролиферацията на лимфоцити в далака. Cistanche deserticola може да активира макрофагите и да регулира имунната система. Полизахаридите на Cistanche deserticola, ехиназидът и пилозидът имат значителни ефекти върху образуването и активността на човешките лимфоцити. Може да увеличи реакцията на пролиферация на лимфоцитите, като по този начин засили имунната функция на тялото.

екстракт от цистанче
Функционалните компоненти на общите гликозиди на Cistanche tubulosa имат значително въздействие върху възстановяването на клетките след радиационно увреждане от 60Coy и могат също така да подобрят имунната функция срещу радиационно увреждане.
Екстрактът от Cistanche tubulosa може не само да компенсира вродения имунен дефицит, но и да засили придобития имунитет.
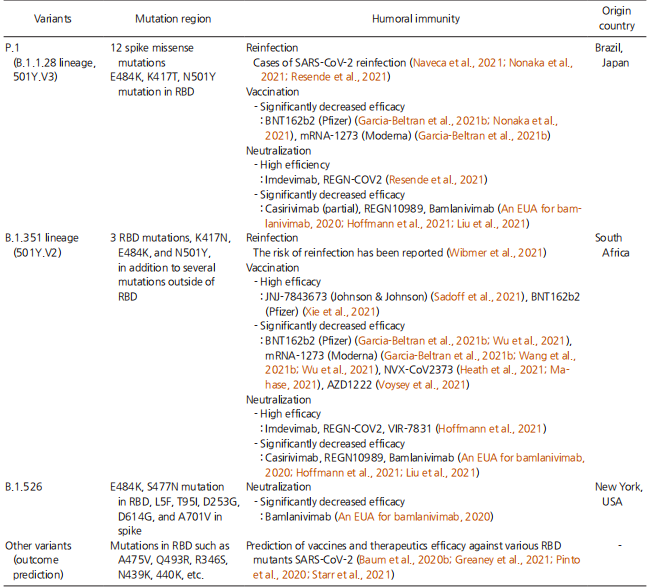
ЕФИКАСНОСТ НА ТЕКУЩИТЕ ТЕРАПЕВТИЦИ И ВАКСИНИ НА БАЗА НА АНТИТЕЛА СРЕЩУ ВАРИАНТИ НА SARS-CoV-2
Strains of SARS-CoV-2 with a mutation in the spike protein were officially identified recently and are spreading rapidly worldwide (Fig. 1). Their altered transmissibility and impaired response to vaccination are increasing social anxiety. The first variant that emerged is D614G, which was first discovered in Germany at the end of February 2020. This has higher transmissibility than the wild-type virus (Wuhan) and became the world's most dominant virus at the end of March 2020 (Korber et al., 2020). In June 2020, B.1.1.298 was identified in Denmark, a SARS-CoV-2 variant that causes transmission between mink and humans (Oude Munnink et al., 2021). Consequently, 17 million minks were killed to prevent interspecies transmission and the evolution of mutated viruses via mink (Oxner, 2020). Many variants with mutations in the RBD region have since been reported (Fig. 1, Table 1). Such a mutation is markedly resistant to certain spike protein monoclonal antibodies (Li et al., 2020) and has the potential to escape antibody recognition (Greaney et al., 2021). At the end of 2020, the B.1.1.7 variant harboring both the N501Y and D614G mutations in the RBD was reported in the UK (Claro et al., 2021; Galloway et al., 2021). This strain exhibits a greater transmission capacity than the D614G variant (Santos and Passos, 2020). To overcome this situation, there is an increasing need for research on whether current vaccines and therapeutics are effective against variants. The mRNA vaccines, including BNT162b2 (Pfizer) and mRNA- 1273 (Moderna), which were manufactured based on SARSCoV-2 isolated early in the epidemic from Wuhan, China, have demonstrated >94% ефикасност при предотвратяване на COVID-19 във фаза 3 проучване и са одобрени съгласно Разрешение за спешна употреба (EUA) от Американската администрация по храните и лекарствата (FDA) (Polack et al., 2020). След появата на варианти е тествана ефикасността на ваксините срещу тях, разкривайки висока ефикасност срещу D614G (Европа) (Garcia-Beltran et al., 2021b; Mahase, 2021; Muik et al., 2021), B.1.1. 7 (UK) (Garcia-Beltran et al., 2021b; Heath et al., 2021; Hoffmann et al., 2021; Muik et al., 2021; Wang et al., 2021b; Wu et al., 2021), B.1.1.298 (Дания) (Garcia-Beltran et al., 2021b) и B.1.429 (САЩ) (Garcia-Beltran et al., 2021b), но значително намалена ефикасност за варианти, съдържащи мутация в RBD, като E484K (Garcia-Beltran et al., 2021b; Hoffmann et al., 2021; Wang et al., 2021b; Wu et al., 2021). Някои моноклонални антитела, включително REGNCOV2 и Bamlanivimab, имат сходни резултати по отношение на ефикасността (EUA за bamlanivimab, 2020; Garcia-Beltran et al., 2021b; Hoffmann et al., 2021; Liu et al., 2021; Muik et al. др., 2021). Следователно, тези резултати предполагат, че някои RBD мутации могат да имат основен ефект върху ефикасността на неутрализацията. В скорошни проучвания са докладвани методи за скрининг на ефикасността на моноклоналните антитела за минимизиране на избягването на мутация на SARS-CoV-2. Баум и др. (2020b) демонстрира, че терапията с коктейл от антитела може да бъде ефективен начин за минимизиране на избягването на мутации от SARS-CoV-2. Грини и др. (2021) и Starr et al. (2021) напълно картографират RBD мутации, които избягват свързването от определени неутрализиращи антитела, чрез установяване на система за показване на дрожди. Тези изследвания ще допринесат силно за откриването на ваксини и лекарства, които имат широк неутрализиращ потенциал срещу избягали мутанти. Избухванията на варианти на SARS-CoV-2 вероятно ще продължат дълго време. Следователно бъдещите изследвания ще изискват специални усилия за непрекъснато проследяване на вариантите и намиране на ефективни начини за предотвратяването им. Освен това трябва да се стремим да изградим система, която може да реагира бързо на неочаквани мутации на вируса.

Фиг. 1. Глобална поява на варианти на SARS-CoV-2. Местоположението и датата на първото огнище на всеки вариант на SARS-CoV-2, включително D614G (Германия), B.1.1.298 (Дания), B.1.427/429 (Калифорния), B.1.351 (501Y. Показани са V2, Южна Африка), B.1.526 (Ню Йорк), B.1.1.7 (501Y. V1, Обединеното кралство), P.1 и P.2 (Бразилия и Япония). Дадените препратки са първите съобщения за появата на съответния вариант.
Таблица 1. Ефикасност на ваксини срещу COVID-19 и неутрализиращи антитела срещу SARS-CoV-2 варианти

ЗАКЛЮЧИТЕЛНИ БЕЛЕЖКИ
Досега тази опустошителна пандемия е довела до 130 милиона случая и 2,84 милиона смъртни случая от COVID-19 по целия свят. През изминалата година бяха генерирани значителни научни познания относно характеристиките на новия SARS-CoV-2, както и имунните отговори на гостоприемника, които са съществено включени в патогенезата на COVID-19. Прегледахме ключови открития относно хуморалните имунни отговори при COVID-19, които формират основата на наличните в момента терапии, включително моноклонални антитела и ваксини. Подобно на други вирусни инфекции, отговорите на антитела срещу SARS-CoV-2 са важни за неутрализацията и бързото изчистване на вируса, но техните въздействия са по-сложни, отколкото очаквахме, като участие в патогенезата и тежестта на COVID{{10} }. Динамиката на отговорите на антителата, кръстосаната реактивност на NAbs, дълготрайността на антителата и В-клетките на паметта и генерирането на автоантитела колективно влияят върху патогенезата и тежестта на COVID-19. Нещо повече, с развитието на вируса бързо се появяват няколко варианта на SARS-CoV-2, които реагират по-малко на настоящите терапии. Следователно са необходими допълнителни проучвания, за да се преодолеят пропуските в текущите знания и да се намери ефективен начин за подготовка за възникващи заплахи.
ПРЕПРАТКИ
EUA за бамланивимаб – моноклонално антитяло за COVID-19. (2020 г.). Med. Lett. Лекарства Ther. 62, 185-186.
Anderson, EM, Goodwin, EC, Verma, A., Arevalo, CP, Bolton, MJ, Weirick, ME, Gouma, S., McAllister, CM, Christensen, SR, Weaver, J., et al. (2021 г.). Сезонните човешки коронавирусни антитела се подсилват при инфекция със SARSCoV-2, но не са свързани със защита. Клетка 184, 1858-1864. e10.
Annavajhala, MK, Mohri, H., Zucker, JE, Sheng, Z., Wang, P., GomezSimmonds, A., Ho, DD и Uhlemann, AC (2021). Нов вариант на SARS-CoV-2, който предизвиква безпокойство, B. 1.526, беше идентифициран в Ню Йорк. MedRxiv, https://doi. org/10.1101/2021.02.23.21252259
Arvin, AM, Fink, K., Schmid, MA, Cathcart, A., Spreafico, R., HavenarDaughton, C., Lanzavecchia, A., Corti, D. и Virgin, HW (2020). Гледна точка за потенциалното антитяло-зависимо усилване на SARSCoV-2. Nature 584, 353-363.
Atyeo, C., Fischinger, S., Zohar, T., Slein, MD, Burke, J., Loos, C., McCulloch, DJ, Newman, KL, Wolf, C., Yu, J., et al. (2020 г.). Различни ранни серологични сигнатури проследяват оцеляването при SARS-CoV-2. Имунитет 53, 524-532.e4.
Baden, LR, El Sahly, HM, Essink, B., Kotloff, K., Frey, S., Novak, R., Diemert, D., Spector, SA, Rouphael, N., Creech, CB, et al. (2021 г.). Ефикасност и безопасност на иРНК-1273 SARS-CoV-2 ваксината. Н. англ. J. Med. 384, 403-416.
Barnes, CO, Jette, CA, Abernathy, ME, Dam, KA, Esswein, SR, Gristick, HB, Malyutin, AG, Sharaf, NG, Huey-Tubman, KE, Lee, YE и др. (2020 г.). SARS-CoV-2 структури на неутрализиращи антитела информират терапевтичните стратегии. Nature 588, 682-687.
Бастард, П., Розен, Л. Б., Джан, К., Михайлидис, Е., Хофман, Х. Х., Джан, Й., Доргам, К., Филипот, К., Розейн, Дж., Безиат, В. и др. . (2020 г.). Автоантитела срещу IFN тип I при пациенти с животозастрашаващ COVID-19. Наука 370, eabd4585.
Баум, А., Аджитдос, Д., Копин, Р., Джоу, А., Ланца, К., Негрон, Н., Ни, М., Уей, Й., Мохамади, К., Мусер, Б., и др. (2020a). Антителата REGN-COV2 предотвратяват и лекуват SARS-CoV-2 инфекция при макаци резус и хамстери. Наука 370, 1110-1115.
Baum, A., Fulton, BO, Wloga, E., Copin, R., Pascal, KE, Russo, V., Giordano, S., Lanza, K., Negron, N., Ni, M. и др. . (2020b). Коктейлът от антитела към шиповия протеин на SARSCoV-2 предотвратява бързото избягване на мутации, наблюдавано при отделни антитела. Наука 369, 1014-1018.
Bhadelia, N., Belkina, AC, Olson, A., Winters, T., Urick, P., Lin, N., Rifkin, I., Kataria, Y., Yuen, RR, Sagar, M. и др. . (2021 г.). Различни сигнатури на автоимунни антитела между хоспитализирани пациенти с остър COVID-19, SARS-CoV-2 реконвалесцентни индивиди и неизложени контроли преди пандемия. MedRxiv,https://doi.org/10.1101/2021.01.21.21249176
Brouwer, PJM, Caniels, TG, van der Straten, K., Snitselaar, JL, Aldon, Y., Bangaru, S., Torres, JL, Okba, NMA, Claireaux, M., Kerster, G., et al. (2020 г.).
Мощни неутрализиращи антитела от пациенти с COVID{0}} определят множество цели на уязвимост. Наука 369, 643-650.
Cao, Y., Su, B., Guo, X., Sun, W., Deng, Y., Bao, L., Zhu, Q., Zhang, X., Zheng, Y., Geng, C., и др. (2020 г.). Мощни неутрализиращи антитела срещу SARS-CoV-2, идентифицирани чрез високопроизводително едноклетъчно секвениране на В-клетки на реконвалесцентни пациенти. Клетка 182, 73-84.e16.
Castagnoli, R., Votto, M., Licari, A., Brambilla, I., Bruno, R., Perlini, S., Rovida, F., Baldanti, F. и Marseglia, GL (2020). Инфекция с коронавирус 2 на тежък остър респираторен синдром (SARS-CoV-2) при деца и юноши: систематичен преглед. JAMA Pediatr. 174, 882-889.
Chen, P., Nirula, A., Heller, B., Gottlieb, RL, Boscia, J., Morris, J., Huhn, G., Cardona, J., Mocherla, B., Stosor, V. и др. ал. (2021 г.). SARS-CoV-2 неутрализиращо антитяло LY-CoV555 при амбулаторни пациенти с Covid-19. Н. англ. J. Med. 384, 229-237.
Claro, IM, da Silva Sales, FC, Ramundo, MS, Candido, DS, Silva, CAM, de Jesus, JG, Manuli, ER, de Oliveira, CM, Scarpelli, L., Campana, G., et al. (2021 г.). Локално предаване на SARS-CoV-2 линия B.1.1.7, Бразилия, декември 2020 г. Emerg. заразявам. дис. 27, 970-972.
Collier, DA, De Marco, A., Ferreira, I., Meng, B., Datir, R., Walls, AC, Kemp, SS, Bassi, J., Pinto, D., Fregni, CS, et al. (2021 г.). Чувствителност на SARS-CoV-2 B.1.1.7 към иРНК антитела, предизвикани от ваксината. Nature 2021, 11 март [Epub].https://doi.org/10.1038/s41586-021-03412-7
Deng, X., Garcia-Knight, MA, Khalid, MM, Servellita, V., Wang, C., Morris, MK, Sotomayor-Gonzalez, A., Glasner, DR, Reyes, KR, Gliwa, AS, и др. . (2021 г.). Предаване, инфекциозност и неутрализиране на антитела на възникващ вариант на SARS-CoV-2 в Калифорния, носещ L452R шипова протеинова мутация. MedRxiv,https://doi.org/10.1101/2021.03.07.21252647
Duysburgh, E., Mortgat, L., Barbezange, C., Dierick, K., Fischer, N., Heyndrickx, L., Hutse, V., Thomas, I., Van Gucht, S., Vuylsteke, B. , et al. (2021 г.). Устойчивост на IgG отговор към SARS-CoV-2. Lancet Infect. дис. 21, 163-164.
Фариа, Н.Р., Мелън, Т.А., Уитакър, С., Кларо, И.М., Кандидо, ДДС, Мишра, С., Криспим, МАЕ, Продажби, Ф.К., Хаврилук, И., Маккроун, Дж.Т., и др. (2021 г.). Геномика и епидемиология на нова SARS-CoV-2 линия в Манаус, Бразилия. MedRxiv, https://doi.org/10.1101/2021.02.26.21252554
