Молекулярно клониране и биохимично характеризиране на нова кумарин гликозилтрансфераза CtUGT1 от Cistanche Tubulosa
Mar 17, 2022
за повече информация:ali.ma@wecistanche.com
Xiping Xu и др
РЕЗЮМЕ
UDP-гликозилтрансферазите (UGT) са важно и функционално разнообразно семейство от ензими, участващи във вторичната метаболитна биосинтеза. Кумаринът е един от най-разпространените скелети на природни продукти с кандидат-фармакологична активност. Въпреки това, към днешна дата много докладвани GTs от растения разпознават главно флавоноидите като акцептори на захар. Само ограничени GT могат да катализират гликозилирането на кумарини. В това проучване е клониран нов UGT отCistanche tubulosa, ценна традиционна тонизираща китайска билка, която изобилства от различни гликозиди като фенилетаноидни гликозиди, лигнанови гликозиди и иридоидни гликозиди. Подравняването на последователностите и филогенетичният анализ показаха товаCtUGT1е филогенетично отдалечен от повечето докладвани флавоноидни UGTs и съседен на фенилпропаноидни UGTs. Обширни in vitro ензимни анализи установиха, че въпреки чеCtUGT1не са участвали в биосинтезата на биоактивни гликозиди вCistanche tubulosa, може да катализира глюкозилирането на кумарини умелиферон 1, ескулетин 2 и химекромон 3 със значителен добив. Гликозилираните продукти бяха идентифицирани чрез сравнение с референтните стандарти или NMR спектроскопия и резултатите показват, чеCtUGT1може региоспецифично да катализира глюкозилирането на хидроксилни кумарини в C7- OH позиция. Ключовите остатъци, които определятCtUGT1Дейността на е допълнително обсъдена въз основа на хомологично моделиране и молекулярни докинг анализи. В комбинация с резултати от насочена към място мутагенеза, беше установено, че H19 играе незаменима роля като решаваща основа за катализа.CtUGT1може да се използва в ензимното получаване на биоактивни кумаринови гликозиди.
Ключови думи:Растителни гликозилтрансферази, кумаринови гликозиди,Cistanche tubulosa, Хомоложно моделиране, Сайт-насочена мутагенеза

Щракнете, за да получите полезни продукти за екстракт от цистанче
Въведение
Гликозилирането е един от най-разпространените видове структурни модификации на вторични природни продукти. Гликозилирането може да промени стабилността и/или разтворимостта на агликона и да допринесе много за разнообразието от естествени/неестествени продукти поради множеството типове конюгация. В растенията тези реакции обикновено се провеждат от зависими от уридин дифосфат (UDP) гликозилтрансферази (UGT), вид ензими, които катализират прехвърлянето на монозахаридни части от активирана нуклеотидна захар към молекула на гликозил акцептор, която може да бъде въглехидрат, гликозид, олигозахарид , или полизахарид [1,2]
Към днешна дата много гени, кодиращи UGT, са изолирани от няколко растения [3]. Гликозилирането се случва главно при хидроксилни групи или карбоксилни групи на широк спектър от вторични продукти, като флавоноиди [4], фенилпропаноиди [5], терпеноиди [6], стероиди [7], алкалоиди [8] и т.н. Кумарините са метаболити на фенилпропаноиди, широко разпространени в много растителни видове. Естествено срещащите се кумарини често съществуват като гликоконюгати и тези производни показват широк спектър от фармакологични действия, включително антиоксидант [9], антивирусен [10,11], хепатопротективен [12], противовъзпалителни [13], противоракови [14] ], антимутагенни [15] и инхибиторни активности на холинестераза (ChE) и моноаминооксидаза (МАО) [14,15] и т.н. Въпреки това, към днешна дата, в сравнение с най-често докладваните и обстойно изследвани флавоноиди UGT, само ограничени UGT са били се съобщава, че могат да прехвърлят захарната част към кумарини [16–18].
Растенията, богати на различни гликозиди, могат да служат като идеален генофонд на UGTs с нови катализни дейности. Освен това се съобщава, че множество UGT притежават значителна акцепторна промискуитетност, за да катализират гликозилирането на множество субстрати, някои от които дори не са разделени в растенията [19]. В тази статия, нова гликозилтрансферазаCtUGT1е идентифициран отCistanche tubulosa, традиционна лечебна билка, която изобилства от различни гликозиди като фенилетаноидни гликозиди (PhGs), лигнанови гликозиди и иридоидни гликозиди. Хетероложната експресия и характеристиката на функцията показват, че макар и рекомбинантенCtUGT1не е участвал в биосинтезата на тези гликозиди вCistanche tubulosa, той може да катализира глюкозилирането на хидроксилни кумарини и реакцията региоспецифично се случва на 7- OH позицията на кумарини умелиферон 1, ескалиращ 2 и химкромон 3, за да се произведат три фармакологично активни съединения обезмасляване (1а), цихориин (2а) и 4-метилумбелиферил глюкозид (3а) съответно със значителен добив. В допълнение, бензофеноновият субстрат 4,4′-дихидрокси бензофенон (4), изофлавоновият субстрат генистеин (5) и антрахиноновият субстрат алое-емодин (6) също могат да бъдат приети отCtUGT1. Каталитичните свойства и ключовите остатъци, подчертаващи способността за катализиране наCtUGT1също бяха оценени въз основа на моделиране на хомология, анализ на AutoDock и насочена към място мутагенеза.
2. Експериментален
2.1. Растителен материал и химикали
Cistanche tubulosaизползван в това проучване е събран от пустинни райони в автономните региони Хетян, Синцзян. Тяхната ботаническа идентичност е потвърдена от професор Pengfei Tu от Пекинския университет. Тестваните кумарини и други субстрати в това проучване са закупени от Sigma-Aldrich (Сейнт Луис, САЩ), Chengdu Push Biotechnology Co., Ltd. (Чънду, Китай) и Chengdu Biopurify Phytochemicals Co., Ltd. (Чънду, Китай ) освен ако не е посочено друго. Референтни стандарти за обезмасляване (1а) и цихориин (2а) бяха закупени от Wuhan Chem Faces Biochemical Co., Ltd. (Ухан, Китай).
2.2. Молекулярно клониране на CtUGT1 от Cistanche tubulosa
Общата РНК наCistanche tubulosaсе екстрахира от месестото стъбло с помощта на OMEGA Plant RNA Kit (GA, USA) и се транскрибира обратно в cDNA с PrimeScript™ RT reagent Kit (TaKaRa, Япония), следвайки инструкциите на производителя. Дегенеративен праймер е проектиран за 3'RACE на базата на аминокиселинните последователности в запазената PSPG (растителни вторични продуктови гликозилтрансферази) кутия от растителни гликозилтрансферази. Усилванията на 3'-края и 5'-края наCtUGT1бяха проведени с помощта на Smart RACE cDNA Amplification Kit (Clontech, САЩ) съгласно протокола на производителя, използвайки праймери (Таблица S1). Пълната дължина на cDNA наCtUGT1се амплифицира чрез PCR, използвайки KOD-Plus Neo ДНК полимераза (TOYOBO, Япония) с генно-специфични двойки праймери (Таблица S1) при следните условия: първоначална стъпка на денатурация при 94 ◦C за 2 минути, последвана от 35 цикъла на денатурация при 98 ◦C за 15 s, отгряване при 55 ◦C за 30 s и удължаване при 68 ◦C за 55 s, с крайна стъпка на удължаване при 68 ◦C за 7 минути. Всички получени ДНК фрагменти бяха клонирани във вектор pEASY-Blunt (TransGen Biotech, Китай) и секвенирани.

2.3. Подравняване на последователности и филогенетичен анализ
Подравняване на последователността наCtUGT1с докладвани гликозилтрансферази (Таблица S2) е извършено с помощта на софтуерен пакет DNAMAN 4.0 (Lynnon Biosoft, Канада). Мотивите и домейните бяха анализирани с помощта на инструмент за запазен домейн (http://www.ncbi.nlm.nih.Gov/Structure/cdd/wrpsb.cgi). Филогенетичното дърво е конструирано чрез стартиране на софтуера MEGA 7.0.14, използвайки метода за свързване на съседи с 1000 първоначални реплики [20]. Преведената протеинова последователност наCtUGT1беше приведен в съответствие с известните растителни гликозилтрансферази, депозирани в базата данни на NCBI GenBank (Таблица S3) с ClustalW.

2.4. Хетероложна експресия и протеиново пречистване на CtUGT1 в Escherichia coli
Кодиращият регион наCtUGT1беше амплифициран с BamH I и Not I като рестрикционни сайтове, използвайки праймери, показани в Таблица S1. PCR реакциите се провеждат с помощта на KOD-Plus-Neo ДНК полимераза (TOYOBO, Осака, Япония). Получените последователности бяха проверени чрез клониране във вектор pEASY-Blunt (TransGen Biotech, Китай). Потвърденият продукт на амплификация наCtUGT1впоследствие се смила и субклонира в експресионния вектор pET-28a(plus) (Novagen, САЩ). След това проверената конструкция се трансформира в E. coli Transetta (DE3), за да се получи рекомбинантният щам. Една нощ култура на рекомбинантен щам се инокулира в среда на Luria-Bertani (LB), съдържаща 50 ug⋅mL− 1 канамицин и 40 ug⋅mL− 1 хлоромицетин в съотношение 1:1{{ 19}}0. Културите се отглеждат при 37 ◦C, 200 rpm, докато стойността на OD600 достигне 0, 4–0, 6. Впоследствие се добавя изопропил- -D-тиогалактопиранозид (IPTG) до крайна концентрация от 0,5 mM и клетките се отглеждат в продължение на 16 часа при 18 °C, 180 rpm. След това клетъчните пелети се събират чрез центрофугиране (7600 × g, 10 минути, 4 ◦ C) и се суспендират повторно в 3 mL/g охладен лизисен буфер (Бележка 1 за допълнителни данни) и се разрушават чрез ултразвук върху лед. Клетъчните остатъци се отстраняват чрез центрофугиране при 7600 × g, 4 ° С за около 30 минути. Предварително уравновесена колона Histrap (GE Healthcare, Uppsala, Швеция) се използва за афинитетна хроматография съгласно инструкциите на производителя. Рекомбинантният протеин се елуира с 10 колонни обема от елуиращ буфер (Бележка за допълнителни данни 1), съдържащ 250 тМ имидазол. Чистотата на протеина се анализира чрез 10 процента SDS-PAGE. Пречистеният протеин се концентрира чрез 30 kDa ултрафилтрационна епруветка (Sigma-Aldrich, САЩ) и се обезсолява с помощта на PD-10 колона (GE Healthcare, Упсала, Швеция) с обезсоляващ буфер (Бележка за допълнителни данни 1). Концентрацията на протеин се определя по метода на Брадфорд, като се използва BSA като стандарт.
2.5. Анализи на ензимната активност и субстратна специфичност на CtUGT1
За да се изследва активността на гликозилиране наCtUGT1, бяха проведени ензимни анализи в реакционна смес (150 μL), съставена от 0.4 mM агликон, 0,8 mM UDP-глюкоза (UDPG) и 50 ug пречистенCtUGT1протеин в буфера за обезсоляване. Всички реакции се инкубират при 30 ◦C в продължение на 12 часа и се прекратяват чрез добавяне на 300 μL студен метанол. Смесите се центрофугират при 15, 000 × g за 30 минути, за да се събере супернатантата за HPLC-UV/ESI-MS анализи. Три паралелни анализа бяха проведени рутинно за всяка реакция. HPLC (Agilent 1260, САЩ) беше оборудван с детектор с диодна матрица и колона CAPCELL PAK C18 (250 mm × 4,6 mm, 5 μm; Shiseido, Япония) при скорост на потока от 1 mL⋅min−1 и температурата на колоната се поддържа при 30 ◦C. Подвижната фаза се състои от А (т.е. 0,1 процента воден разтвор на мравчена киселина) и В (т.е. ацетонитрил). Градиентните програми бяха изброени в Таблица S4. Данните от HRESI-MS бяха записани на система LCMS-IT-TOF, снабдена с интерфейс ESI (Shimadzu, Киото, Япония) с ултра-висока чистота He като сблъсък газ и N2 като пулверизиращ газ. Оптимизираните параметри на източника на ESI бяха както следва: скорост на потока на обвивния газ, 1.5 mL⋅min−1; дебит на спомагателния газ, 1,5 mL⋅min− 1; напрежение на пръскане, 4,5 kV; капилярна температура, 200 ◦C. Спектрите бяха записани в диапазона 100–1500 m/z за пълен MS анализ на сканиране.

2.6. Ефекти на реакционното време, pH стойността и температурата върху ензимната активност и кинетични изследвания на CtUGT1
Ефекти на реакционното време, pH стойността и температурата върху ензимната активност наCtUGT1бяха тествани с използване на UDPG като донор на захар и 3 като акцептор на захар в реакционните условия, както е описано по-горе. За определяне на оптималното pH, ензимната активност беше сравнена в 100 mM буфер (лимонена киселина-натриев цитрат) със стойности на pH, вариращи от 3.0 до 6.{{ 14}}, 10{{20}} mM буфер (KH2PO4-K2HPO4) със стойности на pH, вариращи от 6.0 до 8.{{29} }, 100 mM буфер (Tris-HCl) със стойности на pH в диапазона от 7,0 до 9,0, 100 mM буфер (Na2CO3-NaHCO3) със стойности на pH в диапазона от 9,0 до 11,0. За да се анализира оптималната температура на реакцията, реакциите се инкубират при различни температури, вариращи от 0 до 65 ◦C. Протичането на реакцията се оценява в 12 различни времеви точки между 0 и 24 часа. Всички експерименти бяха проведени в три екземпляра. Реакционните смеси се анализират чрез HPLC-MS, както е описано по-горе. За кинетични изследвания наCtUGT1, ензимните анализи бяха извършени в краен обем от 100 μL, съдържащ 100 mM KH2PO4-K2HPO4 буфер (рН 8,0), 25 ug пречистенCtUGT1, 3 mM UDPG и различни концентрации (50–3000 μM) от 3. Реакциите се провеждат при 37 ◦C за 30 минути и след това се прекратяват със 100 μL леденостуден метанол. Всички тези реакции бяха проведени в три екземпляра и ензимната активност беше оценена чрез количествено определяне на съответните глюкозилирани производни. Кинетичните параметри, включително константата на Михаелис-Ментен (Km) и Vmax, бяха изчислени чрез нелинеен регресионен анализ с помощта на софтуер GraphPad Prism 5.
2.7. Селективност на донор на субстрат и захар на CtUGT1
За да проучите субстратните предпочитания наCtUGT1, общо 27 субстрата, принадлежащи към различни структурни типове, бяха тествани с помощта на UDPG като донор. Тяхната химическа информация е посочена в таблица S5, а техните структури са показани на фиг. S1 и S2. Да се изследва селективността на донорите на захарCtUGT1, анализите са проведени с използване на умелиферон (1), ескулетин (2), химекромон (3), 4,4'-дихидрокси бензофенон (4), генистеин (5) и алое-емодин (6) като субстрати с UDPG, UDP- N ацетил галактозамин, UDP-галактоза, GDP-маноза, GDP-фукоза, UDP галактуронова киселина, UDP-рамноза като донори на захар, съответно. Всички експерименти бяха проведени в три екземпляра. Реакционните смеси се анализират чрез HPLC-MS, както е описано по-горе.

2.8. Получаване на 4-метилумбелиферил глюкозид (съединение 3а) от CtUGT1
Препаративната реакционна смес се състои от {{0}}.034 mmol субстратно съединение 3, 0.04 mmol UDPG, 5 mg пречистенCtUGT1в 50 mL реакционен буфер. Реакциите се разбъркват внимателно при оптимални условия (100 mM KH2PO4-K2HPO4 с рН 8.0; 37 ◦C). След инкубиране при 37 ◦C в продължение на 24 часа, реакционната супернатанта се отделя чрез колонна хроматография с макропореста смола (MCI GEL CHP) след центрофугиране при 12, 000 × g за 30 минути. Подвижната фаза е градиентно елуиране от 100 процента вода до 100 процента метанол. Всяка фракция се анализира чрез HPLC-UV. Фракциите, съдържащи само целеви продукти, се изпаряват до сухо при понижено налягане и се характеризират с 1Н ядрено-магнитен резонанс (NMR) спектроскопия и 13C NMR спектроскопия.
2.9. Молекулярно докинг и сайт-насочена мутагенеза на CtUGT1
Протеиновият модел наCtUGT1е установен с помощта на SWISS-MODEL [21–25]. Кристалната структура на Medicago truncatula гликозил трансфераза UGT85H2 (PDB ID 2PQ6) беше избрана като шаблонна структура [26]. Установеният модел беше оценен от VERIFY-3D [27,28]. Auto-Dock Vina беше използван за молекулярни докинг изследвания [29]. Кристалната структура на UGT74F2 [30], гликозилтрансфераза от Arabidopsis thaliana, в комплекс с лиганд UDP и салицилова киселина (PDB ID 5U6M) беше използвана като контролна структура съответно за анализ на донорен джоб на захар и акцепторен джоб на захар . Auto-Dock-Tools 1.5.6 от MGLTools (инструменти на Molecular Graphics Laboratory) бяха използвани за подготовка на донора на захар UDPG и субстрат 1, 2 за молекулярно докинг. Страничните вериги от остатъци около кухината на активното място бяха поставени гъвкави и въртящите се връзки на лигандите бяха оставени свободни да се въртят. Най-високо класираната поза, оценена от докинг модела на Vina с най-висок (kcat/mol) афинитет, беше подложена на визуален анализ с помощта на софтуер PyMOL 2.0.
За изследвания на мутагенеза оптимизираната последователност ген наCtUGT1(Допълнителни данни Бележка 2) беше синтезиран и тестван като див тип. Насочена към място мутагенеза наCtUGT1беше проведено с помощта на системата за бърза мутагенеза (TransGen Biotech). Мутантите бяха амплифицирани от шаблона на оптимизирания ген, който беше конструиран в pET{0}}вектора, като се използваха специфичните праймери, показани в Таблица S1. Конструираните мутанти бяха проверени чрез PCR и секвениране преди да бъдат трансформирани в Е. coli (DE3) за хетероложна експресия. Пречистване на протеини и ензимни реакции бяха извършени и анализирани, както е описано по-горе.

3. Резултати и обсъждане
3.1. Клониране на cDNA с пълна дължина на гена CtUGT1 отCistanche tubulosa
Cistanche tubulosa(L.) (RouCongRong) е традиционна китайска лечебна билка, произвеждаща голямо разнообразие от биоактивни естествени гликозиди. Трябва да има значителен брой нови гени на гликозилтрансферазите, които съществуват в неговия геном. За да се търсят нови гликозилтрансферази с интересни катализни активности, беше проектиран дегенеративен праймер за 3'-RACE въз основа на запазения PSPG мотив за клониране на пермисивни UGT отCistanche tubulosa. Получената 3' крайна последователност беше допълнително анализирана чрез NCBI бласт и специфичният праймер за 5'-RACE беше проектиран въз основа на получената последователност. Амплифицираните 5' сДНК краища и 3' сДНК краища бяха сплайсирани и пълната дължина наCtUGT1последователност, включваща 1739 нуклеотида, беше получена (фиг. S3) и изброена в Допълнителни данни Бележка 3. Впоследствие отворена четяща рамка (ORF) наCtUGT1беше намерено от инструментите NCBI ORF Finder и кодиращата последователност от 1482 bp беше успешно клонирана чрез RT-PCR амплификация, използвайки специфични праймери в таблица S1. cDNA последователността на CtUGT1 е представена на NCBI (номер за достъп MW629113).
3.2. Анализ на последователността и хетероложна експресия на CtUGT1
TheCtUGT1се очаква генът да кодира протеин от 493 аминокиселинни остатъка с приблизителна молекулна маса от 55,78 kDa. NCBI blast разкри, че изведената протеинова последователност наCtUGT1споделя най-висока идентичност (76,39 процента) с UGT86A1-подобни ензими. Биохимичните функции на този вид ензим не са напълно характеризирани. Предвижда се, че те могат да участват в адаптацията на растенията към абиотичен стрес. Подравняването на аминокиселинните последователности на CtUGT1 и други растителни гликозилтрансферази е показано на Фиг. S4.
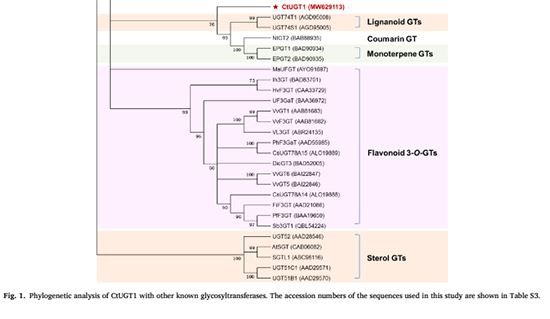
Силно запазените 44 остатъка от PSPG мотива бяха открити в С-терминала наCtUGT1. В рамките на PSPG-кутия, пептидна последователност на HCGWNS е разположена на 373-та аминокиселина, която е открита в 95 процента от всички гликозилтрансферази [31]. Крайният остатък от PSPG мотива беше глутамин, което показва, че този ензим има тенденция да използва UDPG като свой захарен донор [32] (фиг. S4). Филогенетичното дърво е конструирано въз основа на предсказаните полипептидни последователности наCtUGT1и различни видове гликозилтрансферази от растителен произход, които участват в биосинтезата на различни вторични метаболити. Досега повечето от докладваните гликозилтрансферази от растения разпознават флавоноиди като техни субстрати, като флавон 7-O-гликозилтрансферази, флавоноид 3-O-глюкозилтрансферази, изофлавон 7-O-гликозилтрансферази и халкон гликозилтрансферази. Това показват резултатите от филогенетичния анализCtUGT1не е групиран в групата на флавоноидите GTs. Вместо това, той е разположен в съседство с UGT74T1 и UGT74S1 (лигнан гликозилтрансферази от Linum usitatissimum) и NtGT2 (кумарин гликозилтрансфераза от Nicotiana tabacum), което показва, чеCtUGT1може да има някои нови каталитични активности към фенилпропаноидни субстрати (фиг. 1), особено като се има предвид, че само ограничени членове са функционално идентифицирани, принадлежащи към тези клади.
За по-нататъшно разкриване на неговата каталитична активност,CtUGT1последователността се експресира под контрола на T7 lac промотора в E. coli Transetta (DE3) клетки като His6-маркиран слят протеин. His-маркираният рекомбинантCtUGT1беше ефективно пречистен до хомогенност чрез Ni-NTA афинитетна хроматография. Молекулното тегло на пречистения рекомбинантен CtUGT1 е приблизително 55 kDa (фиг. S5), което е в съответствие с прогнозираната молекулна маса.


3.3. In vitro акцепторна субстратна специфичност на CtUGT1
За да се тества активността на гликозилиране наCtUGT1бяха проведени in vitro ензимни анализи. UDPG се използва като донор на захар. Акцепторите на захар бяха избрани въз основа на различни опасения. Първо, наCtUGT1генът е клониран отCistanche tubulosaчиито основни химически компоненти са PhGs. За да се провери далиCtUGT1участва в биосинтезата на PhGs, обичайните агликони на PhGs вCistanche tubulosaкато тирозол (NP1, Фиг. S2) и салидрозид (NP2, Фиг. S2) първо бяха избрани като субстрати. За съжаление, HPLC и HRESI-MS анализите не откриха никакви гликозилирани продукти, което показва, чеCtUGT1може да не участват в биосинтезата на PhGs.
Второ, въз основа на подравняването на последователността и резултатите от филогенетичния анализ (фиг. 1),CtUGT1е филогенетично свързан с лигнаноидни и кумарин гликозилтрансферази, което предполага, чеCtUGT1вероятно е фенилпропаноид гликозилтрансфераза. За да се провери тази прогноза, три кумаринови субстрата 1, 2 и 3 заедно с един лигнаноиден субстрат магнолол NP17 бяха тествани съответно като акцептори на захар. Топлинно инактивирани ензими (100 ◦C, 10 минути) се използват като отрицателна контрола. HPLC-HRESI-MS анализ на реакции с използване на NP17 като субстрат не откри никакъв продукт. За разлика от това,CtUGT1показаха очевидни способности за глюкозилиране срещу тестваните кумаринови субстрати (1,2,3). Използвайки субстрат 1 като пример, както е показано на Фиг. 2А, нов пик (1а) с намалено време на задържане (11,46 минути) в сравнение с това на субстрат 1 (19,75 минути) се получава отCtUGT1при доходност от 37,78 процента. Неговият UV абсорбционен спектър съответства на 1. HRESI-MS спектърът показва, че пик 1а показва [M плюс H] плюс при m/z 325.1029 и [M плюс Na] плюс при m/z 347.0710 (изчислено 347.0737 за C15H16O8Na ) с предвидената формула на C15H16O8, която е 162 amu по-голяма от тази на 1 и в съответствие с теоретичната формула на глюкозилиран продукт (фиг. 2A). По подобен начин, глюкозилираният продукт на субстрат 2 (14,21 минути, Фигура 2В) и 3 (21,92 минути, Фигура 2С) също беше открит при време на задържане от 10,85 минути и 13,80 минути, със степен на превръщане от 22,03 процента и 68,67 процента , съответно. Молекулната маса на продуктите съвпада точно с изчислената маса на глюкозилираните продукти, което потвърждава товаCtUGT1може да катализира глюкозилирането на кумаринови съединения 1-3 (Таблица 1).
Впоследствие, като се има предвид, че повечето от наскоро докладваните ензими показват промискуитет на катализа in vitro, за по-нататъшно изследване на субстратния спектър наCtUGT1бяха проведени експанзивни ензимни анализи към различни съединения, принадлежащи към различни видове природни продукти, включително флавоноиди, фенолни съединения, кумарини, стилбен, антрахинони, бензофенон, нафталин и иридоид (Фигури S1-S2), като се използва UDPG като донор на захар. Установено е, че бензофеноновият субстрат 4,4′-дихидрокси бензофенон (4), изофлавонният субстрат генистеин (5) и антрахиноновият субстрат алое-емодин (6) също могат да бъдат катализирани отCtUGT1за да образува съответния глюкозилиран продукт 4а, 5а, 6а с по-висока полярност (фиг. 3). HRESI-MS анализът показа, че йонните пикове на продуктите са 162 amu по-високи от тези на субстратите, което предполага, чеCtUGT1може да катализира глюкозилирането на тези съединения, за да образува съответния им моноглюкозиден продукт. Коефициентите на преобразуване на 4, 5 и 6 бяха съответно 4,12 процента, 14,14 процента и 23,33 процента (Таблица 1).
Селективността на донора на захар наCtUGT1също беше проучен. В допълнение към UDPG, шест други донора, включително UDP-N-ацетил галактозамин, UDP галактоза, GDP-маноза, GDP-фукоза, UDP-галактуронова киселина и UDP рамноза, бяха тествани с помощта на субстрати 1–6 като акцептори. Резултатите показаха товаCtUGT1изключително избран UDPG като донор на захар. Не е наблюдаван продукт, когато са тествани други активирани захари (данните не са показани).

3.4. Биохимични свойства и кинетични параметри на CtUGT1
Биохимични свойства наCtUGT1бяха изследвани с използване на 3 като акцептор на захар и UDPG като донор на захар, както е показано на Фиг. 4. Каталитична активностCtUGT1беше тестван в температурен диапазон от 4–60 ◦C, оптималната активност беше открита при 37 ◦C (фиг. 4A). Анализът на ензимната активност между pH 3.0 и 9.0 показа, че оптималната стойност на pH се наблюдава при pH 8.0 (100 mM буфер KH2PO4-K2HPO4, Фиг. 4C). Добивът на продукта на глюкозилиране 3а нараства линейно в рамките на 1 час и скоростта на растеж се изравнява след 5 часа (фиг. 4В). Привидната стойност на кмCtUGT1за 3 беше 218,7 ± 7,176 μM, а Vmax беше 0.02255 ± 0,0001796 nmol⋅min− 1⋅ug− 1.
3.5. Ензимен препарат и структурна идентификация на глюкозилирани продукти
Въз основа на резултатите от ензимните анализи,CtUGT1има тенденция да бъде специфична глюкозилтрансфераза, която може да катализира глюкозилирането на различни видове природни продукти. Информацията за HPLC-HR-MS за продуктите е обобщена в таблица 1. Сред тях кумариновите субстрати показват значителна скорост на превръщане. Ензимната активност срещу кумарини беше допълнително анализирана. Трябва да се отбележи, че и трите тествани кумаринови субстрата са приети отCtUGT1имат хидроксилна група в C-7 позиция, докато ескулетин (2) има допълнителна хидроксилна група в C-6 позиция. HPLC профилът на глюкозилирания продукт на ескулетин е показан на Фиг. 2. Наблюдава се само един продукт, което предполага, че реакцията на глюкозилиране се е случила региоспецифично на C-6 или C-7 позиция. За да се потвърди мястото на гликозилиране, продукт 2а беше идентифициран чрез сравнение с автентичните глюкозиди чрез HPLC-UV/HRESI-MS анализ. При добавяне на автентичния глюкозид цихориин (глюкозилиран на 7-OH позиция на 2) в реакционната система, пикът се припокрива с 2а, ко-HPLC профил допълнително потвърждава, че гликозилираният продукт на 2, катализиран отCtUGT1е cichoriin [33], което доказва, че глюкозилната част е специфично прехвърлена на C7-OH позиция. Продукт 1а също беше идентифициран чрез сравнение с референтния стандарт. UV-HPLC спектрите заедно с ко-HPLC анализ (фиг. 2) разкриха, че химичната структура на 1а се приписва на обезмасляване [34], което е глюкозилиран продукт на 1 на C7-OH позиция.
Продукт 3а беше получен от реакция с увеличен мащаб и структурно характеризиран чрез HRESI-MS, 1H NMR и 13C NMR спектроскопия (фигури S13, S14 и бележка 4). В 1H NMR сигнала, в сравнение със субстрат 3, фенолен хидроксилен сигнал на позиция C{{10}} изчезна и въглеродният сигнал на C-7 се измести δ 1.{{25} } ppm към високото поле, докато C-6 и C-8 сигналите се изместват към ниското поле в 13C NMR. Тези констатации потвърждават, че глюкопиранозиловият остатък е прикрепен към фенолната хидроксилна група в C-7 позиция на 3 [35]. Освен това, 1H NMR спектърът показва аномерни протонни сигнали при δH 5.00 (1H, d, J=7.0 Hz); захарният компонент беше посочен като -D-глюкопираноза. Този резултат демонстрираCtUGT1е кумарин О-глюкозилтрансфераза, която катализира глюкозилирането на хидроксил кумарин в 7-OH позиция.

3.6. Моделиране на хомология, молекулярно докинг и сайт-насочена мутагенеза на CtUGT1 протеин
Обширни ензимни реакции разкриха товаCtUGT1може да катализира глюкозилирането на три кумарина в техния съответен глюкозилиран продукт, а глюкозилираната позиция се случва конкретно в 7- OH позиция. За идентифициране на ключовите остатъци, които определят катализните дейности наCtUGT1бяха извършени хомоложно моделиране, молекулярно докинг и изследвания на насочена към място мутагенеза на CtUGT1. Хомоложно молекулярно моделиране за CtUGT1 беше установено с помощта на SWISS-MODEL [21–25]. Кристалната структура на Medicago truncatula гликозил трансфераза UGT85H2 (PDB ID 2PQ6), определена при разделителна способност от 2,1 Å, показва най-висок общ резултат с максимална хомология на последователността и ниска E-стойност, е избрана като шаблонна структура [26]. Оценката на рационалността на установения модел беше показана в диаграмата Рамачандран (фиг. S6), 88,5 процента от остатъците в установения модел са в най-облагодетелствания регион. Хомоложният модел на CtUGT1 се състои от два подобни мотива на гънки от тип Rossmann съответно на N- и C-терминала (фиг. 5A). N-терминалният домейн има седем верижни успоредни листа около десет спирали. С-терминалният домен съдържа шест верижни листа, оградени от девет спирали (фиг. 5A, S7).
За допълнително изясняване на активния джоб наCtUGT1беше извършено молекулярно докинг. Тъй като UGT85H2 има само структура на аро форма, друг хомолог UGT74F2 с UDP и салицилова киселина като два лиганда бяха избрани като контролен шаблон. UDPG се приготвя като донор на захар. Два кумаринови субстрата 1 и 2 бяха приготвени съответно като акцептори на захар. Местата на свързване на гликозил донор и акцептор бяха изчислени и докингирани поотделно, както е показано на Фиг. 5. Резултатите показват, че и двата свързващи джоба са разположени вътре в дълбоката цепнатина в зоната на взаимодействие на плътно опакования N-терминален домен и C -краен домейн наCtUGT1и пространствено близки един до друг (фиг. 5А). С-краят наCtUGT1участва главно в контакт с гликозилния донор, както е описано в UGT на други растения, и повечето от околните остатъци са хидрофилни и силно запазени. Като типичната PSPG-кутия, остатъкът W377 в този мотив може да образува водородни връзки с глюкозната група на UDPG (фиг. 5B); N378 и S379 в този мотив могат да образуват водородни връзки с дифосфатната група на UDPG (фиг. 5B). В допълнение, според резултатите от докинга, остатъците от W356 и Q359 могат да взаимодействат с групата на уридин чрез взаимодействие с водородна връзка, за да стабилизират донора в активния джоб. За да се провери функцията на тези прогнозирани ключови остатъци, бяха избрани общо 16 места и подложени на аланинова сканираща мутагенеза. Катализните активности на тези мутанти бяха тествани с помощта на всичките шест положителни субстрата, споменати по-горе. HPLC анализите показват, че когато остатъци от G18, H19, S295, F296, W356, C357, Q359, H374, G376, W377, N378, S379, E382, Y397 и D398 са мутирани в аланин, гликозилиращата активност на протеина е била напълно загубен спрямо всички тествани субстрати. Тези резултати предполагат, че горните 16 остатъка са ключовите остатъци, които определят свързването на UDPG донора и активността на гликозилиране наCtUGT1.
To identify the crucial residues in the sugar acceptor binding pocket, molecular docking analyses were performed on 1 and 2, respectively. These two substrates have the same coumarin core. 2 have two hydroxyl groups at both C-6 and C-7 position while 1 only has one hydroxyl group at the C-7 position. The overlapped docking results of these two compounds were shown in Fig. 5C. They exhibited almost the same confirmation in the glycosyl acceptor binding pocket (1 in cyan color and 2 in green color). Two hydrogen bonds were observed between the NE2 atom of the imidazole ring of H19 and the OH group of coumarins at positions C-6 (~3.1 Å) and C-7(~3.0 Å) respectively (Fig. 5D). It was calculated that H19 is much closer to the 7-OH group which will make the hydroxyl group at the C-7 position easily to be deprotonated by H19 to form the nucleophilic oxyanion that could attack the C1′ carbon of UDPG to initiate the glycosylation reaction. This may explain why the glycosylation position was preferred to happen at the 7-OH position of coumarins substrates. Besides, it can be seen that H19 is located at the cleft of the two active pockets, and interacts with both the substrate and UDPG (Fig. 5B, C, D). Mutation of His19 to alanine will lead to the complete loss of enzyme activity, which confirmed the irreplaceable role of H19 that plays a role as the crucial catalysis basis, meanwhile, stabilizing the UDPG donor. Alanine scanning mutagenesis of some other sites in the acceptor binding pocket also resulted in no detectable enzyme activity, including Y16, L213, F296, or significantly decrease of the enzyme activity (>44 процента) като V14, V132, E153, T212 и I209 (фиг. S8). Предвижда се, че тези хидрофобни остатъци, обграждащи ароматния пръстен, могат да образуват ван дер Ваалсови взаимодействия със субстрата в свързващия джоб.

4. Обсъждане
Гликозилирането е една от най-важните стъпки на модификация в пътищата на биосинтеза на много вторични метаболити. Гликозилирането може да увеличи бионаличността на природните продукти чрез подобряване на тяхната разтворимост във вода и намаляване на тяхната токсичност. Кумаринът се счита за най-простата форма в рамките на огромен клас естествено срещащи се фенолни вещества, изградени от -пиронов пръстен, слят с бензенов пръстен. Както естествените, така и синтетичните съединения на базата на кумарин привлякоха голямо внимание от медицинските химици и учените в дизайна на лекарства като следствие от техните разнообразни фармакологични и биологични свойства [36]. Допълнителна гликозилирана модификация на кумарини може да помогне за обогатяване на структурното разнообразие на тези съединения и също така да подобри тяхната разтворимост и бионаличност. В растенията такъв процес на гликозилиране се катализира от UDP-гликозилтрансфераза. Въпреки че са идентифицирани множество UGT от различни растения, към днешна дата повечето от докладваните UGT са участвали в гликозилираната модификация на флавоноидите. Съобщава се, че само ограничени UGT могат да приемат кумарини като субстрати. В това изследване нов гликозилтрансферазен генCtUGT1е клониран от традиционната китайска билкаCistanche tubulosa. Подравняването на последователността и резултатите от филогенетичния анализ показаха товаCtUGT1е филогенетично отдалечен от повечето докладвани флавоноидни UGT и много близо до фенилпропаноидните UGT. Обширни ензимни анализи разкриват, че CtUGT1 не може да катализира гликозилирането на фенилетанолни съединения за образуване на PhGs, което е основният химичен компонент наCistanche tubulosa. Вместо това, той може да разпознае кумарините като свои субстрати и да проведе реакцията на гликозилиране. Изясняването на структурата на продуктите показва, че мястото на гликозилиране, катализирано отCtUGT1региоспецифично се случва в C7-OH позицията на кумарините. Използвайки CtUGT1, три кумаринови гликозида, включително обезмасляване (1а), цихориин (2а) и 4-метилумбелиферил глюкозид (3а), бяха успешно ензимно синтезирани и структурно идентифицирани. Всички тези три съединения са докладвани като фармацевтично активни молекули. Например, счита се, че 1а притежава различни фармакологични активности, включително ренопротективна активност, противовъзпалителни, противоракови и антиамебни свойства [37]. 2а показва висока антибактериална активност срещу някои Грам-положителни бактерии като Bacillus cereus и Staphylococcus aureus [38]. 3a може да помогне на растенията да подобрят способността си за реакция към химикали и токсини [39].
В допълнение към кумарините, обширни ензимни анализи установиха, чеCtUGT1също така показа видима активност на глюкозилиране към бензофенонов субстрат 4, изофлавонов субстрат 5 и антрахинонов субстрат 6, което показва, че CtUGT1 има определена толерантност към субстрата. Въпреки това,CtUGT1не може да катализира биосинтезата на гликозидни компоненти вCistanche tubulosaкато фенилетаноидни гликозиди (PhGs), лигнаноидни гликозиди и иридоидни гликозиди. Освен това, според предишни изследвания, не са изолирани кумаринови гликозиди отCistanche tubulosa. И така, in vivo функцията наCtUGT1все още трябва да се проучи допълнително. Глюкозилиращата активност на CtUGT1 към кумаринови субстрати прави този ензим полезен инструмент за ензимна гликозилираща модификация на кумарини и също така показва, че тези растителни вторични метаболитни ензими могат да извършват неоценими катализни дейности, които са далеч извън техните естествени функции.
Декларация за конкурентен интерес
Авторите декларират, че няма конфликт на интереси.
Признание
Тази работа беше финансово подкрепена от Пекинската фондация за природни науки (грант № 7192112); Програма за спонсорство на млади елитни учени от CAST (Грант № CACM− 2018− QNRC1− 02); Национална фондация за природни науки на Китай (грант № 81402809); Държавен фонд за стипендии на Китайския съвет за стипендии (грант № 201906555010) и научна фондация за елитни млади учени на Пекинския университет по китайска медицина (грант № 2018-JYB-XJQ006).
Приложение A. Допълнителни данни
Допълнителни данни към тази статия могат да бъдат намерени онлайн на https://doi. org/10.1016/j.fitote.2021.104995.
От: ' Молекулярно клониране и биохимично характеризиране на нова кумарин гликозилтрансферазаCtUGT1отCistanche tubulosa' отXiping Xu и др
---Fitoterapia 153 (2021) 104995 https://doi.org/10.1016/j.fitote.2021.104995
Препратки
[1] Y. Li, S. Baldauf, EK Lim, DJ Bowles, Филогенетичен анализ на мултигенното семейство UDPglycosyltransferase на Arabidopsis thaliana, J. Biol. Chem. 276 (2001) 4338–4343, https://doi.org/10.1074/jbc.M007447200.
[2] LF Mackenzie, Q. Wang, RAJ Warren, SG Withers, Glycosynthases: мутантни гликозидази за синтез на олигозахариди, J. Am. Chem. Soc. 120 (1998) 5583–5584, https://doi.org/10.1021/ja980833d.
[3] CJ Thibodeaux, CE Melancon, HW Liu, Необичаен биосинтез на захар и гликодиверсификация на естествени продукти, Nature 446 (2007) 1008–1016, https://doi.org/ 10.1038/nature05814.
[4] Y. Ji, B. Li, M. Qiao, J. Li, H. Xu, L. Zhang, X. Zhang, Напредък в in vivo и in vitro гликозилирането на флавоноиди, Appl. Microbiol. Биотехнология. 104 (2020) 6587–6600, https://doi.org/10.1007/s00253-020-10667-z.
[5] T. Koeduka, Y. Ueyama, S. Kitajima, T. Ohnishi, K. Matsui, Молекулярно клониране и характеризиране на UDP-глюкоза: летлива бензеноид/фенилпропаноид глюкозилтрансфераза в цветя на петуния, J. Plant Physiol. 252 (2020) 153245, https://doi.org/10.1016/j.jplph.2020.153245.
[6] S. Rahimi, J. Kim, I. Mijakovic, KH Jung, G. Choi, SC Kim, YJ Kim, Тритерпеноид-биосинтетични UDP-гликозилтрансферази от растения, Biotechnol. адв. 37 (2019) 107394, https://doi.org/10.1016/j.biotechadv.2019.04.016.
[7] G. Singh, YV Dhar, MH Asif, P. Misra, Изследване на функционалното значение на ензимите стерол гликозилтрансфераза, Prog. Lipid Res. 69 (2018) 1–10, https://doi. org/10.1016/j.plipres.2017.11.001.
[8] KF McCue, PV Allen, LV Shepherd, A. Blake, J. Whitworth, MM Maccree, DR Rockhold, D. Stewart, HV Davies, WR Belknap, Първичната in vivo стероидна алкалоидна глюкозилтрансфераза от картофи, Фитохимия. 67 (2006) 1590–1597, https://doi.org/10.1016/j.phytochem.
[9] J. Yu, L. Wang, RL Walzem, EG Miller, LM Pike, BS Patil, Антиоксидантна активност на цитрусови лимоноиди, флавоноиди и кумарини, J. Agric. Food Chem. 53 (2005) 2009–2014, https://doi.org/10.1021/jf0484632.
[10] HJ Cho, SG Jeong, JE Park, JA Han, HR Kang, D. Lee, MJ Song, Антивирусна активност на ангелицин срещу gammaherpesviruses, Antivir. Рез. 100 (2013) 75–83, https://doi.org/10.1016/j.antiviral.2013.07.009.
[11] Z. Xu, Q. Chen, Y. Zhang, C. Liang, Производни на базата на кумарин с мощна анти-HIV активност, Fitoterapia. 150 (2021) 104863, https://doi.org/10.1016/j. fitote.2021.104863.
[12] AT Mossa, TM Heikal, M. Belaiba, EG Raoelison, H. Ferhout, J. Bouajila, Антиоксидантна активност и хепатопротективен потенциал на Cedrelopsis grevei върху индуциран от циперметрин оксидативен стрес и увреждане на черния дроб при мъжки мишки, BMC Complement. Алтернативен. Med. 15 (2015) 251, https://doi.org/10.1186/s12906-015-0740-2.
[13] Y. Bansal, P. Sethi, G. Bansal, Coumarin: потенциално ядро за противовъзпалителни молекули, Med. Chem. Рез. 22 (2013) 3049–3060, https://doi.org/10.1007/s00044-012-0321-6.
[14] M. Kumar, R. Singla, J. Dandriyal, V. Jaitak, Производни на кумарин като противоракови средства за терапия на рак на белия дроб: преглед, Anti Cancer Agents Med. Chem. 18 (2018) 964–984, https://doi.org/10.2174/1871520618666171229185926.
[15] A. Stefanachi, F. Leonetti, L. Pisani, M. Catto, A. Carotti, Coumarin: естествено, привилегировано и многостранно скеле за биоактивни съединения, Molecules 23 (2018) 250, https://doi.org /10.3390/molecules23020250.
[16] Т. Тагучи, Н. Убуката, Х. Хаяшида, М. Ямамото, Оказаки, клониране и характеризиране на глюкозилтрансфераза, която реагира на 7-хидроксилна група на флавонол и 3-хидроксилна група на кумарин от тютюневи клетки, арх. Biochem. Biophys. 420 (2003) 95–102, https://doi.org/10.1016/j.abb.2003.09.027.
[17] L. Zhou, T. Tian, B. Xue, L. Song, L. Liu, R. Yu, Биосинтеза на кумаринови гликозиди от трансгенни космати корени на Polygonum multiflorum, Biosci. Биотехнология. Biochem. 76 (2012) 1008–1010, https://doi.org/10.1271/bbb.110347.
[18] H. Kanoh, M. Kawauchi, M. Kuroyanagi, T. Arima, Молекулярно клониране и характеризиране на кумарин глюкозилтрансфераза в космати корени на Pharbitis nil (Ipomoea nil), Plant Tissue Cult. Лет. 31 (2014) 21–28, https://doi.org/10.5511/plantbiotechnology.13.1203a.
[19] JB He, P. Zhao, ZM Hu, S. Liu, Y. Kuang, M. Zhang, B. Li, CH Yun, X. Qiao, M. Ye, Молекулярна и структурна характеристика на безразборна Cglycosyltransferase от Trollius Chinensis, Angew. Chem. Вътр. Ед. инж. 58 (2019) 11513–11520, https://doi.org/10.1002/anie.201905505.
[20] S. Kumar, G. Stecher, K. Tamura, MEGA7: анализ на молекулярна еволюционна генетика версия 7.0 за по-големи набори от данни, Mol. Biol. Еволюция 33 (2016) 1870–1874, https://doi. org/10.1093/molbev/msw054.
[21] A. Waterhouse, M. Bertoni, S. Bienert, G. Studer, G. Tauriello, R. Gumienny, FT Heer, TAP de Beer, C. Rempfer, L. Bordoli, R. Lepore, T. Schwede, SWISS-MODEL: хомологично моделиране на протеинови структури и комплекси, Nucleic Acids Res. 46 (2018) W296–W303, https://doi.org/10.1093/nar/gky427.
[22] N. Guex, MC Peitsch, T. Schwede, Автоматизирано сравнително моделиране на протеинова структура с SWISS-MODEL и Swiss-Pdb viewer: историческа перспектива, Electrophoresis 30 (2009) S162–S173, https://doi.org/ 10.1002/elps.200900140.
[23] S. Bienert, A. Waterhouse, TAP de Beer, G. Tauriello, G. Studer, L. Bordoli, T. Schwede, The SWISS-MODEL repository-нови характеристики и функционалност, Nucleic Acids Res. 45 (2017) D313–D319, https://doi.org/10.1093/nar/gkw1132.
[24] G. Studer, C. Rempfer, AM Waterhouse, G. Gumienny, J. Haas, T. Schwede, QMEANDisCo-ограничения на разстоянието, приложени към оценката на качеството на модела, Bioinformatics. 36 (2020) 1765–1771, https://doi.org/10.1093/bioinformatics/ btz828.
[25] M. Bertoni, F. Kiefer, M. Biasini, L. Bordoli, T. Schwede, Моделиране на протеинова кватернерна структура на хомо- и хетеро-олигомери извън бинарните взаимодействия чрез хомология, Sci. Rep. 7 (2017) 10480, https://doi.org/10.1038/s41598-017-09654-8.
[26] L. Li, LV Modolo, LL Escamilla-Trevino, L. Achnine, RA Dixon, X. Wang, Кристалната структура на Medicago truncatula UGT85H2-вникване в структурната основа на многофункционален (изо)флавоноид гликозилтрансфераза, J. Mol. Biol. 370 (2007) 951–963, https://doi.org/10.1016/j.jmb.2007.05.036.
[27] R. Lüthy, JU Bowie, D. Eisenberg, Оценка на протеинови модели с триизмерни профили, Nature 356 (1992) 83–85, https://doi.org/10.1038/ 356083a0.
[28] RA Laskowski, MW MacArthur, DS Moss, JM Thornton, PROCHECK: програма за проверка на стереохимичното качество на протеиновите структури, J. Appl. Crystallogr. 26 (1993) 283–291, https://doi.org/10.1107/S0907444998006684.
[29] O. Trott, AJ Olson, AutoDock Vina: подобряване на скоростта и точността на докинг с нова функция за точкуване, ефективна оптимизация и многопоточност, J. Comput. Chem. 31 (2010) 455–461, https://doi.org/10.1002/jcc.21334.
[30] AM George Thompson, CV Iancu, KE Neet, JV Dean, JY Choe, Разлики в конюгациите на салицилова киселина и глюкоза от UGT74F1 и UGT74F2 от Arabidopsis thaliana, Sci. 7 (2017) 46629, https://doi.org/10.1038/srep46629.
[31] T. Vogt, P. Jones, Гликозилтрансферази в синтеза на естествени растителни продукти: характеризиране на семейство супергени, Trends Plant Sci. 5 (2000) 380–386, https://doi.org/10.1016/s1360-1385(00)01720-9.
[32] A. Kubo, Y. Arai, S. Nagashima, T. Yoshikawa, Промяна на специфичността на донора на захар на растителни гликозилтрансферази чрез едноточкова мутация, Arch. Biochem. Biophys. 429 (2004) 198–203, https://doi.org/10.1016/j. абб.2004.06.021.
[33] H. Kanho, S. Yaoya, T. Itani, T. Nakane, N. Kawahara, Y. Takase, K. Masuda, M. Kuroyanagi, Глюкозилиране на фенолни съединения от Pharbitis nil hairy roots: I. Глюкозилиране на кумарин и флавонови производни, Biosci. Биотехнология. Biochem. 68 (2004) 2032–2039, https://doi.org/10.1271/bbb.68.2032.
[34] J. Bjerre, EH Nielsen, M. Bols, Хидролиза на токсични естествени глюкозиди, катализирана от циклодекстрин дицианохидрини, Eur. J. Org. Chem. 2008 (2010) 745–752, HTTPS:// doi.org/10.1002/ejoc.200700954.
[35] B. Xue, LB Zhou, JW Liu, RM Yu, Биотрансформация на производни на хидроксикумарин чрез култивирани суспензионни клетки на Catharanthus roseus, Pharmazie 67 (2012) 467–471, https://doi.org/10.1691/ph.2012.1741 .
[36] T. Al-Warhi, A. Sabt, EB Elkaeed, WM Eldehna, Последни постижения на базирани на кумарин противоракови агенти: актуален преглед, Bioorg. Chem. 103 (2020) 104163, https://doi.org/10.1016/j.bioorg.2020.104163.
[37] X. Li, MY Gruber, DD Hegedus, DJ Lydiate, MJ Gao, Ефекти на кумариново производно, 4-methylumbelliferone, върху покълването на семената и създаването на разсад в Arabidopsis, J. Chem. Ecol. 37 (2011) 880–890, https://doi.org/10.1007/s10886-011-9987-3.
[38] K. Xu, ZM Feng, YN Yang, JS Jiang, PC Zhang, Осем нови сесквитерпеноиди от тип евдесман и еремофилан от Atractylodes lancea, Fitoterapia. 114 (2016) 115–121, https://doi.org/10.1016/j.fitote.2016.08.017.
[39] Y. Lou, H. Wu, J. Zheng, X. He, Z. Wu, X. Lu, Y. Qiu, Определяне и фармакокинетично изследване на скиминг чрез UHPLC-MS/MS в плазма на плъх, J. Pharm . Biomed. анален 179 (2020) 112969, https://doi.org/10.1016/j.jpba.2019.112969.

