Невропротекция на N-бензил ейкозапентаенамид при новородени мишки след хипоксично-исхемично мозъчно увреждане
Mar 21, 2022
Контакт:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Резюме:
Мака(Lepidium meyenii) се превърна в популярна функционална растителна храна поради своите лечебни свойства и хранителна стойност.Макамиди, тъй като изключително активните съставки, открити вмака, са уникална серия от неполярни, дълговерижни N-бензил амиди на мастни киселини с множество биоактивности като характеристики против умора и подобряване на репродуктивното здраве. В това проучване е идентифициран нов вид максимизиране, N-бензил ейкозапентаенамид (NB-EPA), отмака. Допълнително изследваме неговата потенциална невропротективна роля при хипоксично-исхемично мозъчно увреждане. Нашите открития показват, че лечението с биосинтезиран NB-EPA значително облекчава размера на мозъчния инфаркт и подобрява невроповеденческите разстройства след хипоксично-исхемично увреждане на мозъка при новородени мишки. NB-EPA инхибира апоптозата на невронни клетки след исхемично предизвикателство. NB-EPA подобрява оцеляването и пролиферацията на невронните клетки чрез активирането на фосфорилираното AKT сигнализиране. Трябва да се отбележи, че защитното свойство на NB-EPA срещу исхемично увреждане на невроните зависи от потискането на пътя p53-PUMA. Взети заедно, тези открития предполагат, че NB-EPA може да представлява нов невропротектор за новородени с хипоксично-исхемична енцефалопатия.
Ключови думи:мака; N-бензил ейкозапентаенамид; неонатална хипоксично-исхемична енцефалопатия; невропротекция; PUMA
1. Въведение
Неонаталната хипоксично-исхемична енцефалопатия (HIE) е честа причина за мозъчно увреждане поради лишаване от кислород и намаляване на кръвния поток [1,2]. HIE е изключително противно на развитието на мозъка, което е основният фактор, причиняващ неврологична дисфункция при децата [3]. Най-честите последици от HIE включват церебрална парализа, тежко когнитивно увреждане и двигателни и поведенчески дефицити, което води до милиони неонатални смъртни случаи или дълготрайни увреждания всяка година [4]. Терапевтичната хипотермия е клинично обичайното лечение за неонатални пациенти с HIE и е доказано, че подобрява неврологичните резултати при оцелелите [5]. Въпреки това, само използването на лечение с хипотермия не е достатъчно за намаляване на смъртността или избягване на тежки нарушения на неврологичното развитие при тежка HIE [6]. Въпреки значителния напредък в съвременните медицински технологии, няма ефективно медицинско лечение за увреждане на нервите, причинено от HIE [7]. Невропротективната терапия е от голямо значение за дългосрочното възстановяване на мозъчната функция [8]. Следователно е необходимо да се разработят безопасни и ефективни невропротективни терапевтици.

от къде мога да купя кора от цистанче
Мака(Lepidium meyenii) е едногодишна или двугодишна билка от южноамериканското семейство кръстоцветни, която беше класифицирана като нова ресурсна храна през 2011 г. [9,10]. Разнообразие от компоненти с фармакологични и хранителни ефекти са идентифицирани в мака, което включва полизахариди, фитостероли, алкалоиди, глюкозинолати, макаени имакамиди[11,12]. Сред тези биоактивни съставки, макамидите, група от неполярни, дълговерижни N-бензил амидни съединения на мастни киселини, са признати за характерни съставки, като същевременно допринасят за основните ефикасности на мака като против умора, против остеопороза и подобряване на плодовитостта [13]. -15]. Наскоро се съобщава, че макамидите и техните синтетични аналози проявяват отчетлива инхибиторна активност на амид хидролазата на мастни киселини (FAAH), което предполага, че тези съединения притежават потенциална невропротективна и противовъзпалителна активност [16,17].

цистанче тубулоза
В настоящото изследване е идентифициран нов вид максимизиращ N-бензил ейкозапентаенамид (NB EPA) отмака. Ние допълнително изследваме неговите биологични активности върху хипоксично-исхемично увреждане на мозъка. Нашите открития показват, че NB-EPA значително подобрява HI-медиираното неонатално мозъчно увреждане чрез подобряване на мозъчния инфаркт и поведенческите разстройства. Трябва да се отбележи, че невропротективният ефект на NB-EPA върху оцеляването на исхемичните неврони зависи от потискането на сигналния път на p53-PUMA.
2. Резултати
2.1. Идентификация и синтез на N-бензил ейкозапентаенамид
Макамидиса клас амидни алкалоиди, образувани от бензиламин и част от мастна киселина, които се считат за характерните маркерни съединения намака. Тук идентифицирахме ново максимизиране, NB-EPA (молекулна формула C27H37NO), от мака. Както е показано на Фигура 1А, високоефективната течна хроматография с електроспрей йонизираща масспектрометрия (HPLC-ESI-MS/MS) показва два пика, които са записани в общата йонна хроматограма на m/z 392.3 с времена на задържане 7.{{1 0}} мин. и съответно 9.0 мин. MS/MS спектърът демонстрира, че информацията за фрагмента на пика с време на задържане от 7,0 минути е в съответствие с теоретичните фрагменти на NB-EPA (Фигура 1В). Основният йонен пик на фрагмента, открит от този нов макамид, беше m/z 91,1, съответстващ на бензила [C7H7] плюс . Пиковете на йонните фрагменти на MS/MS от страната на мастните киселини са в съответствие с докладваните MS/MS данни за ейкозапентаенова киселина в уеб книгата по химия на Националния институт за стандарти и технологии (NIST) (SRD 69).
Поради ниското съдържание на NB-EPA вмака, след това синтезирахме NB-EPA, използвайки метода на карбодиимидна кондензация. Синтезираната смес се пречиства чрез полупрепаративна HPLC система. Фракцията с време на задържане от 23,5 до 25,5 минути беше събрана и чистотата на събраната фракция достигна 98,2 процента (Фигура 1C, D). HPLC-MS/MS анализът показа, че биосинтезираната NB-EPA и естествената NB-EPA имат идентични характеристики на хроматографско разделяне и информация за вторичен масспектрометричен фрагмент (Фигура 1E–G). Заедно тези данни предполагат, че новмакамидNB-EPA беше идентифициран отмакаи успешно синтезиран.
2.2. NB-EPA намалява инфарктните обеми и невроповеденческите дефицити при неонатална HI мозъчна травма
След това изследвахме биоактивността на NB-EPA при новородени мишки след хипоксично-исхемично (HI) мозъчно увреждане. Изображенията на външния вид на мозъка показват, че исхемичната мозъчна тъкан става бяла и подута в групата с носител на дни 1, 3, 7 и 14 след HI (Фигура 2А). Обратно, прилагането на NB-EPA в доза от 250 µg/ден за 3 d значително облекчава подуването на мозъка и съдържанието на мозъчна вода (Фигура 2A, B). Оцветяването с 2,3,5-трифенил тетразолиев хлорид (TTC) показва, че лечението с NB-EPA (11,13 ± 2,58 процента) ясно намалява размера на мозъчния инфаркт 3 дни след HI в сравнение с носителя (37,01 ± 4,68 процента ) (Фигура 2C). Невроповеденческите тестове показаха, че мишките в групата с носител показват значителни невроповеденчески разстройства на 1, 3 и 7 ден след HI (Фигура 2D–F). Напротив, лечението с NB-EPA ясно подобри тези неврологични дефекти (Фигура 2D–F). По този начин, тези данни показват, че NB-EPA предпазва от исхемични лезии и невроповеденчески дефицити при новородени мишки след HI мозъчно увреждане.
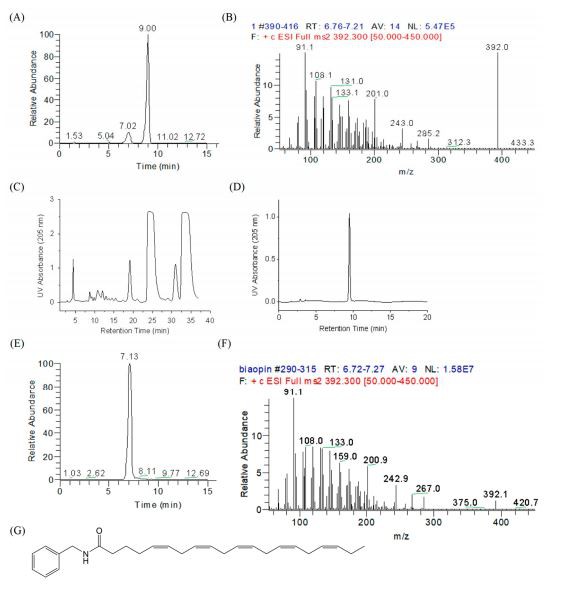
Фигура 1. Хроматограми и MS/MS спектри на естествен NB-EPA и синтетичен NB-EPA. (A) Представителна хроматограма на общ йонен ток (TIC), получена в режим на положително избран йонен мониторинг (SIM) за проба от екстракт от мака. (B) MS/MS спектри на m/z3923 ([NB-EPA плюс H]*) за пробата от екстракт от мака. (C) Полупрепаративна HPLC хроматограма на синтетични NB-EPA материали. (D)HPLC хроматограма на NB-EPA фракции (23.5-25.5 минути), събрани от полупрепаративна HPLC система. (E) Представителна TIC хроматограма, получена в положителен SIM режим за синтетична NB-EPA проба. (F) MS/MS спектри на m/z 392.3 за биосинтетична NB-EPA проба (G) Химическа структура на NB-EPA.
2.3. NB-EPA намалява индуцираното от HI мозъчно увреждане чрез потискане на невронната апоптоза
След това проучихме дали защитата на NB-EPA при HI мозъчно увреждане е замесена в модулирането на невронната смърт. Оцветяването с хематоксилин-еозин (HE) показа, че подреждането на невроните в кортекса, хипокампуса dentate gyrus (DG), амоняка на Cornu (CA) 1 и CA3 областите са нарушени. и нервните влакна бяха разхлабени и вакуолизирани в исхемични мозъци след HI нараняване. Въпреки това, лечението с NB-EPA ясно отмени увреждането на невронните клетки (Фигура 3А). Western blot потвърди, че NB-EPA значително намалява експресията на проапоптотични протеини като p53, PUMA и Bax в исхемична мозъчна тъкан (Фигура 3B, C). В допълнение, антигенът на невронните ядра (NeuN) и двойното оцветяване с TUNEL демонстрират значително намаляване на броя на TUNEL плюс NeuN плюс клетките 7 дни след HI при мишки, третирани с NB-EPA (5,80 ± 1,35 процента) в сравнение с носители (14,39 ± ± 2,55 процента). (Фигура 3D). Заедно тези данни предполагат, че благоприятният ефект на NB-EPA при HI мозъчни инсулти е включен в инхибирането на апоптозата на невронните клетки.

Фигура 2. Приложението на NB-EPA намалява церебралния инфаркт и поведенческите дефекти при новородени мишки след HI мозъчно увреждане. (A) Представителни изображения на външния вид на мозъка на 1, 3, 7 и 14 дни след HI. (B) Статистически анализ на водното съдържание на мозъка от всяка група мишки на 3 дни след HI. (C) Представителни снимки на оцветени с TTC коронални мозъчни срезове от всяка група мишки на 3 дни след HI и количествен анализ на обема на инфаркта. (DF) Невроповеденчески резултати от рефлекса на геотаксис (D), реакция на избягване на скала (E) и тест за захващане (F) на 1, 3 и 7 дни след HI. Данните са средна ± стандартна грешка на средната стойност (SEM) ( n=8 на група).*стр<0.05 compared="" to="">
2.4. NB-EPA намалява индуцираното от HI мозъчно увреждане чрез потискане на невронната апоптоза
Оцветяването по Nissl показа, че голям брой неврони показват атрофия, подуване и ядрена пикноза и дори умират с изчезването на телата на Nissl в исхемичния мозък. За разлика от това, NB-EPA очевидно подобрява оцеляването на невроните и пренареждането на невроните след HI нараняване (Фигура 4A, B). Western blot показа, че NB-EPA повишава нивата на фосфорилиран AKT (p-AKT), действащ като сигнализация за оцеляване, в исхемична мозъчна тъкан 7 дни след HI предизвикателство (Фигура 4C, D). Doublecortin (DCX) е маркер за невронни прекурсори и млади мигриращи неврони [18], а Ki-67 е маркер за клетъчна пролиферация [19]. Третирането с NB-EPA (19,83 ± 1,25 клетки/mm3) забележително повишава броя на Ki-67 плюс DCX плюс клетките 7 дни след HI в сравнение с носителя (11,83 ± 1,08 клетки/mm3) (Фигура 4E). Следователно, тези данни предполагат, че NB-EPA улеснява оцеляването и пролиферацията на невроните при новородени мишки след HI мозъчно увреждане.
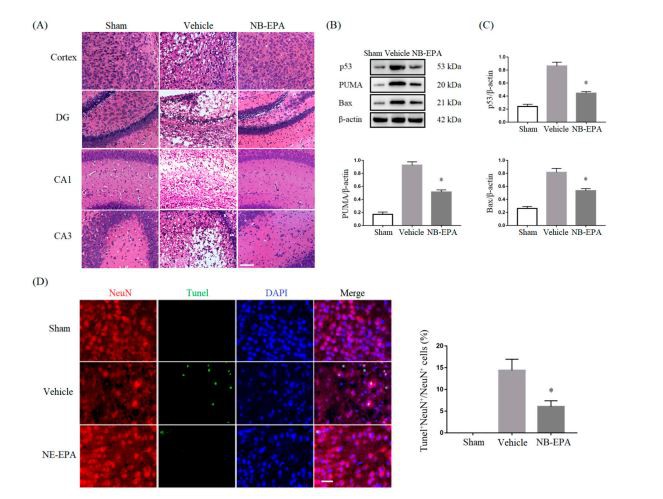
Фигура 3. NB-EPA инхибира смъртта на невроните при новородени мишки след HI мозъчно увреждане. (A) Представителни снимки на HE оцветяване в кората, хипокампуса DG, CA1 и CA3 региони от всяка група мишки на 7 дни след HI (мащабна лента, 75 μm). (B) Представителни Western blot изображения на p53, PUMA, и Bax от всяка група мишки на 7 дни след HI. (C) Денситометричният анализ на данните е показан в (B). (D) Представителни изображения на NeuN (червено) и TUNEL (зелено) от всяка група мишки на 7 дни след HI (вляво, мащабна лента, 25 um) в мозъчната кора; Количествено определяне на NeuN и TUNEL двойно маркирани клетки на 7 дни след HI (вдясно). Данните са средни ± SEM (n =8 за група). *стр<005 compared="" to="">

cistanche pdf
2.5. NB-EPA намалява индуцираното от HI мозъчно увреждане чрез потискане на невронната апоптоза
Въз основа на горния защитен ефект на NB-EPA при неонатално HI увреждане на мозъка, ние допълнително оценихме прякото влияние на NB-EPA върху оцеляването на невроните in vitro. Първичните кортикални неврони, култивирани в продължение на 7 дни in vitro, бяха кръгли и малки, с богати синапси и взаимосвързани мрежи (Фигура 5А). Чистотата на невроните се определя чрез поточна цитометрия и положителният процент е над 95 процента (Фигура 5B). NeuN* невроните също бяха идентифицирани чрез имунофлуоресценция (Фигура 5C). Тези резултати показват, че първичните кортикални неврони са успешно култивирани.

Фигура 4. NB-EPA подобрява оцеляването и пролиферацията на невроните при новородени мишки след HI мозъчно увреждане. (A) Представителни снимки на оцветяване с Nissl в регионите на кората, хипокампуса DG, CAl и CA3 от всяка група мишки на 7 дни след HI (мащабна лента, 75 μm). (B) Статистическият анализ на броя на невроните е показан в (A). (C) Представителни Western blot изображения на p-AKT и AKT от всяка група мишки на 7 дни след H. (D) Денситометричният анализ на данните е показан в (C). (E) Представителни изображения на DCX (зелено) и Ki -67 (червено) от всяка група мишки на 7 дни след HI (вляво, мащабна лента, 25 um) в региони на DG на хипокампуса; количествено определяне на DCX и Ki-67 двойно маркирана клетка на 7 дни след HI (вдясно). Данните са средни ±SEM (n=8 за група).*p<0.05 compared="" to="">
След това невроните бяха подложени на 3 часа лишаване от кислород-глюкоза (OGD) и третирани с различни концентрации на NB-EPA. Хипоксичните неврони се появяват с атрофия и ядрена пикноза в носител, третирани с PBS култури. Обратно, лечението с NB-EPA значително подобрява оцеляването на невроните след OGD (Фигура 5D). Преживяемостта на невроните беше измерена 24 часа по-късно с помощта на анализ на комплект за броене на клетки-8(CCK-8). Както е показано на фигура 5E, лечението с NB-EPA очевидно е спасило степента на оцеляване на невроните след OGD iniury. Максималната ефикасност на NB-EPA беше постигната при 1 μM, който беше използван за всички следващи in vitro експерименти. Анализът на поточната цитометрия потвърди, че броят на анексин-позитивните неврони в третираните с NB-EPA култури е значително намален в сравнение с третираните с носител PBS култури (Фигура 5F). Междувременно лечението с NB-EPA също значително инхибира експресията на протеини, свързани с апоптоза, включително p53, PUMA и Bax в неврони, обусловени от OGD (Фигура 5G, H). Следователно, тези данни предполагат, че NB-EPA отслабва невронното увреждане чрез регулиране на оцеляването на невроните, като същевременно инхибира невронната апоптоза.
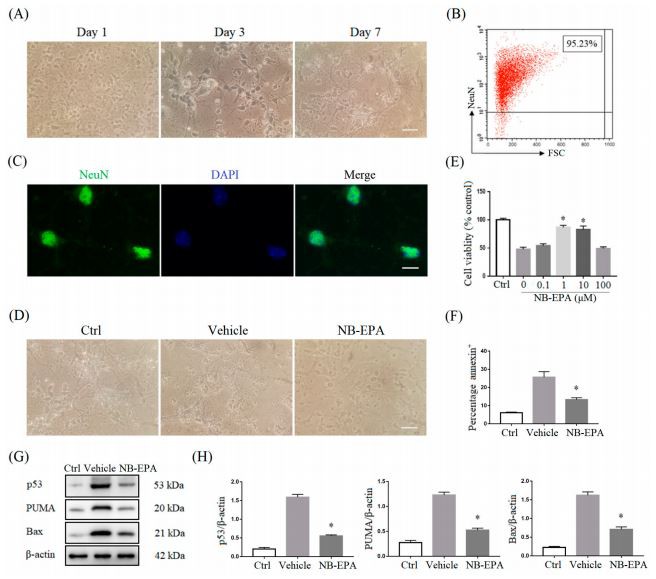
Фигура 5. NB-EPA намалява исхемичното невронно увреждане след OGDchallenge. (A) Представителни изображения на първични кортикални неврони, култивирани на 1, 3 и 7 дни (мащабна лента, 25 μm). (B) Процентът на NeuN плюс клетки от първични кортикални неврони, култивирани в продължение на 7 дни in vitro. (C) Представителни изображения на NeuN (зелено) и 4',6-диамидино-2-фенилиндол (DAPI) ( синьо) от първични кортикални неврони, култивирани в продължение на 7 дни in vitro (мащабна лента, 10 um). (D) Представителни изображения на първични кортикални неврони от всяка група при 24 h култура след 3 часа OGD (мащабна лента, 25 μm). (E)CCK-8 анализ в обогатени с неутрони култури, подложени на 3 h OGD или контролни условия, последвани от третиране с диапазон от концентрации на NB-EPA за още 24 h. (F) Процентът на анексиращите неврони на 24 h на култура след 3 часа OGD. (G) Представителни Western blot изображения на p53, PUMA и Bax от всяка група при 24 часа култура след 3 часа OGD. (H) Денситометричният анализ на данните е показан в (G). Данните са средни ±SEM (n =3 във всяка група).* p<0.05 compared="" to="">
2.6. NB-EPA защитава невроните от апоптоза чрез потискане на p53-PUMA
Сигнализиране Известно е, че пътят p53–PUMA участва в индуцирана от исхемия/реперфузия апоптоза на церебрални невронални клетки [20]. Тук проучихме дали защитата на NB-EPA срещу невронална смърт е свързана с инхибирането на пътя p53–PUMA. Както е показано на Фигура 6А, NB-EPA отменя обусловената от OGD клетъчна апоптоза, но няма ефект върху проби, предварително третирани с пифифитрин- (PFT), инхибитор на р53. Междувременно лечението с NB-EPA значително инхибира експресията на проапоптотичен протеин Bax в OGD-кондиционирани неврони, но няма ефект върху тези, които са били предварително третирани с PFT (Фигура 6B). Експресията на PUMA се повиши забележимо в невроните след предизвикателството с OGD, докато експресията на PUMA иРНК и протеин не се промени в предварително третирани с PFT неврони, което показва, че индукцията на PUMA в невроните е p53-зависима (Фигура 6C). Лечението с NB-EPA инхибира индуцираната от OGD експресия на PUMA в неврони, но няма ефект върху предварително третирани с PFT неврони (Фигура 6C). Церебралните неврони със специфично заглушаване на PUMA показват по-нисък процент апоптотични клетки (Фигура 6D) и намалена експресия на Bax протеин (Фигура 6E) на 24 часа след OGD предизвикателството в сравнение с PUMA-експресиращи неврони. Следователно, тези данни показват, че медиираното от NB-EPA инхибиране на OGD-индуцираната невронна апоптоза до голяма степен зависи от потискането на пътя p53–PUMA.

Фигура 6. NB-EPA намалява невронната апоптоза чрез инхибиране на p53-PUMA пътя. (A) Процентът на анексин плюс неврони с или без инхибиране на р53 при 24 часа култура с или без NB-EPA и след 3 часа OGD. (B) Представителни Western blot изображения на Bax с или без инхибиране на р53 при 24 часа култура с или без NB-EPA и след 3 часа OGD (вляво); денситометричен анализ на експресията на Bax протеин (вдясно). (C) PUMA mRNA експресия в неврони на 12 h от културата със или без NB-EPA и след 3 h OGD (вляво); средни проценти на експресия на PUMA протеин в неврони на 24 h култура с или без NB-EPA и след 3 h OGD (вдясно). (D) Процентът на анексинови неврони с или без PUMA нокдаун при 24 h култивиране с или без NB-EPA и след 3 h OD. (E) Представителни Western blot изображения на Bax с или без PUMA нокдаун при 24 h култивиране с или без NB-EPA и след 3 часа OGD (вляво); денситометричен анализ на експресията на Bax протеин (вдясно). Данните са средни ± SEM (n=3 за група).*p< 0.05="" compared="" to="" vehicle.="" n.s.="" not="">
3. Дискусия
Неонаталното хипоксично-исхемично увреждане, причинено от перинатална асфиксия, е едно от най-честите заболявания в неонаталния период. Липсват ефективни фармацевтични терапевтични интервенции, които намаляват церебралното увреждане или подобряват неврологичната функция при кърмачета [21]. В настоящото проучване открихме, че лечението с нов макамид NB-EPA значително облекчава хипоксично-исхемичното увреждане на мозъка при новородени мишки. Невропротекцията на NB-EPA е свързана с повишаване на регулацията на оцеляването на невроните, като същевременно инхибира невронната смърт. Трябва да се отбележи, че NB-EPA-медиираният антиапоптотичен механизъм зависи от потискането на p53-PUMA сигнализирането. Макамидите, известни като характерните маркерни съединения на мака, се състоят от бензиламин и част от мастна киселина с дълга верига с различна степен на ненаситеност [22].
Съобщава се за двадесет и три вида макамиди в екстракта от мака, сред които N-бензилхексадеканамидът е най-разпространеното съединение в мака от Перу, докато N-бензил-9Z,12Z-октадекадиенамидът е най-богатото съединение в мака Юнан [23]. В това проучване ние идентифицирахме нов макамид NB-EPA в мака от Юнан. Макамидът NB-EPA е съставен от бензиламин и ейкозапентаенова киселина (EPA; 20:5, n-3), един от основните компоненти на омега-3 полиненаситената мастна киселина (n-3 PUFA ). Съобщава се, че n-3 PUFA и техните метаболити съществуват в централната нервна система и играят решаваща роля в мозъчната функция и заболяване, като невротрансмисия, неврогенеза и невровъзпаление [24]. Трябва да се отбележи, че някои проучвания предполагат, че EPA, а не n-3 PUFAs и докозахексаенова киселина (DHA; 22:6, n-3), е свързана с по-ниски рискове от повечето видове исхемичен инсулт [25 ]. В съгласие с тези констатации, ние демонстрирахме, че този нов макамид NB-EPA не само облекчава мозъчното увреждане, но също така подобрява невроповеденческите дефицити след HI нараняване. Невроните са най-основните структурни и функционални единици на нервната система, които имат функцията да свързват и интегрират входящата информация и да изпращат информация. При увреждане на мозъка, причинено от хипоксия и исхемия, се увреждат голям брой неврони, което от своя страна причинява неврологична дисфункция. p53, ключов регулатор на реакцията на клетъчния стрес, може да се активира в исхемичните области след мозъчно увреждане [26]. Той може да насърчи невронната апоптоза, а дефицитът на р53 или прилагането на инхибитори на р53 може значително да намали увреждането на мозъка при различни модели на инсулт [27]. p53-медиираната апоптоза възниква чрез различни молекулярни механизми, сред които PUMA, ap53- и регулиран нагоре модулатор на апоптозата, е мощен проапоптотичен ген след p53 [28]. Проучванията показват, че пътят p53–PUMA участва в индуцирана от митохондриални инхибитори апоптоза на неврони на стриатума при плъхове [29].

увреждане и заболяване на бъбрецитеcistanche propiedades
Инхибирането на активирането на обратната връзка на p53–PUMA от p53 инхибитори и PUMA siRNA може да намали невроналната апоптоза и възпалението, предизвикано от исхемия-реперфузия [30]. Тук нашите открития са в съответствие с тези проучвания, показващи, че PUMA е силен изпълнител на p53-медиирана апоптоза в неврони след HI мозъчно увреждане. Лечението с NB-EPA инхибира HI-индуцираното повишаване на PUMA в невроните. Освен това, защитните ефекти на NB-EPA върху оцеляването на невроните зависят до голяма степен от потискането на PUMA сигнализирането. Допълнителни доказателства показват, че n-3 PUFA допринасят за оцеляването на невроните и неврогенезата след исхемично церебрално увреждане [31,32]. Те могат да подобрят прогнозата на инсулт и да ограничат по-нататъшното увреждане на невроните [33]. Въпреки че исхемичният инсулт индуцира пролиферацията и диференциацията на невронни прогениторни клетки в субвентрикуларната зона (SVZ), повечето от новосъздадените неврони умират скоро след инсулт [34]. Съобщава се, че n-3 PUFA не само подобряват оцеляването на незрели неврони, но също така улесняват тяхното съзряване в кортикалния паренхим след увреждане от инсулт [35]. Напоследък няколко проучвания също така предполагат благоприятния ефект на макамидите за облекчаване на увреждането на невроните, което е свързано с подобряването на дихателната функция на митохондриите [36,37].
Пътят на AKT сигнална трансдукция играе важна роля в антиапоптозния механизъм. Когато мозъкът е наранен, пътят на AKT се активира и тялото инициира самозащита и възстановяване на нараняване, което води до повишена експресия на p-AKT [38–41]. В съответствие с тези констатации, ние наблюдаваме, че лечението с NB-EPA защитава оцеляването на невроните срещу HI-медиирано мозъчно увреждане чрез активиране на про-оцеляване AKT сигнализиране, като същевременно инхибира про-апоптотичния път.
Дълго време невробиолозите вярваха, че невронните стволови клетки (НСК) изчезват малко преди или след раждането и неврогенезата спира по това време. Идеята, че няма нови неврони в зрелия мозък, започва да се променя през 1960s. С развитието на изследванията беше установено, че NSC за възрастни съществуват главно в SVZ и субгранулираната зона (SGZ) на хипокампалния зъбчат гирус [42–44]. Освен това по-късно беше потвърдено, че НСК съществуват и в други обширни области на централната нервна система (ЦНС) [45]. Последните проучвания показват, че ендогенните НСК в кората могат да се активират след мозъчно увреждане, за да допринесат за възстановяването на хипоксично-исхемично мозъчно увреждане чрез самообновяване, пролиферация и генериране на нови неврони, астроцити и олигодендроцити [46,47] . DCX допринася за възстановяването на невроните чрез стабилизиране на микротубулите в невронните клетки и представлява маркер за проследяване на миграцията на нови неврони в увредените места на мозъка [48]. Хипоксично-исхемичното мозъчно увреждане и тежкото травматично мозъчно увреждане увеличават производството на нови неврони на стриатума, които експресират DCX [49]. Ki-67 е ядрен антиген, свързан с пролифериращи клетки, покриващ всеки цикъл на пролиферация, различен от G0 фазата. В това проучване приложението на NB-EPA очевидно насърчава неврогенезата, която е свързана с регулирането на Ki-67 плюс DCX плюс клетките след HI мозъчно увреждане. Въпреки това, дали увеличаването на броя на Ki -67 плюс DCX плюс клетките е свързано с пролиферацията и диференциацията на невронни стволови клетки, индуцирани от NB-EPA, все още трябва да бъде допълнително проучено.
Препратки
1 Thornton, C.; Rousset, C.; Кичев, А.; Миякуни, Й.; Vontell, R.; Бабурамани, АА; Флейс, Б.; Gressens, P.; Hagberg, H. Молекулярни механизми на неонатално мозъчно увреждане. неврол. Рез. Вътр. 2012, 2012, 506320. [CrossRef]
2. Ма, К.; Zhang, L. Епигенетично програмиране на хипоксично-исхемична енцефалопатия в отговор на фетална хипоксия. Прог. Neurobiol. 2015, 124, 28–48. [CrossRef] [PubMed]
3. Conforti M, HD; Дениз, BF; де Алмейда, В.; Мигел, PM; Bronaugh, L.; Виейра, MC; де Оливейра, пр.н.е.; Pereira, LO Неонаталната хипоксия-исхемия причинява лека двигателна дисфункция, възстановена чрез акробатично обучение, без да се засягат морфологичните структури, участващи в моторния контрол при плъхове. Brain Res. 2019, 1707, 27–44. [CrossRef]
4. Йълдъз, ЕП; Екичи, Б.; Tatlı, B. Неонатална хипоксично-исхемична енцефалопатия: Актуализация на патогенезата и лечението на заболяването. Експерт. преп. Неуротер. 2017, 17, 449–459. [CrossRef]
5. Azzopardi, DV; Strohm, B.; Едуардс, AD; Dyet, L.; Халидей, HL; Juszczak, E.; Kapellou, O.; Левен, М.; Марлоу, Н.; Портър, Е.; et al. Умерена хипотермия за лечение на перинатална асфиксична енцефалопатия. Н. англ. J. Med. 2009, 361, 1349–1358. [CrossRef] [PubMed]
6. Tagin, MA; Woolcott, CG; Vincer, MJ; Уайт, РК; Stinson, DA Хипотермия за неонатална хипоксично-исхемична енцефалопатия: актуализиран систематичен преглед и мета-анализ. арх. Pediatr. Юношески Med. 2012, 166, 558–566. [CrossRef] [PubMed]
7. Торесен, М.; Sabir, H. Епилепсия: Неонаталните гърчове все още нямат безопасно и ефективно лечение. Nat Rev Neurol. 2015, 11, 311–312. [CrossRef] [PubMed]
8. Nair, J.; Kumar, VHS Текущи и нововъзникващи терапии при лечението на хипоксична исхемична енцефалопатия при новородени. Деца 2018, 5, 99. [CrossRef] [PubMed]
9. Гонзалес, GF; Gonzales, C.; Gonzales-Castañeda, C. Lepidium meyenii (Мака): Растение от планините на Перу – от традицията към науката. Форш. Допълнено. 2009, 16, 373–380. [CrossRef]
10. Чен, Л.; Li, J.; Fan, L. Хранителният състав на мака в хипокотили (Lepidium meyenii Walp.), култивирани в различни региони на Китай. J. Качество на храните 2017, 2017, 3749627. [CrossRef]
11. Балик, MJ; Лий, Р. Мака: От традиционна хранителна култура до стимулант за енергия и либидо. Алтернативен. Там. Health Med. 2002, 8, 96.
12. Чен, SX; Li, KK; Кръчма, Д.; Jiang, SP; Чен, Б.; Чен, LR; Янг, З.; Ma, C.; Gong, XJ Оптимизиране на екстракция с помощта на ултразвук, HPLC и UHPLC-ESI-Q-TOF-MS/MS анализ на основни макамиди и макаени от мака (сортове на Lepidium meyenii Walp). Molecules 2017, 22, 2196. [CrossRef]
13. Янг, Q.; Джин, В.; Lv, X.; Дай, П.; Ao, Y.; Wu, М.; Deng, W.; Yu, L. Ефекти на макамидите върху капацитета за издръжливост и свойствата против умора при продължителни плуващи мишки. Pharm. Biol. 2016, 54, 827–834. [CrossRef] [PubMed]
14. Уанг, Т.; Слънце, CH; Zhong, HB; Gong, Y.; Cui, ZK; Xie, J.; Wang, YP; Liang, C.; Сао, HH; Чен, XR; et al. N-(3- метоксибензил)-(9Z,12Z,15Z)-октадекатриенамид насърчава образуването на кост чрез каноничния Wnt/-катенин сигнален път. Фитотер. Рез. 2019, 33, 1074–1083. [CrossRef]
15. Учияма, Ф.; Джикио, Т.; Такеда, Р.; Ogata, M. Lepidium meyenii (Maca) повишава серумните нива на лутеинизиращ хормон при женски плъхове. J. Ethnopharmacol. 2014, 151, 897–902. [CrossRef] [PubMed]
16. Аласмари, М.; Бьолке, М.; Kelley, C.; Махер, Т.; Pino-Figueroa, A. Инхибиране на амидна хидролаза на мастни киселини (FAAH) от макамиди. Mol. Neurobiol. 2019, 56, 1770–1781. [CrossRef]
17. Хуанг, YJ; Peng, XR; Qiu, MH Напредък на химическите съставки, получени от глюкозинолати в мака (Lepidium meyenii). Нац. произв. Биопроспект. 2018, 8, 405–412. [CrossRef] [PubMed]
18. Пиенс, М.; Мюлер, М.; Бодсън, М.; Baudouin, G.; Plumier, JC Кратка промоторна област нагоре по веригата медиира транскрипционната регулация на миши двоен кортин ген в диференциращи неврони. BMC. Neurosci. 2010, 11, 64. [CrossRef]
19. Рахманзаде, Р.; Hüttmann, G.; Gerdes, J.; Scholzen, T. Подпомогнато от хромофор светлинно инактивиране на PKI -67 води до инхибиране на синтеза на рибозомна РНК. Cell Prolif. 2007, 40, 422–430. [CrossRef]
20. Хонг, LZ; Джао, XY; Zhang, HL п53-медиирана невронална клетъчна смърт при исхемично мозъчно увреждане. Neurosci Bull. 2010, 26, 232–240. [CrossRef]
21. Вахтел, Е. В.; Верма, С.; Mally, PV Актуална информация за текущото управление на новородени с неонатална енцефалопатия. Curr Probl Pediatr. Юношески Здравеопазване 2019, 49, 100636. [CrossRef] [PubMed]
22. Уанг, С.; Zhu, F. Химичен състав и здравни ефекти на мака (Lepidium meyenii). Food Chem. 2019, 288, 422–443. [CrossRef]
23. Карвальо, Ф.В.; Ribeiro, PR Структурно разнообразие, биосинтетични аспекти и компилация на данни LC-HRMS за идентифициране на биоактивни съединения на Lepidium meyenii. Food Res. Вътр. 2019, 125, 108615. [CrossRef]
24. Bazinet, RP; Layé, S. Полиненаситени мастни киселини и техните метаболити в мозъчната функция и заболяване. Нац. Rev. Neurosci. 2014, 15, 771–785. [CrossRef] [PubMed]
25. Вено, Словакия; Bork, CS; Якобсен, MU; Lundbye-Christensen, S.; Макленън, Полша; Бах, FW; Overvad, K.; Schmidt, EB Marine n-3 Полиненаситени мастни киселини и рискът от исхемичен инсулт. Ход 2019, 50, 274–282. [CrossRef]
26. Йонекура, И.; Такаи, К.; Асаи, А.; Кавахара, Н.; Kirino, T. p53 потенцира хипокампалната невронна смърт, причинена от глобална исхемия. J. Cereb. Кръвотечение. Metab. 2006, 26, 1332–1340. [CrossRef] [PubMed]
27. Xie, YL; Джан, Б.; Jing, L. MiR-125b блокира Bax/Cytochrome C/Caspase-3 апоптотичен сигнален път в плъхове модели на церебрална исхемия-реперфузионно увреждане чрез насочване. неврол. Рез. 2018, 40, 828–837. [CrossRef] [PubMed] 28. Chen, H.; Тиан, М.; Джин, Л.; Jia, H.; Jin, Y. PUMA участва в индуцирана от исхемия/реперфузия апоптоза на миши церебрални астроцити. Неврология 2015, 284, 824–832. [CrossRef] [PubMed]
29. Джан, XD; Wang, Y.; Wang, Y.; Джан, X.; Хан, Р.; Wu, JC; Liang, ZQ; Gu, ZL; Хан, Ф.; Фукунага, К.; et al. p53 медиира активиране на автофагия, предизвикано от митохондриална дисфункция и клетъчна смърт в стриатум на плъх. Autophagy 2009, 5, 339–350. [CrossRef] [PubMed]
30. Ли, XQ; Ю, К.; Chen, FS; Тан, WF; Zhang, ZL; Ma, H. Инхибирането на аберантно активиране на веригата за обратна връзка на p53-PUMA отслабва индуцираната от исхемия реперфузия невроапоптоза и невровъзпаление при плъхове чрез понижаване на каспаза 3 и NF-кВ цитокиновия път. J. Neuroinflflamm. 2018, 15, 250. [CrossRef] [PubMed]
31. Ши, З.; Ren, H.; Luo, C.; Яо, X.; Устна.; Той, C.; Канг, JX; Уан, JB; Юан, TF; Su, H. Обогатени ендогенни омега-3 полиненаситени мастни киселини защитават кортикалните неврони от експериментално исхемично увреждане. Mol. Neurobiol. 2016, 53, 6482–6488. [CrossRef] [PubMed]
32. Белаев, Л.; Хонг, SH; Менгани, Х.; Марсел, SJ; Obenaus, A.; Freitas, RS; Khoutorova, L.; Балащук, В.; Джун, Б.; Ория, РБ; et al. Докозаноидите насърчават неврогенезата и ангиогенезата, целостта на кръвно-мозъчната бариера, защитата на Penumbra и невроповеденческото възстановяване след експериментален исхемичен инсулт. Mol. Neurobiol. 2018, 55, 7090–7106. [CrossRef]
33. Зендедел, А.; Хабиб, П.; Dang, J.; Lammerding, L.; Хофман, С.; Beyer, C.; Slowik, A. Omega-3 полиненаситените мастни киселини облекчават невровъзпалението и смекчават увреждането от исхемичен инсулт чрез взаимодействия с астроцити и микроглия. J. Neuroimmunol. 2015, 278, 200–211. [CrossRef]
34. Охаб, JJ; Флеминг, С.; Blesch, A.; Carmichael, ST Невроваскуларна ниша за неврогенеза след инсулт. J. Neurosci. 2006, 26, 13007–13016. [CrossRef] [PubMed]
35. Джан, В.; Wang, H.; Джан, Х.; Теч, РК; Shi, Y.; Ху, X.; Гао, Й.; Chen, J. Диетичните добавки с омега -3 полиненаситени мастни киселини силно насърчават невроваскуларната възстановителна динамика и подобряват неврологичните функции след инсулт. Exp. неврол. 2015, 272, 170–180. [CrossRef]
36. Гуняни, Канзас; Ву, Н.; Rondón-Ortiz, AN; Бьолке, М.; Махер, TJ; Pino-Figueroa, AJ Невропротективна активност на макамиди върху индуцирано от манган митохондриално разрушаване в U-87 MG глиобластомни клетки. Токсикол. Приложение Pharmacol. 2018, 340, 67–76. [CrossRef]
37. Джоу, Й.; Wang, H.; Guo, F.; Si, N.; Brantner, A.; Янг, Дж.; Хан, Л.; Вей, X.; Zhao, H.; Bian, B. Интегрирана протеомика и липидомично изследване на механизма, лежащ в основата на невропротективния ефект на N-бензилхексадеканамид. Molecules 2018, 23, 2929. [CrossRef] [PubMed]
38. Лиу, Й.; Liu, Y.; Джин, Х.; Cong, P.; Джан, Й.; Tong, C.; Ши, X.; Лиу, X.; Тонг, З.; Shi, L.; et al. Индуцираното от студов стрес мозъчно увреждане регулира TRPV1 каналите и PI3K/AKT сигналния път. Brain Res. 2017, 1670, 201–207. [CrossRef]
39. Xu, W.; Ли, Т.; Гао, Л.; Lenahan, C.; Zheng, J.; Ян, J.; Шао, А.; Zhang, J. Натриевият бензоат намалява вторичното мозъчно увреждане чрез инхибиране на невронната апоптоза и намаляване на медиирания от митохондриите оксидативен стрес в плъх модел на интрацеребрален кръвоизлив: възможно участие на DJ-1/Akt/IKK/NFκB път. Преден. Mol. Neurosci. 2019, 12, 105. [CrossRef]
40. Ли, Дж.; An, Y.; Wang, JN; Ин, XP; Джоу, Х.; Wang, YS Куркуминът е насочен към васкуларните ендотелни растежни фактори чрез активиране на сигналния път PI3K/Akt и подобрява хипоксично-исхемичното увреждане на мозъка при новородени плъхове. корейски. J. Physiol. Pharmacol. 2020, 24, 423–431. [CrossRef]
41. Ли, Т.; Xu, W.; Гао, Л.; Гуан, Г.; Джан, З.; Той, П.; Xu, H.; Фан, Л.; Ян, Ф.; Chen, G. Мезенцефалният невротрофичен фактор, получен от астроцити, осигурява невропротекция на ранно мозъчно увреждане, предизвикано от субарахноиден кръвоизлив чрез активиране на Akt-зависим път на просурвивалност и защита на целостта на кръвно-мозъчната бариера. FASEB J. 2019, 33, 1727–1741. [CrossRef]
42. Morshead, CM; Reynolds, BA; Крейг, CG; McBurney, MW; Стейнс, Вашингтон; Morassutti, D.; Weiss, S.; van der Kooy, D. Невронни стволови клетки в предния мозък на възрастни бозайници: относително неподвижна субпопулация от субепендимални клетки. Neuron 1994, 13, 1071–1082. [CrossRef]
43. Chiasson, BJ; Tropepe, V.; Morshead, CM; van der Kooy, D. Епендималните и субепендималните клетки на предния мозък на възрастни бозайници демонстрират пролиферативен потенциал, но само субепендималните клетки имат характеристики на нервните стволови клетки. J. Neurosci. 1999, 19, 4462–4471. [CrossRef] 44. Alvarez-Buylla, A.; Lim, DA В дългосрочен план: Поддържане на зародишни ниши в мозъка на възрастните. Neuron 2004, 41, 683–686. [CrossRef]
45. Vescovi, AL; Snyder, EY Establishment и свойства на клонове на нервни стволови клетки: Пластичност in vitro и in vivo. Мозъчен патол. 1999, 9, 569–598. [CrossRef] [PubMed] 46. Buffo, A.; Обред, И.; Tripathi, P.; Leiper, A.; Чолак, Д.; Хорн, AP; Мори, Т.; Götz, M. Произход и потомство на реактивна глиоза: източник на мултипотентни клетки в увредения мозък. Proc. Natl. акад. Sci. САЩ 2008, 105, 3581–3586. [CrossRef]
47. Ахмед, AI; Щая, АБ; Забен, MJ; Оуенс, EV; Kiecker, C.; Грей, WP Ендогенни GFAP-положителни невронни стволови/прогениторни клетки в постнаталната кора на мишка се активират след травматично мозъчно увреждане. J. Neurotrauma 2012, 29, 828–842. [CrossRef] [PubMed] 48. Horesh, D.; Сапир, Т.; Франсис, Ф.; Вълк, SG; Каспи, М.; Елбаум, М.; Chelly, J.; Reiner, O. Doublecortin, стабилизатор на микротубули. тананикам Mol. Женет. 1999, 8, 1599–1610. [CrossRef] [PubMed]
49. Ong, J.; Самолет, JM; Родител, JM; Silverstein, FS Хипоксично-исхемично увреждане стимулира пролиферацията на субвентрикуларната зона и неврогенезата при новородени плъхове. Pediatr. Рез. 2005, 58, 600–606. [CrossRef] [PubMed]
50. Шао, Й.; Li, Y.; Liu, T. Проучване за оптимизиране на процеса на екстракция на основните макамиди от Maca (Lepidium meyenii Walp.). Храна. Рез. Dev. 2017, 38, 35–39.
51. Скорупскайте, В.; Макаревичене, В.; Gumbyte, M. Възможности за едновременна екстракция на масло и трансестерификация по време на производството на биодизелово гориво от микроводорасли: преглед. гориво. Процес. техн. 2016, 150, 78–87. [CrossRef]
52. Райс, JE, 3-ти; Vannucci, RC; Brierley, JB Влиянието на незрелостта върху хипоксично-исхемично увреждане на мозъка при плъхове. Ан. неврол. 1981, 9, 131–141. [CrossRef] [PubMed]
53. Xiao, AJ; Чен, В.; Xu, B.; Лиу, Р.; Турлова, Е.; Barszczyk, A.; Слънце, CL; Лиу, Л.; Deurloo, М.; Wang, GL; et al. Морското съединение ксилокетал B намалява неонаталното хипоксично-исхемично увреждане на мозъка. Март. Наркотици 2014, 13, 29–47. [CrossRef] [PubMed]
54. Дзяо, М.; Ли, X.; Чен, Л.; Уанг, X.; Юан, Б.; Лиу, Т.; Dong, Q.; Mei, H.; Yin, H. Невропротективен ефект на IL-33, получен от астроцити, при неонатално хипоксично-исхемично мозъчно увреждане. J. Neuroinflflamm. 2020, 17, 251. [CrossRef] [PubMed]
