Рапамицин алтернативно модифицира динамиката на митохондриите в дендритните клетки, за да намали бъбречното исхемично реперфузионно увреждане
Feb 22, 2022
Резюме:Дендритните клетки (DCs) са уникални имунни клетки, които могат да свържат вродени и адаптивни имунни отговори и имунометаболизмът значително влияе върху техния фенотип. Рапамицинът е макролидно съединение, което има имуносупресивни функции и се използва за предотвратяване на загуба на присадка при бъбречна трансплантация. Настоящото проучване оценява терапевтичния потенциал на ex vivo третирани с рапамицин DC за защитабъбрецив миши модел на acuteувреждане на бъбреците (AKI). За еднократно (S) лечение с рапамицин (Rapa-S-DC), Veh-DCs бяха третирани с рапамицин (10 ng/mL) за 1 час преди LPS. Обратно, многократното (M) лечение с рапамицин (Rapa-M-DC) беше изложено на 3 лечения в продължение на 7 дни. Само множество ex-vivo лечения с рапамицин на DC индуцират постоянно препрограмиране на митохондриалния метаболизъм. Тези DC имат 18-кратно повече митохондрии, имат почти 4-кратно по-високи нива на потребление на кислород и произвеждат повече ATP в сравнение с Veh-DC (контролни DC, третирани с Veh). Анализът на пътя показва сигнализирането на IL10 като основен допринасящ път към променения имунофенотип след лечение с рапамицин в сравнение с носител със значително по-ниски цитокини Tnfa, Il1b и Il6, докато регулаторите на митохондриалното съдържание Pgc1a, Tfam и Ho1 остават повишени. Критично, адоптивен трансфер на DCs, третирани с рапамицин, към реципиенти на WT 24 часа преди двустраннобъбрекисхемия значително защити набъбрециот нараняване със значително 3-кратно подобрение набъбречна функция. И накрая, вливането на DCs, съдържащи по-висок брой митохондрии (третирани ex-vivo със здрави изолирани митохондрии (10 µg/mL) един ден преди това) също частично защитибъбрециот IRI. Тези проучвания показват, че превантивната инфузия на ex vivo препрограмирани DC, които имат по-високо съдържание на митохондрии, има терапевтичен капацитет да индуцира противовъзпалителен регулаторен фенотип за защитабъбрециот нараняване.
Ключови думи:дендритна клетка; рапамицин; митохондриите; остра бъбречна травма; исхемично реперфузионно увреждане
ВъведениеПатобиологията на острияувреждане на бъбрецитее многофакторен и включва сложни взаимодействия междубъбречнапаренхимни клетки и имунни клетки [1,2]. Вбъбрек,конвенционалните дендритни клетки (DC) са основната подгрупа на имунните клетки и се намират интимно в интерстициалното пространство вбъбрек[3–5]. DC са един от основните типове клетки, участващи във вродения имунитет и са от съществено значение за осигуряване на защита срещу патогени. Нашата по-рано публикувана работа, използваща DCs, получени от костен мозък, показа, че терапията с DCs може да регулира различни вродени и адаптивни имунни отговори, свързани с AKI [6,7].
DCs са разположени широко във всички тъкани, като подгрупа от DCs (CD11c плюс DCs) се намира вбъбречнапаренхим. Въпреки това, тези CD11c плюс DC също играят патогенна роля при влошаванебъбречно уврежданеслед исхемично-реперфузионно увреждане (IRI) [8]. IRI се дефинира като увреждане в резултат на повторно въвеждане на кислородна кръв към орган след период на исхемия и често се наблюдава при миокарден инфаркт, инсулт и трансплантация на твърди органи. В отговор на IRI, CD11c плюс DC съдържат значителна част от възпалителния клетъчен инфифилтрат вбъбречнатъкан.

DCs са способни да разпознават свързани с патогени молекулярни модели (PAMPs) чрез различни рецептори за разпознаване на образи, разположени на повърхността на DCs, като например tolllike рецептори (TLRs) и NOD-подобни рецептори. Свързването на рецептори за разпознаване на образи (PRRs) към техните специфични PAMPs води до активиране на няколко пътя, които включват провъзпалителни реакции, синтез на антимикробен пептид и индукция на лимфоцитно медииран адаптивен имунитет [9]. Значителни изследвания са посветени на изучаването на промените в клетъчната биоенергетика на DCs при активиране от PAMPs. Установено е, че активирането на DCs с липополизахарид (LPS; PAMP, различен от грамотрицателните бактерии), чрез свързване към неговия специфичен рецептор TLR4 води до метаболитна промяна от високоефективно окислително фосфорилиране до процес, много подобен на метаболизма на Варбург или аеробна гликолиза . Метаболизмът на Warburg се характеризира с отклоняване на пируват, генериран от гликолиза, към превръщане в лактат за производство на енергия и далеч от транспортиране в митохондриите, за да се подложи на катаболизъм чрез TCA цикъла, въпреки достатъчното наличие на кислород. Едно обяснение за това явление включва един от многото низходящи ефекти на активирането на TLR4, което е повишената активност на серин/треонин киназата, целта на рапамицин при бозайниците (mTOR). Инхибирането на mTOR от рапамицин запазва митохондриалната функция в активирани DCs чрез понижаване на iNOS, като DCs, третирани с рапамицин, стимулирани в присъствието на LPS, показват намалени нива на аеробна гликолиза [10]. Инхибитори на mTORC1 като рапамицин понастоящем се използват при трансплантация на твърди органи като възможна алтернатива на инхибиторите на калциневрин за избягване на хроничнибъбречнаувреждане на алографта, тъй като той също има потенциал за разширяване на CD4 плюс CD25 плюс регулаторни Т-клетки [11,12]. Въпреки това, употребата на рапамицин при трансплантация може да доведе до възпалителни усложнения, които включват периферен оток, повишаване на креатинина и тромбоцитопения. Предишни проучвания показват, че неблагоприятните ефекти на хипоксичните стимули се засилват от експозицията на LPS и се отслабват от рапамицин [8,13].
Целта е да се разработят методи за използване на одобрени от FDA клинични лекарства като Rapamycin за индуциране на регулаторни DC, които могат да контролират нежелани вродени и адаптивни имунни отговори. Целта на това проучване беше да се определи потенциалният защитен механизъм(и) на BMDCs, стимулирани с рапамицин, в предклиничен миши модел набъбрекIRI. Лечението на BMDCs ex vivo с рапамицин избягва всякакви неблагоприятни нецелеви ефекти и възпалителни усложнения, свързани със системни лекарствени инжекции. Оптималната доза и времето на повечето фармакологични съединения или лекарства зависят от различни параметри. В раковите клетки ниската доза рапамицин в сравнение с високата доза диференциално инхибира mTORC1 и mTORC2, което води до частично или пълно инхибиране на прогресията на клетъчния цикъл [14]. За всички наши проучвания за кондициониране на ex-vivo BMDCs в настоящия ръкопис ние избрахме ниската доза от 10 ng/mL рапамицин въз основа на докладвани по-рано проучвания с толерогенни BMDCs [15,16]. Времето за колко дози (три или една) се основава на нашата предишна публикувана работа с размножаване на миши BMDCs и добавено с GMCSF [17,18]. Нашите настоящи данни показват, че както единичното, така и многократното(ите) лечение(я) на DCs с рапамицин индуцира по-малко стабилни имуногенни отговори (по-ниски цитокини и костимулиращи молекули) след LPS стимулация. Прехвърлянето на единични или множество DCs, третирани с рапамицин, защитава еднаквобъбрециот IRI в сингенни (C57BL/6 BMDC→C57BL/6 мишки) или алогенни (BALB/c BMDC→C57BL/6 мишки) модели на IRI. Въпреки това, многократно ex-vivo лечение с рапамицин (3 лечения за 7 дни), в допълнение към намаляването на имуногенните отговори, също повишава броя и функцията на митохондриите (Seahorse Analyzer) в сравнение с DCs, третирани с носител. Тези експериментални наблюдения показват, че DCs с по-висок брой митохондрии имат потенциала да станат регулаторни и прехвърлянето на тези DCs може да защитибъбрециот исхемично увреждане. Както показа нашето скорошно проучване, използващо DCs, третирани с FTY720 [18], фармакологични или митохондриални трансплантации, които индуцират по-висок брой митохондрии в имунните клетки (DC или макрофаги), също карат тези клетки да имат противовъзпалителен фенотип, ефект, който вероятно се дължи на поддържането на митохондриите окислително фосфорилиране (OXPHOS) и с намалено преминаване към гликолиза за енергия след стимулация. За тези ефекти, ние екзогенно увеличихме броя на митохондриите в DC, за да проверим дали по-високият брой на митохондриите може да индуцира регулаторен фенотип чрез използване на митохондриални трансплантации. Прехвърлянето на тези Mito-DC е защитенобъбрециот IRI; въпреки това, за разлика от Rapa-DCs, тези Mito-DCs нямат намалени имуногенни отговори (MHCII, костимулиращи молекули и цитокини) след LPS стимулация, което вероятно показва, че увеличаването на броя на копията на митохондриите може да отмени функционалните промени, предизвикани от екзогенна LPS стимулация. В това проучване и както беше демонстрирано по-рано [6,7,18], системно инжектираните DCs (третирани с носител, рапамицин или митохондрии) в доза от половин милион се откриват предимно само в далака и не се открива никакъв сигнал вбъбреци. В далака като FTY720-DCs, богатите на рапамицин и митохондрии DC могат да предизвикат противовъзпалителен отговор, водещ до защита отбъбрекIRI. Тези семенни находки предоставят нови доказателства, които предполагат, че увеличаването на броя на митохондриите (екзогенно чрез митохондриални трансплантации или чрез фармакологична интервенция (FTY720 или рапамицин)) в имунните клетки може да бъде нов терапевтичен начин за окончателно регулиране на техните имунологични отговори за превенция и/или ранно лечение наувреждане на бъбреците.
Материали и методи
мишкиВсички процедури и манипулации с животни бяха извършени в съответствие с Ръководството за грижа и използване на лабораторни животни на Националните институти по здравеопазване, а номерът на протокола Bajwa UTHSC, 18-080, дата на одобрение 28.09.2018 г. беше одобрен от Университета на Институционални комитети за грижа и използване на животните в Центъра за здравни науки в Тенеси (UTHSC). Политиките за грижа за лабораторните животни следват Политиката на общественото здравеопазване за хуманна грижа и използване на лабораторни животни. Всички резултати се докладват по начин, съответстващ на насоките на ARRIVE [19]. За всички изследвания на трансфер C57BL/6J и BALB/c мишки бяха закупени от The Jackson Laboratory (Bar Harbor, ME, USA). Мишките се държат в стандартен вивариум с 12--часов цикъл светло/тъмно на диета с храна и вода е свободно достъпна.
Бъбречна исхемия-реперфузионно увреждане Всички подробни хирургични процедури бяха следвани, както беше съобщено по-рано [18]. C57BL/6 мъжки мишки (на възраст 8-12 седмици) бяха подложени на 26--минутна двустранна исхемия, последвана от 20-24 h реперфузия. Накратко, всички мъжки мишки бяха анестезирани с интраперитонеална (ip) инжекция от смес от кетамин и ксилазин, с подкожно инжектиране на бупренорфин и поставени върху топла подложка за поддържане на телесната температура при 34,5–36 ◦C. След това мишките бяха рандомизирани на фалшиво състояние или IRI операция. Извършен е двустранен хълбочен разрез. Телесната температура се проверява и поддържа през целия исхемичен период. Шамоперираните мишки са подложени на същата процедура, с изключение на клампиране на съдове и затваряне на хирургични рани. Мишки, които имаха такъвбъбрекбез реперфузия 24 часа след исхемия бяха изключени от всички анализи.
Оценка на бъбречната функция и хистологияБеше взета кръв под анестезия от ретро-орбиталния синус и плазменият креатинин (mg/dL) беше определен чрез използване на ензимен метод с незначителни модификации от протокола на производителя (Diazyme Laboratories, Poway, Калифорния, САЩ) и азот в кръвната урина (BUN ) и измерването на креатинина беше извършено с помощта на комплект за анализ на урея QuantiChrom (DIUR-100, BioAssay Systems, Hayward, Калифорния, САЩ), както е описано по-горе [18,20]. За хистологията,бъбрецибяха фиксирани за една нощ в 4% PLP или 10% формалин и вградени в парафин.Бъбрецибяха подготвени за H&E оцветяване, както е описано по-горе [18] и бяха направени снимки с настройка на яркост/контраст, направена с микроскоп EVOS (Thermo Fisher Scientifific, Waltham, MA, USA). За количествено определяне на оценката на тубулното нараняване, срезовете бяха оценени чрез преброяване на процента на тубулите, които показват клетъчна некроза, загуба на граница на четката, образуване на отливка и дилатация на тубулите, както следва: 0=нормално; 1=По-малко или равно на 10 процента; 2=10 до 25 процента; 3=26 до 50 процента; 4=51 до 75 процента; 5=По-голямо или равно на 75 процента. Пет до 10 полета от всяка външна медула бяха оценени и отбелязани по заслепен начин. Хистологичната промяна се изразява като остра тубулна некроза (ATN), оценявана, както е описано по-горе [7,21]. Апоптозните клетки бяха открити чрез TUNEL анализ (комплект за откриване на клетъчна смърт In Situ, TMR Red; Roche, Basel, Швейцария) съгласно инструкциите на производителя.

Култура на дендритни клетки (DC), извлечена от костен мозък (BM) и приемен трансферМъжки мишки C57BL/6J или BALB/c WT на възраст 8–1{12}} седмици бяха използвани за генериране на DC от цели BM прекурсори [22]. Богатият на GMCSF супернатант е получен от J558L клетки, стабилно трансфектирани с миши GMCSF. Клетъчната линия беше щедър подарък от д-р Ира Мелман (Катедра по биология, Йейлски университет, Ню Хейвън, Коннектикут, САЩ). Накратко, прясно изолиран BM се култивира с 6 ng/mL рекомбинантен миши GMCSF (общо 3 лечения) в продължение на 8 дни в RPMI 1640 (Invitrogen, Карлсбад, Калифорния, САЩ). Оптималната доза от 10 ng/mL рапамицин беше определена след тестване на различни дози (0,1–10 ng/mL). BMDC бяха третирани с 10 ng/mL рапамицин (Sigma, St. Louis, MO, USA) за общо три лечения или 1-лечение за една нощ). BMDCs бяха третирани с TLR4 агонист липополизахарид (LPS; Escherichia coli серотип 0111:B4: 100 ng/mL; Sigma-Aldrich); или носител (1 × PBS) за 24 часа в културална среда за сингенни изследвания (C57BL/6J BMDCs→C57BL/6J мишки) и оставени нетретирани за алогенни изследвания (BALB/c BMDCs→C57BL/6J мишки). Клетките се промиват и 0,5 × 106 клетки на мишка се инжектират интравенозно (iv) в наивни мишки 1 ден преди двустраннобъбрекIRI. BMDCs бяха белязани с MitoTracker CMXRos Red или MitoTracker Deep Red (100 nM, 30 минути при 37 °C, Invitrogen) или Mitosox (5 µM; 10 минути при 37 °C; Invitrogen).
Количествен PCR в реално времеОтносителното ниво на експресия на митохондриална ДНК (mtDNA) се измерва, както е описано по-горе [23]. Накратко, общата геномна ДНК беше изолирана и равни количества (5 ng) бяха използвани за RTPCR, използвайки ND1 като сурогатни праймери за mtDNA и HK2 праймери за ядрена ДНК (nDNA) за мишка и ND6 за човешка mtDNA, както е описано по-рано [23,24]. Тоталната РНК се изолира и се транскрибира обратно към сДНК и RT-PCR се извършва, както е описано по-горе [7,25,26].
Изолиране и количествено определяне на митохондриитеМитохондриите бяха изолирани от HEK293 клетки, както е описано по-горе [18]. Накратко, 60 cm плочи от HEK293 клетки бяха събрани чрез добавяне на 5 mL хомогенизиращ буфер (300 mmol/L захароза, 10 mmol/L HEPES-KOH, 1 mmol/L EGTA-KOH, pH 7,4) с 1 mg Subtilisin A протеаза от Bacillus licheniformis (Sigma-Aldrich). Подробен протокол за изолиране на митохондрии може да бъде намерен в нашия предишен публикуван ръкопис [18].
2 Биоанализатор Seahorse FluxСедемдневни BMDC бяха прехвърлени в плаки за тъканни култури с 24-ямки Seahorse и беше измерена скоростта на консумация на кислород (OCR) и параметрите бяха изчислени, както е описано по-горе [25] със следната модификация. След измерване на базалната респираторна честота, олигомицин (Sigma; 2 µM), FCCP (Sigma; 1,5 µM; карбонил цианид 4- (трифлуорометокси)-фенилхидразон (FCCP)) и инхибитори на електрон-транспортна верига (комплекс I и III), ротенон (Sigma; 0.5 µM) и антимицин А (Sigma; 0.5 µM)) бяха инжектирани последователно по време на анализа. Базално митохондриално дишане, ATP-свързано дишане, изтичане на протони (несвързана с ATP консумация на кислород), максимално дишане, немитохондриално дишане, резервен респираторен капацитет, съотношение на респираторен контрол и ефективност на свързване бяха определени в цели клетки съгласно Brand et al . [27]; N=4–5 ямки бяха използвани за всяка експериментална група и експериментите бяха повторени минимум 3 пъти.
Поточен цитометричен анализ, Western Blot и ELISAПолучаването на данни от поточна цитометрия беше извършено на FACS Calibur (Becton Dickinson, Сан Хосе, Калифорния, САЩ) с Cytek {{0}}цветна flflow цитометрична надстройка (Cytek Development, Inc., Fremont, CA, САЩ). Данните бяха анализирани от софтуер FlowJo 9.0 (Tree Star, Ashland, OR, САЩ), както е описано по-горе [6,7,28]. За ELISA средата се събира от BMDCs 24 часа след третиране със 100 ng/mL LPS. Нивата на TNF, IL6 или IL10 се измерват чрез използване на комплекти ELISA за мишки (Invitrogen), следвайки протокола на производителя и както е описано по-горе [18]. Veh- или Mito-DC, третирани с и без LPS за 6 или 24 часа, се използват за изолиране на общ протеин, като се използва RIPA лизисен буфер, допълнен с протеазен и фосфатазен инхибиторен коктейл (Thermo Fisher Scientifific, Vernon Hills, IL, USA). За GAPDH лизат супернатантите или се варят (10 минути при 100 ◦C) и лизатите се оставят на стайна температура за 10 минути за OXPHOS коктейл за гризачи (Abcam, Cambridge, MA, USA) [18]. По-подробни методи са описани по-рано [18].
Данни и статистически анализGraphPad Prism 8 (GraphPad Inc., Сан Диего, Калифорния, САЩ) беше използван за анализиране и представяне на данните. Данните бяха анализирани, след трансформация, ако е необходимо за генериране на нормално разпределение, чрез 2-опашен t тест или 1-way ANOVA с последващ анализ според случая. Двустранен несдвоен t тест беше използван за анализ на две групи. p По-малко или равно на 0.05 беше използвано за обозначаване на значимост.
Резултати
Многократно лечение с рапамицин (Rapa-M) индуцира по-висок брой митохондрии и по-малко имуногенни DCC57BL/6 WT DCs бяха изолирани и размножени в продължение на 8 дни в присъствието на GMCSF и носител (1X PBS) или рапамицин (10 ng/mL), общо три третирания. DC бяха третирани със 100 ng/mL LPS за една нощ. Третираните с LPS DCs бяха използвани за RNASeq или маркирани с различни митохондриални багрила. Данните от RNASeq потвърждават предишни данни, че лечението с рапамицин индуцира по-малко имуногенни DC с по-ниски провъзпалителни цитокини, които регулират вродени и адаптивни имунни отговори с IL10 като основен променящ се път (фигура S1A, B и таблица S1 на допълнителния материал). В сравнение с лечението с носител, лечението с рапамицин повишава митохондриалното съдържание в BMDCs (Фигура 1A), както е проверено с MitoTracker CMXRos Red (50 nM) със и без LPS. По подобен начин имаше значително по-високо маркиране с MitoTracker Deep Red (100 nM) и значително по-ниско маркиране с MitoSox (5 µM) и след LPS стимулация през нощта в Rapa-M-DC в сравнение с Veh-DC (Фигура 1B,C). Полу-количествено определяне на хистограмите MFI за всички митохондриални багрила (Фигура 1D). Освен това, Veh- и Rapa-M-DCs се оцветяват с помощта на JC-1, за да се провери дали лечението с рапамицин променя потенциала на митохондриалната мембрана. Многократното третиране с рапамицин не променя изходния мембранен потенциал на митохондриите в сравнение с третирани с носител контролни BMDCs, както е показано чрез имунофлуоресценция (фигура S2A на допълнителен материал) и проточна цитометрия (фигура на допълнителен материал S2B,C).

(Veh) и етикетирани с (A) MitoTracker CMXRos (50 nM) или (B) MitoSox (5 µM) или (C) MitoTracker Deep Red (100 nM) . (D) Полу-количествен анализ на MFI на митохондриални багрила, маркирани с flflow цитометрични данни. (E) DC бяха посяти в анализатор Seahorse XF-24e, стимулирани със и без LPS за 24 часа и скоростта на консумация на кислород (OCR) беше определена по време на последователно третиране с олигомицин (1), FCCP (2) и антимицин А/ротенон (3). (F) Количествено определяне на базалното производство на OCR и ATP. (G) нива на mRNA на Pgc1a и Tfam във Veh-DC и Rapa-M-DC, третирани със 100 ng/mL LPS или оставени нестимулирани за 24 часа. (H) Анализ на поточна цитометрия на MHC II, костимулиращи молекули (CD40/80/86) и експресия на PDL1 се определя със и без LPS стимулация. (I) ELISA на IL10, IL6 и TNF от Veh-DC и Rapa-M-DC, третирани със 100 ng/mL LPS за 24 часа. (J–L) нива на mRNA на Il10, Tnfa и Il6 във Veh-DC и Rapa-M-DC, третирани със 100 ng/mL LPS или оставени нестимулирани за 24 часа. * p По-малко или равно на 0,05, ** p По-малко или равно на 0,01 и *** p По-малко или равно на 0,001, еднопосочен ANOVA, последван от пост-теста на Tukey. Данните представляват средно ± SEM от три екземпляра.
Променена митохондриална функция, биоенергиен анализ беше оценен с помощта на Seahorse Bioanalyzer. Както се съобщава по-рано [18], LPS намалява консумацията на кислород в сравнение с Veh контролите във Veh-DCs, както се очаква (Фигура 1E, синя до черна линия). Интересно е, че rapa-M DCs със или без LPS имат по-висок базален OCR (Фигура 1E, зелена до синя линия при нулев момент). Rapa-M-DC демонстрира неуспех за увеличаване на максималния респираторен капацитет след инжектиране на FCCP в нестимулирани клетки, който се поддържа с LPS стимулация, демонстрирайки, че рапамицинът премахва резервния респираторен капацитет, както докладвахме преди това за работата с FTY-DC [18]. Третираните с LPS DC имат намалено производство на ATP, измерено чрез OCR (синьо към черно) в сравнение с Veh-DCs. Rapa-M-DC демонстрира значително по-голямо производство на ATP в сравнение с Veh-DC както в нестимулирани, така и в LPS-стимулирани DCs (Фигура 1F). Rapa-M-DCs показват повишени нива на mRNA за активиран от пероксизомен пролифератор рецепторен гама ко-активатор 1-алфа (Pgc1a) в сравнение с Veh-DCs (Фигура 1G) и генна експресия за Pgc1a и митохондриален транскрипционен фактор A (Tfam ) се поддържат в Rapa-M-DCs след LPS стимулация. Тези данни показват, че размножаването на BMDCs в присъствието на рапамицин повишава митохондриалното съдържание, базалното OCR и производството на ATP.
За да се тества дали рапамицин в допълнение към увеличаването на броя и функцията на митохондриите също предизвиква промяна в DC костимулиращи молекули след тестване на LPS. Интересното е, че след лечение с LPS, Rapa-M-DC има значително по-ниски нива на експресия на костимулиращи антиген представящи молекули (CD80, CD86 и CD40), MHCII и PDL1 в сравнение с Veh-DC (Фигура 1H, синьо срещу червено). Интересното е, че Rapa-M-DC имат подобни нива на експресия за PDL1 в сравнение с Veh-DCs, но имат значително увеличение на съотношението PDL1/CD86 след LPS стимулация в сравнение с третирани с LPS Veh-DCs, където PDL1/CD{{ 18}} намаля (Veh/Veh 0.59 ± 0.03 срещу Veh/LPS 0.43 ± 0.{{33 }}02, p < 0.001="" и="" rapa/veh="" 0,56="" ±="" 0,001="" спрямо="" rapa/lps="" 0,73="" ±="" 0,02,="" p="">< 0,05).="" не="" са="" наблюдавани="" значителни="" промени="" в="" експресията="" на="" cd11c="" между="" veh-="" и="" rapa-m-dcs,="" въпреки="" че="" rapa-m-dc="" има="" по-нисък="" сигнал="" на="" странично="" разсейване,="" показващ="" по-малкия="" размер="" на="" клетките="" след="" lps="" стимулация="" (данните="" не="" са="" показани).="" rapa="" m-dc="" имат="" по-високи="" относителни="" нива="" на="" mtdna/ndna="" в="" сравнение="" с="" veh-dc="" (105,7="" ±="" 8,7="" срещу="" 196,8,9="" ±="" 49,3),="" което="" показва,="" че="" лечението="" с="" рапамицин="" увеличава="" броя="" на="" dc="" митохондриите.="" рапамицинът="" значително="" намалява="" генната="" експресия="" на="" lps-индуцираните="" il6,="" il10="" и="" tnfa="" и="" протеиновите="" концентрации="" на="" tnf="" и="" il6,="" но="" поддържа="" по-високи="" нива="" на="" il10="" в="" сравнение="" с="" veh-dc,="" третиран="" с="" lps="" (фигура="" 1i–l).="" други="" гени,="" за="" които="" е="" известно,="" че="" се="" регулират="" от="" рапамицин="" (автофагия="" или="" възпаление),="" са="" изброени="" в="" таблица="" s2="" на="" допълнителния="" материал.="" гените="" след="" lps,="" посочени="" в="" зелено,="" са="" регулирани="" надолу="" и="" в="" червено="" са="" регулирани="" нагоре="" в="" сравнение="" със="" съответното="" третиране="" с="">
Прехвърлянето на Rapa-M-DC предпазва бъбреците от исхемично уврежданеВсички DC бяха активирани със 100 ng/mL LPS преди трансфера във всички сингенни изследвания (C57BL/6 BMDC→C57BL/6 мишки). Половин милион DC бяха инжектирани 1 ден преди 26-min двустраннобъбрекIRI. Схема на дизайна на изследването (Фигура 2A). Като контрола, мишките бяха инжектирани с 1 × PBS като контроли без клетки (NC). В сравнение с мишките, третирани с NC и Veh-DC, мишките, третирани с Rapa-M-DC, значително защитаватбъбрециот нараняване, плазмен креатинин (Фигура 2B); подобни промени в BUN са наблюдавани при тези мишки [Sham 41.30 ± 3.4 срещу NC 159.75 ± 3.2 срещу Veh-DC 151.82 ± 1.5 срещу Rapa-M-DC 114.68 ± 16.3; p <0,05 nc="" или="" veh-dc="" спрямо="" rapa-m-dc].="" морфологичните="" промени="" (фигура="" 2c,="" d)="" са="" успоредни="" на="" функционалните="" изследвания.="" мишките,="" третирани="" с="" rapa-m-dcs,="" имат="">бъбрекнива на иРНК на Kim1 [Veh DC 0.016 ± 0.009 срещу Rapa-M-DC {{2{{23} }}}.001 ± 0.002], Ngal [Veh-DC 2,14 ± 1,2 спрямо Rapa-M-DC 0,12 ± 0,09] и Tnfa [Veh-DC 0,19 ± 0,15 срещу Rapa-M-DC 0,0005 ± 0,0002] в сравнение с мишки, третирани с Veh-DC. В тези проучвания и както беше показано по-рано [6,7,17,18], мишки, третирани с Veh-DC в доза от половин милион, имат сравними промени вбъбречна функцияибъбрекцитокинов профил. В проучвания за сингенен трансфер, мишки, третирани с Rapa-M-DCs, имат намалена апоптоза (терминална дезоксинуклеотидил трансфераза, медиирана от дигоксигенин дезоксиуридин маркиране в крайния край [TUNEL]) в сравнение с мишки, третирани с Veh-DC (Veh-DC 3,8 ± 1,4 спрямо Rapa- M-DC 1,1 ± 0.6; p < 0.05);="" представителни="" изображения="" от="" tunel="" анализ="" са="" показани="" на="" фигура="" s3="" на="" допълнителния="" материал.="" интересното="" е,="" че="" няма="" значителни="" промени="" в="" броя="" на="" инфифилтриращите="" неутрофили="" при="" мишки,="" третирани="" с="" rapa-m-dc="" в="" сравнение="" с="" veh-dc="" (данните="" не="" са="" показани),="" което="" предполага,="" че="" мишките,="" третирани="" с="" rapa-m-dc,="" може="" да="" нямат="" промени="" в="" хемокините,="" въпреки="" че="" функцията="" на="" тези="" инфифилтриращи="" вродени="" имунни="" клетки="" може="" да="" бъде="">

Еднократно лечение с рапамицин (Rapa-S) индуцира по-малко имуногенни DC, без да променя митохондриалната динамикаСлед това тествахме дали еднократно лечение с рапамицин е достатъчно, за да индуцира регулаторен фенотип, като по този начин прави възможността за индуциране на регулаторен фенотип на DCs по-клинично значима. WT DC бяха изолирани и размножени в продължение на 8 дни в присъствието на GMCSF, общо три третирания. Седемдневни DCs бяха третирани с рапамицин (10 ng/mL) преди третиране с 100 ng/mL LPS за инкубиране през нощта и маркирани на следващия ден с MitoTracker CMXRos Червено (50 nM). В сравнение с лечението с носител, лечението с Rapa-S не променя митохондриалното съдържание в BMDCs (Фигура 3A) със и без LPS. По същия начин няма промяна в етикетирането с MitoTracker Deep Red (100 nM) и MitoSox (5 µM) и след LPS стимулация през нощта в Rapa-S-DC в сравнение с Veh-DC (Фигура 3B,C). Полу-количествено определяне на хистограмите MFI за всички митохондриални багрила (Фигура 3D). По подобен начин, за многократен анализ на третиране, Veh- и Rapa-S-DCs се оцветяват, като се използва JC{{20}}, за да се провери дали едно третиране с рапамицин променя потенциала на митохондриалната мембрана. Единичното третиране с рапамицин не променя изходния мембранен потенциал на митохондриите в сравнение с третирани с носител контролни BMDCs, както е показано чрез имунофлуоресценция (фигура S2A на допълнителен материал) и проточна цитометрия (фигура на допълнителен материал S2B,C). LPS намалява консумацията на кислород в сравнение с Veh контролите във Veh-DC, както се очаква (Фигура 3E, синя до черна линия). Rapa-S-DC нямат промяна в базалния OCR (Фигура 3E, зелена до синя линия при нулев момент). Когато производството на ATP беше количествено определено, LPS намали производството на ATP, измерено чрез OCR (синьо до черно) във Veh-DCs и Rapa-S-DC (Фигура 3F). Въпреки това, Rapa-S-DCs показват повишени нива на mRNA за Pgc1a в сравнение с Veh контролите и тези нива се поддържат в Rapa-S-DCs след LPS (Фигура 3G), малко или никаква промяна не се наблюдава в нивата на транскрипция на Tfam. След това тествахме дали еднократно лечение с рапамицин предизвиква промяна в DC костимулиращи молекули след LPS. Интересното е, че след лечение с LPS, Rapa-S-DC имат значително по-ниски нива на експресия на костимулиращи молекули за представяне на антиген (CD80, CD86 и CD40), MHCII, и PDL1 в сравнение с Veh-DC (Фигура 3H). Rapa-S-DCs имаха подобно ниво на експресия за PDL1 в сравнение с Veh-DCs и имаха подобни значими понижения в съотношението PDL1/CD86 след LPS стимулация в сравнение с Veh-DCs (Veh/Veh 0. 59 ± 0,03 спрямо Veh/LPS 0,43 ± 0,002, p < 0,001="" и="" rapa-s/veh="" 0,69="" ±="" 0,02="" спрямо="" rapa-s/lps="" 0,56="" ±="" 0,008,="" p="">< 0,05).="" еднократно="" лечение="" с="" rapamycin="" значително="" намалява="" генната="" експресия="" на="" lps-индуцирани="" il6,="" il10="" и="" tnfa="" заедно="" с="" по-ниски="" протеинови="" концентрации="" на="" il10="" с="" малка="" или="" никаква="" промяна="" в="" tnf="" и="" след="" лечение="" с="" lps="" (фигура="" 3i–l).="" други="" известни="" гени,="" които="" трябва="" да="" бъдат="" регулирани="" от="" rapamycin="" (автофагия="" [beclin,="" atg7,="" atg9,="" lc3b="" и="" lamp2]="" или="" възпаление="" [il1b,="" il12p40,="" tlr4,="" nos2,="" hif1a="" и="" ho1])="" са="" само="" частично="" регулирани="" в="" сравнение="" с="" dcs="" на="" носител="" след="" lps="" стимулация="" (допълнителна="" таблица="" на="" материалите="">
Прехвърлянето на Rapa-S-DC предпазва бъбреците от исхемично уврежданеВсички DCs бяха активирани със 100 ng/mL LPS или третирани с рапамицин (10 ng/mL) преди трансфер във всички сингенни изследвания (C57BL/6 BMDC→C57BL/6 мишки). Половин милион DC бяха инжектирани 1 ден преди двустраннобъбрекIRI. Схема на дизайна на изследването (Фигура 4A). Като контрола, мишките бяха инжектирани с 1 × PBS като контроли без клетки (NC). В сравнение с мишките, третирани с Veh-DC, мишките, третирани с Rapa-S-DC, значително защитаватбъбрециот увреждане плазмен креатинин (Фигура 4B); подобни промени в BUN са наблюдавани при тези мишки [Veh-DC 151.82 ± 1.5 срещу Rapa-S-DC 139.53 ± 3.8]. Морфологичните промени (Фигура 4C, D) са успоредни на функционалните изследвания. Мишките, третирани с Rapa-S-DCs, имат по-нискибъбрекнива на иРНК на Kim1 [Veh-DC 0.016 ± 0.{{10}}{{20}}9 срещу Rapa -S-DC 0.004 ± 0,002], Ngal [Veh DC 2,14 ± 1,2 спрямо Rapa-S-DC 0,14 ± 0,008] и Tnfa [Veh-DC 0,196 ± ± 0,15 срещу Rapa-S-DC 0,0017 ± 0,001] в сравнение с мишки, третирани с Veh-DC.


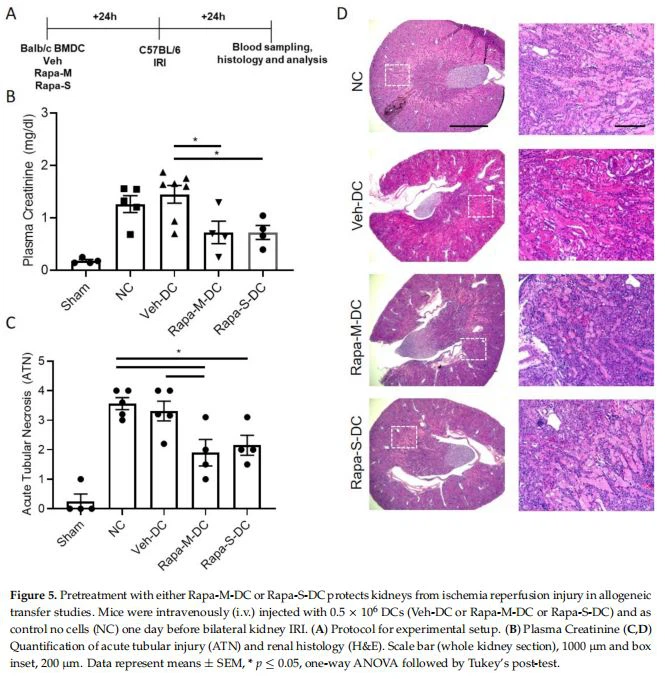
Алогенният BMDC трансфер на Rapa-M-DC или Rapa-S-DC предпазва еднакво бъбреците от исхемично уврежданеПоловин милион DC бяха инжектирани 1 ден преди двустраннобъбрекIRI за алогенни (BALB/C BMDC→C57BL/6 мишки) проучвания за трансфер. Схема на дизайна на изследването (Фигура 5A). Като контрола, мишките бяха инжектирани с 1x PBS като контроли без клетки (NC). В сравнение с мишките, третирани с Veh-DC, мишките, третирани с Rapa-M-DC или Rapa-S-DC, значително защитаватбъбрециот нараняване (Фигура 5B). Морфологичните промени (Фигура 5C, D) са успоредни на функционалните изследвания. Мишките, третирани с рапамицин DC, имат по-нискибъбрекнива на иРНК на Kim1 [Veh-DC 0.04 ± 0.{{10}}2 срещу Rapa-M-DC 0. 005 ± 0.0{{30}}2 срещу Rapa-S-DC 0.{{37} }05 ± 0.0002], Ngal [Veh-DC 0,57 ± 0,3 спрямо RapaM-DC 0,19 ± 0,11 спрямо Rapa- S-DC 0,05 ± 0,01] и Tnfa [Veh-DC 0,037 ± 0,02 срещу Rapa-M-DC 0,007 ± 0,003 срещу Rapa-S-DC 0,008 ± 0,005] в сравнение с мишки, третирани с Veh-DC. При проучвания за алогенен трансфер, мишки, третирани с Rapa-M-DC или Rapa-S-DC, имат намалена апоптоза TUNEL в сравнение с мишки, третирани с Veh-DC (Veh-DC 16,7 ± 8,2 спрямо Rapa-M-DC 7,2 ± 2,5 спрямо Rapa- S-DC 9,1 ± 0,1).
Екзогенни митохондриално заредени DC (Mito-DC) с по-висока митохондриална динамика и по-имуногенен фенотип след LPS стимулацияWT DC бяха изолирани и размножени в продължение на 8 дни в присъствието на GMCSF, общо 3 третирания. Седемдневни DC бяха третирани за една нощ с човешки екзогенни митохондрии (10 µg/mL). В сравнение с третирането с носител, третираните с митохондрии DC Mito-DC имат по-високи митохондрии. Митохондриите са изолирани от HEK293 човешка клетъчна линия. BMDCs бяха анализирани за наличието на човешки митохондрии в миши WT DCs, използвайки човешки mtDNA праймери за NADH дехидрогеназа (ND). Относителното човешко [mtDNA] съдържание във Veh-DC беше {{10}}.26 ± 0.10 спрямо 16.8 ± 0.59; p < 0,001,="" увеличение="" 63-кратно="" на="" геномна="" днк,="" изолирана="" от="" bmdcs.="" ограничение="" на="" настоящия="" анализ="" е,="" че="" той="" измерва="" човешка="" или="" миша="" mtdna="" спрямо="" ядрена="" днк="" и="" малкото="" количество="" човешка="" mtdna,="" открито="" във="" veh-dc,="" може="" да="" се="" дължи="" на="" незначително="" припокриване="" в="" последователността="" на="" nd="" в="" pcr="" анализа="" или="" на="" възможност,="" тъй="" като="" ние="" сме="" показваща="" относителна="" експресия="" към="" миша="" ядрена="" днк.="" за="" да="" се="" определи="" дали="" по-високото="" митохондриално="" съдържание="" също="" променя="" митохондриалната="" функция,="" беше="" извършен="" биоенергиен="" анализ="" с="" помощта="" на="" seahorse="" bioanalyzer.="" lps="" намалява="" консумацията="" на="" кислород="" в="" сравнение="" с="" veh="" контролите="" във="" veh-dcs,="" както="" се="" очаква="" (фигура="" 6a,="" синя="" към="" черна="" линия).="" mito-dcs="" имат="" по-висок="" базален="" ocr="" (фигура="" 6a,="" зелена="" до="" синя="" линия="" при="" нулев="" момент).="" при="" лечение="" с="" разединител="" fccp,="" mito-dc="" демонстрира="" неуспех="" да="" увеличи="" максималния="" респираторен="" капацитет="" в="" нестимулирани="" клетки,="" който="" се="" поддържа="" с="" lps="" стимулация,="" демонстрирайки,="" че="" лечението="" с="" изолирани="" митохондрии="" премахва="" резервния="" респираторен="" капацитет="" (вероятно="" защото="" вече="" е="" при="" максимален="" ocr="" в="" базално="" състояние).="" когато="" производството="" на="" atp="" беше="" количествено="" определено,="" lps="" намали="" производството="" на="" atp,="" измерено="" чрез="" ocr="" (синьо="" до="" черно)="" във="" veh-dcs.="" mito-dc="" демонстрира="" значително="" по-голямо="" базално="" производство="" на="" ocr="" и="" atp="" в="" сравнение="" с="" veh-dc="" в="" lps-стимулирани="" dcs="" (фигура="" 6b).="" mito-dcs="" показват="" повишени="" нива="" на="" mrna="" за="" pgc1a="" и="" интересно="" значително="" по-ниски="" tfam="" в="" сравнение="" с="" veh="" контролите="" (фигура="" 6c).="" разликите="" в="" pgc1a="" и="" tfam="" в="" този="" набор="" от="" експерименти="" след="" lps="" стимулации="" в="" сравнение="" с="" данните="" на="" фигури="" 1="" и="" 3="" вероятно="" се="" дължат="" на="" използването="" на="" balb/c="" bmdcs.="" в="" сравнение="" с="" c57bl/6="" bmdcs,="" dcs="" от="" balb/c="" имат="" значителни="" промени="" в="" производството="" на="" митохондрии="" и="" цитокини="" след="" стимулация="" [29,30].="" възможност="" поради="" тези="" промени="" в="" dcs,="" исторически="" ние="" сме="" използвали="" по-високо="" исхемично="" време="" при="" balb/c="" мишки="" в="" сравнение="" с="" c57bl/6,="" за="" да="" имаме="">бъбрекнараняване [6,18]. Тези данни показват, че прехвърлянето на екзогенни здрави митохондрии води до повишено митохондриално съдържание, базално OCR и производство на АТФ. Това предполага потенциал за противовъзпалителен фенотип в DCs след лечение с екзогенни митохондрии, както е показано в нашето предишно проучване [18]. След това тестваме дали DCs, третирани с екзогенни митохондрии, което води до увеличен брой и функция на митохондриите, също предизвиква промяна в DC костимулиращи молекули след LPS. Забележително е, че със и без LPS стимулация, Mito-DC има значително по-високи нива на експресия на костимулиращи антиген представящи молекули (CD80, CD86 и CD40), MHCII и PDL1 в сравнение с Veh-DC (Фигура 6D). Освен това, Mito-DC имат по-високо ниво на експресия за PDL1 в сравнение с Veh-DCs; въпреки това, те също имат увеличение на съотношението PDL1/CD86 след LPS стимулация в сравнение с Veh-DCs, третирани с LPS (данните не са показани). Mito-DC значително намали генната експресия на LPS-индуцирана Tnfa, но по-висока генна експресия на Il6 и Il10 в сравнение с Veh-DC и по-ниски протеинови концентрации на TNF и IL10, но поддържа по-високи нива на IL6 в сравнение с Veh-DC, третиран с LPS (Фигура 6E –H). Други гени, за които е известно, че се регулират от митохондриите (автофагия [Beclin, Atg7, Atg9, Lc3b и Lamp2] или възпаление [Il1b, Il12p40, Tlr4, Nos2, Hif1a и Ho1]) са частично регулирани след LPS стимулация (Таблица на допълнителния материал S3). Veh-DC и Mito-DCs бяха третирани с LPS за 6 и 24 часа. Бяха измерени относителни промени в митохондриалния комплекс. Mito-DC, третирани с и без LPS, имат значително по-високи протеинови нива на митохондриалните комплекси IV, II и I и значително по-ниски нива на комплекси V и III в сравнение с Veh-DCs (Фигура 6I). Полуколичествен анализ на относителната протеинова експресия на митохондриални комплекси към GAPDH (Фигура 6J). Петна с пълна дължина са предоставени като допълнителни фигури (фигури на допълнителни материали S4–S7).
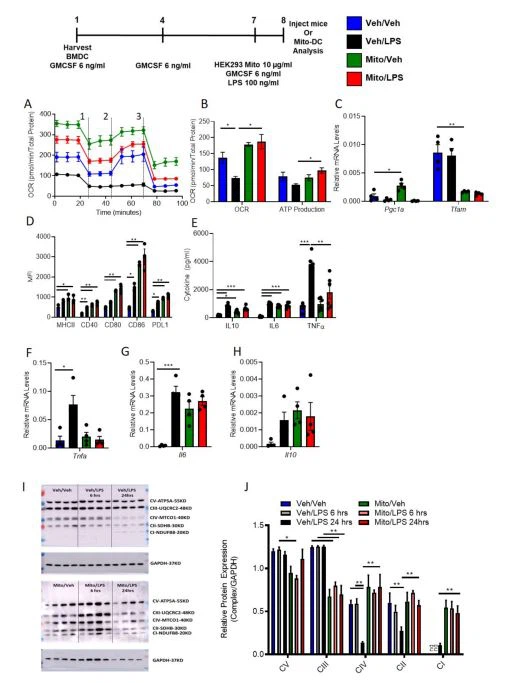
Фигура 6. Заредени с митохондрии DC (Mito-DC) имат по-висока митохондриална функция и имуногенност след LPS стимулация в сравнение с Veh-DC. Седемдневни Veh-DC и бяха инкубирани с 10 µg/mL HEK293 митохондрии един ден преди третиране с 100 ng/mL LPS за допълнителни 24 часа или оставени нестимулирани ( Veh). (A) 24 часа след добавяне на митохондрии, DCs се посяват в анализатор Seahorse XF-24e, стимулират се със и без LPS за 24 часа и се определя скоростта на консумация на кислород (OCR) по време на последователно третиране с олигомицин (1 ), FCCP (2) и антимицин А/ротенон (3). (B) Количествено определяне на базалното производство на OCR и ATP. (C) нива на mRNA на Pgc1a и Tfam във Veh-DC и Mito-DC, третирани със 100 ng/mL LPS или оставени нестимулирани за 24 часа. (D) Анализ на поточна цитометрия на MHCII, костимулиращи молекули (CD40/80/86) и експресия на PDL1 се определя със и без LPS стимулация. (E) ELISA на IL10, IL6 и TNF от Veh-DC и Mito-DC, третирани със 100 ng/mL LPS за 24 часа. (F–H) нива на mRNA на Tnfa, Il6 и Il10 във Veh-DC и Mito-DC, третирани със 100 ng/mL LPS или оставени нестимулирани за 24 часа. Данните представляват средни стойности ± SEM, * p По-малко или равно на 0,05, ** p По-малко или равно на 0,01 и *** p По-малко или равно на 0,001, еднопосочен ANOVA, последван от пост-теста на Tukey. Данните представляват средно ± SEM от три екземпляра.
Алогенен BMDC трансфер на Mito-DC защитаваБъбрециот исхемично увреждане Половин милион DC бяха инжектирани 1 ден преди двустраннобъбрекIRI за проучвания за алогенен трансфер на Mito-DC (BALB/C BMDC→C57BL/6 мишки). Схема на дизайна на изследването (Фигура 7A). Като контрола, мишките бяха инжектирани с 1x PBS като контроли без клетки (NC). В сравнение с мишките, третирани с Veh-DC, мишките, третирани с Mito-DC, значително защитаватбъбрециот нараняване (Фигура 7B). Морфологичните промени (Фигура 7C, D) са успоредни на функционалните изследвания. Мишките, третирани с Mito-DCs, имат по-нискибъбрекнива на иРНК на Kim1 [Veh-DC 0.04 ± 0.02 срещу Mito-DC 0.02 ± 0.01], Ngal [Veh-DC 0.57 ± 0.3 срещу Mito-DC 0.39 ± {{29} }.20] и Tnfa [Veh-DC 0,037 ± 0,02 срещу Mito-DC 0,0028 ± 0,0013] в сравнение с мишки, третирани с Veh-DC. При проучвания за алогенен трансфер, мишки, третирани с Mito-DC, имат намалена апоптоза TUNEL в сравнение с мишки, третирани с Veh-DC (Veh-DC 16,7 ± 8,2 спрямо Mito-DC 3,0 ± 1,2).

Дискусия В настоящото проучване демонстрирахме защита отбъбрекIRI, индуциран от адоптивен трансфер на третирани с рапамицин DC (еднократно или многократно), алтернативно регулира DC функцията, която зависи от относителните промени в динамиката на митохондриите. Както единичното, така и многократното(ите) лечение(я) с рапамицин индуцира намалени имуногенни (по-ниски цитокини и костимулиращи молекули) DC. Прехвърлянето на Rapa-M-DCs или Rapa-S-DCs защитавабъбрециот исхемично реперфузионно увреждане, което показва, че намаленото имуногенно състояние на модифицираните с рапамицин DC индуцира защитата. Освен това, прехвърлянето на Veh-DC, което има преходно увеличение на броя на митохондриите, също защитавабъбрециот IRI (Фигура 8A–D)). От тези проучвания можем да заключим, че инжектирането на по-малко имуногенни DC е централно за предизвикване на защита от IRI процес, който може да бъде постигнат чрез фармакологично лечение (рапамицин) или чрез трансфер на здрави екзогенни митохондрии. Както беше съобщено по-рано [31] и потвърдено в нашите проучвания на RNAseq, като цяло няма ясна толерогенна сигнатура, свързана с рапамицин-модулирани DCs. Въпреки че DCs на рапамицин показват някои значителни промени в гените след LPS стимулация в сравнение с DCs на носителя, те са ограничени до RapaM-DCs, имащи по-ниска цитокин-медиирана сигнализация и производство на цитокини (TNF-сигнализиране чрез NF-kB и производство на IFN), всички критични и в двете вродени и адаптивни имунни отговори. Както беше съобщено по-рано и потвърдено в нашето проучване, сигнализирането на IL-10 беше идентифицирано като основен път, който беше различен при третирани с рапамицин DCs с FDR от 5,87 × 10 4 (допълнителна материална фигура S1), отличителен цитокин на толерогенен подпис в DC.

Исторически погледнато, толерогенните DCs (Tol-DC) се идентифицират като нарушено съзряване или полунезрели с ниска експресия на костимулатор (CD80, CD86, CD40) с повишено производство на IL10, придружено от ниска секреция на IL12 и IFN , по-ниска способност за иницииране на Т клетки и потенциал за индуциране на Treg след провъзпалителна стимулация [32,33]. Регулаторните или толерогенни DCs могат да бъдат диференцирани in vitro чрез използване на имуносупресивни лекарства или съединения като FTY720 [18] или рапамицин (настоящото проучване), или противовъзпалителни цитокини като IL10 [34] или чрез генетична модификация.
Роля на дендритните клетки при остро бъбречно увреждане (ОПН)Въпреки че е постигнат голям фармакологичен напредък за превенция или лечение на различни наранявания, нито едно не е налично за AKI, поради което то остава като основна тежест за здравето [35]. Освен това, за предотвратяване или намаляване на адаптивни имунни отговори, медиирано отхвърляне на алографт или автоимунно заболяване, използването на неспецифични имуносупресивни лекарства е свързано с нежелани странични ефекти. По този начин използването на тип имунни клетки като DC, които могат да се насочат към вродени и адаптивни имунни отговори, е предимство. Освен това, DCs са важни клетки за имунитета или толерантността и идеята за използване на ex-vivo регулаторни или толерирани DCs в клетъчно-базирани терапии за рак, автоимунни заболявания и трансплантация е обект на проучване [36]. Фармакологични (FTY720 [18]) или биологични стратегии (генетично модифицирани) индуцират регулаторни или толерогенни DC (Tol-DC) [37], които са или устойчиви на съзряване, или имат по-ниски нива на зреене, или алтернативно се активират, което в крайна сметка експресира ниски нива на MHC I или MHC II и костимулиращи молекули като CD40, CD80 и CD86. Използвайки CD11c-DTR трансгенни мишки, преди това публикувахме проучвания, които демонстрираха, че изчерпването на DCs с дифтериен токсин значително защитава мишкатабъбрециот исхемично реперфузионно увреждане (IRI) [7,38] и обратното, дозозависимото увеличение на DC числата се влошаваувреждане на бъбреците[7], което предполага, че DC могат да играят основна роля в регулирането на AKI. Струва си да се спомене, че при AKI моделът на AKI, който се използва (химиотерапия, използваща цисплатин или исхемия), диктува ролята, която играят DC за промяна на имунологичните отговори. При AKI, индуцирана от цисплатин, DC аблация чрез използване на трансгенни мишки или чрез инжектиране на липозомен хлодронат води до повече наранявания, тъй като IL-10, произведен от DCs в този модел, в крайна сметка е необходим за намаляване на нефротоксичното увреждане [39,40].
Рапамицин: възпаление, имунни клетки, исхемично реперфузионно увреждане (IRI)По-рано публикувани проучвания демонстрират защитна роля на рапамицин при модели на AKI, използвайки IRI проучвания, които включват регулиране на инфифилтрацията на NKT клетките и функцията, като по този начин подобряватувреждане на бъбреците[41], в това проучване мишките са третирани перорално три пъти с рапамицин 24 часа, 1 час преди исхемия и 12 часа след исхемия. Хронично орално дозиране на мишки един ден преди товабъбрекIRI и всеки ден след това (до 7 дни) водят до по-високиувреждане на бъбрецитепоради инхибиране набъбречнатубулна клетъчна пролиферация на 1 и 3 дни след исхемия [42]. Това беше очевидно както при миши модел на едностранна уретерална обструкция (UUO), където лечението с рапамицин се подобрибъбрекфиброза чрез директно инхибиране на mTOR сигнализиране в миофибробласти и интерстициални макрофаги [43]. Тези проучвания показват, че рапамицин може да има противоположни ефекти при различни остри и хроничнибъбрекмодели. Различни проучвания обаче съобщават за вредна роля на рапамицин при животински модели на IRI. Пероралното дозиране на рапамицин (4 mg/ден) в продължение на 7 дни при йоркширски прасета увреди ендотелно-зависимата вазорелаксация и увеличи миокардната некроза в модел на оклузия на коронарната артерия [44]. Въпреки това, при мишки, остро лечение с рапамицин (един час преди исхемия, интраперитонеална инжекция) индуцира кардиопротекция чрез регулиране на JAK2-STAT3 сигнализиране за защита срещу миокарден инфаркт [45]. В зависимост от пътя (сонда, подкожно или интраперитонеално), дозиране (0.1–6 mg/kg/ден), време (рано или забавено) [46] и вида на използвания модел (сърце [47] , черен дроб [48] илибъбрек[41,49]), е доказано, че рапамицинът е защитен [47] или не е защитен [50].
Клетъчна терапия и рапамицинРазмножаването на миши BMDC или човешки CD14 плюс моноцити, които считаме за хронични, индуцира алтернативен защитен или регулаторен фенотип в DC, който регулира както вродените, така и адаптивните имунни отговори. При смъртоносна болест присадка срещу гостоприемник, DCs, генерирани с рапамицин, са намалили MHC II и костимулиращи молекули, но са имали по-висока популация от IL12, продуцираща след LPS стимулация. Тези продуциращи IL12 Rapa-M-DC усилват алореактивната Т-клетъчна апоптоза, механизъм, включващ IFN [51]. По подобен начин, CD14 плюс моноцити, размножени в присъствието на рапамицин, също произвеждат по-високи IL12p70 заедно с нивата на IL27, които регулират функцията на NK клетките, като по този начин променят алогенните Т клетъчни отговори чрез IFN [52]. вбъбрек,прехвърлянето на третираните с рапамицин Tregs има значително потиснати Т-клетъчни, миелоидни клетъчни и миофибробластни отговори, което води до подобрени остри и хроничнизаболяване на бъбрецитев сравнение с директното третиране на мишки с Rapamycin [53]. По подобен начин се подобрява адаптивният трансфер на третирани с рапамицин миелоидни супресорни клетки (MDSCs) в мишкибъбречна функцияс намалени хистологични увреждания и имунна клетъчна инфифилтрация [54]. Тези проучвания предоставят доказателства, че клетъчната терапия, която включва лечение на клетки с рапамицин преди инжектиране, избягва неблагоприятните странични ефекти, които могат да бъдат свързани със системното лечение с рапамицин. Освен това тествахме употребата на метформин или съединения като 5-аминоимидазол-4-карбоксамид-1- -4- рибофуранозид (AICAR) за индуциране на регулаторен фенотип в миши DCs, за да тестваме тяхната роля в промяната набъбрекIRI. Подобно на стратегията за дозиране, използвана с рапамицин (Rapa-S-DC), ние лекувахме BMDC с ниски дози метформин (1 mM) или AICAR (1 mM) на ден 7 заедно с LPS. Инжектирахме системно 0.5 x 106 метформин-DCs или AICAR-DCs един ден преди товабъбрекIRI. Мишки, третирани или с метформин-DCs, или с AICAR-DCs, са значително защитени в сравнение с мишки, третирани с NC или Veh-DCs (непубликувани наблюдения, Bajwa lab). По този начин, множество лекарства или съединения, които предизвикват метаболитни промени или активират AMPK пътя, може да си струва да бъдат тествани самостоятелно или в комбинация. Струва си да се отбележи, че използването на множество комбинации от лекарства или съединения (метформин или AICAR), които потенциално биха могли да допълнят защитните ефекти на рапамицин, все още не е проучено, когато се оценява тяхното използване в BMDCs. В раковите клетки, комбинирането на AICAR с рапамицин повишава ефикасността на рапамицин за допълнително потискане на mTORC2 за индуциране на апоптоза [55]. В Т-клетките комбинираното използване на метформин и рапамицин също е тествано като потенциален регулатор на метаболитен контролен пункт за повлияване на функцията на Т-клетките [56]. По този начин тези комбинирани терапевтични модалности трябва да бъдат тествани в бъдеще с толерогенни или регулаторни BMDCs като потенциални директни или индиректни регулатори на метаболитните контролни точки.

Рапамицин: Роля на митохондриите в дендритни клетки и макрофагиФункциите на DC и макрофагите се регулират от митохондриалния метаболизъм. Макрофаги тип 1 [57,58] и имуногенни DC (TLR-медиирано активиране) имат метаболитен преход, при който митохондриалното окислително фосфорилиране се инхибира от ендогенно синтезиран азотен оксид (NO) и ангажираност към високи аеробни гликолитични скорости [59]. Активирането на DC или макрофаги от няколко TLR агонисти (LPS или CpG) води до бързо повишаване на гликолизата, последвано от намаляване на OXPHOS и потенциала на митохондриалната мембрана [59–61]. Известна роля за митохондриите е демонстрирана с DCs, третирани in vitro с витамин D; тези DC са увеличили OXPHOS, митохондриалната маса и производството на mROS [62], нашето скорошно проучване, използващо FTY720 [18], показа подобни промени в DC (по-висок OXPHOS и по-малка имуногенност), е доказано, че острото лечение с рапамицин удължава клетъчния живот на DCs, които зависят от запазването на митохондриалната функция [10] чрез инхибиране на NO. Противно на увеличаването на продължителността на живота на DCs, същите групи също съобщават, че острата или кратка експозиция на рапамицин в DCs също ги прави мощни активатори на антиген специфични CD8 плюс Т клетки, като по този начин подобрява контрола на B16 меланома като ваксинация при мишки [63]. Острата обработка (90 минути) на DCs, получени от човешки моноцити, с рапамицин потиска LPS-индуцираните имуностимулиращи молекули и ало-стимулиращия потенциал, който включва неспособността на третираните DCS да увеличат NF-kB сигнализирането [64]. В макрофагите рапамицинът потиска производството на IL1 и IL-18след LPS стимулация, процес, който също така включва намаляване на митохондриалната ROS (mtROS) чрез директно инхибиране на NLRP3 inflammasome-p38 MAPK-NF-kB пътища [65]. кондиционираните с рапамицин DC (Rapa-DC) от мишки и хора се държат по различен начин в сравнение с миши Rapa-DC, човешките Rapa-DC са доказали, че са частично резистентни към съзряване след проинфламаторни цитокини и показват хетерогенност в регулирането на ефекторната Т-клетъчна експанзия и функция [66]. Голяма част от имунорегулаторните свойства на кондиционираните от рапамицин DCs, получени от моноцити, и тяхната роля в трансплантацията са елегантно прегледани от Macedo et al. [67].
Нашите настоящи открития показват, че единични или множество DCs, третирани с рапамицин, имат намален имуногенен и имуностимулиращ фенотип след LPS стимулация. Прехвърлянето на тези DC защитавабъбрециот IRI. Рапамицин алтернативно регулира динамиката на митохондриите; само многократното третиране предизвиква по-висок брой митохондрии. Тези данни предполагат, че митохондриалната динамика на DC (по-високо съдържание на митохондрии), заедно с по-малко имуногенен фенотип, индуциран от рапамицин, съвместно защитаватбъбрециот е химическо нараняване. Въпреки че е по-интересно, нашите данни с DCs, третирани с екзогенни митохондрии, показват, че по-високият брой митохондрии може да преодолее по-имуногенното състояние на DCs след LPS стимулация, за да защити същобъбрециот IRI. Ще бъде интересно да се потвърди дали по-високите числа на митохондриите в DC променят отговорите на Т клетките, DC имат способността да променят имунния отговор, както показа предишното ни проучване. Нашите предварителни данни показват, че в проучвания за алогенна Т-клетъчна пролиферация, DC с по-висок брой митохондрии наистина потискат CD4 Т-клетъчната пролиферация при смесени лимфоцитни реакции (MLR, данните не са показани). Понастоящем не е ясно дали DCs с по-високи митохондриални числа могат да индуцират Treg отговор, който може да допринесе положително за защитатабъбрециот IRI. Това ще бъде фокусът на следващите ни проучвания.
Изводи В обобщение, ние показахме, че BMDC могат да регулиратувреждане на бъбрецитечрез механизъм, който включва митохондриална биогенеза или чрез многократно третиране с рапамицин, или екзогенно увеличаване на броя на митохондриите чрез използване на екзогенни митохондрии. Ние заключаваме, че регулаторните DC (DC с по-висок брой митохондрии) могат да бъдат полезни прибъбрекIRI, както и при други възпалителни състояния като трансплантация и автоимунни заболявания за предотвратяване или лечение на нараняване.
