Характеризиране на кафеоилхиновите киселини от Lepisorus Thunbergianus и тяхната инхибиторна активност върху меланогенезата
Mar 29, 2022
Контакт: Audrey Hu Whatsapp/hp: 0086 13880143964 Имейл:audrey.hu@wecistanche.com
Hak Hyun Kim, Jae Kwon Kim, Jaehyun Kim, Se-Hui Jung* и Kooyeon Lee*
РЕЗЮМЕ:Хиперпигментацията в резултат на свръхактивирането на тирозиназата води до по-тъмни петна или петна по човешката кожа. Въпреки че тези явления са безвредни, все още има голямо търсене на инхибитори на меланогенезата за предотвратяване на хиперпигментация чрез инхибиране на тирозиназата, ензим, ограничаващ скоростта на меланогенезата. Въпреки че Lepisorus thunbergianus се използва в народните лекарства като диуретик и хемостатичен агент, ефектът му върху меланогенезата все още не е докладван. В това изследване ние приготвихме екстракт от L.thunbergianus и неговите фракции на разтворителя и оценихме тяхната биологична активност срещу синтеза на свободни радикали и меланин. Екстрактът от L. thunbergianus инхибира активността на тирозиназата на гъбите по-ефикасно от и с подобна антиоксидантна активност на арбутин in vitro. Сравнителна оценка на анти-меланогенезата и анти-тирозиназната активност на фракциите на разтворителя на L. thunbergianus демонстрира, че чрез инхибиране на тирозиназната активност бутаноловата фракция има най-висок потенциал за инхибиране на меланогенезата в меланомните клетки. Ние открихме чрез структурен анализ с помощта на високоефективна течна хроматография (HPLC) и NMR спектроскопия, че основните съединения в бутаноловата фракция са три производни на кафеоилхинова киселина. Трите производни имаха сходни действия за улавяне на радикали и анти-тирозиназа in vitro, докато само 5-кафеоилхинова киселина имаше инхибиторен ефект върху -MSH-индуцираната меланогенеза. Инхибиторният ефект на 5-кафеоилхинова киселина беше потвърден чрез определяне на съдържанието на меланин и активността на тирозина в меланома след третиране на клетките с търговско съединение. Освен това разкрихме, че 5-кафеоилхинова киселина инхибира меланогенезата чрез хелатиране на меден катион от комплекс мед-тирозиназа. По този начин, 5-кафеоилхинова киселина или фракция на бутанол, изолирана от L. thunbergianus, може да бъде полезна в козметиката като средство за избелване на кожата.
Cistanche tubulosa: средство за избелване на кожата.
ВЪВЕДЕНИЕ
Меланинът, група от естествени пигменти, намиращи се в повечето организми, играе важна роля в покафеняването на плодове, гъби и зеленчуци и пигментацията на човешката кожа.1 Меланини, произведени от аминокиселината тирозин чрез многоетапен процес, който включва ензимно окисление и полимеризация. 2 При хората меланиновият пигмент се синтезира от специализирани дендритни клетъчни меланоцити, разположени на кръстовището между епидермиса и дермата, в които синтезът се инициира чрез излагане на ултравиолетови (UV) лъчи.3 Меланиновият пигмент се транспортира до кератиноцитите, за да предпази кожата от UV лъчи и свободни радикали; по този начин цветът на кожата се определя от модела на разпределение на пигмента меланин.2 Нарушаването на регулацията на синтеза на меланин води до много форми на хиперпигментация, като мелазма, лунички, възрастови петна, слънчево лентиго, постинфламаторна хиперпигментация и други синдроми на хиперпигментация.4 Повече от стотици протеини са свързани със синтеза на томеланин и сред тях тирозиназата е ензимът, ограничаващ скоростта, който се признава за отговорен за синтеза на формеланин.5 По този начин повечето изследователски работи за предотвратяване на хиперпигментация са фокусирани върху идентифицирането, изолирането, синтеза и характеризирането на нови мощни тирозиназни инхибитори за превенция на меланогенезата. 1,6 Редица тирозиназни инхибитори, като коджикова киселина, арбутин, хидрохинон, азелаинова киселина, елагова киселина и транексамова киселина, са били широко използвани в козметичната индустрия като средства против меланогенеза; въпреки това, поради ограниченията на химическите лекарства, които включват цитотоксичност и странични ефекти, все още има търсене на нови материали с подобрена безопасност, стабилност и ефикасност.7
Естествените продукти, включително растения, бактерии и гъбички, са се превърнали в алтернативни източници за откриването на ефикасни съставки за избелване на кожата поради тяхната по-малка токсичност и по-добра биосъвместимост и бионаличност.1,8 Lepisorus thunbergianusis папрат, принадлежаща към Polypodiaceae, която расте прикрепена към стари скали или кората на дърветата и се разпространява в умерените региони на Източна Азия, като Корея, Япония, Китай, Филипините и Индокитай. L. thunbergianus е бил използван като диуретик, хемостатичен агент и е антитусивен в корейските народни лекарства. Предишни проучвания съобщават, че екстрактът от L. thunbergianus има локална антилипидна пероксидационна активност при локална и антиоксидантна активност.9 Освен това, екстрактите от L. thunbergianus показват значително инхибиране на растежа в зависимост от концентрацията при орален рак и рак на дебелото черво.10 Екстрактът от L. thunbergianus може да има потенциални приложения в козметичната индустрия, тъй като това растение съдържа различни флавоноидни съединения и множество биоактивни молекули, които включват кверцетин 3-метил етер-глюкозид, витексин, ориентал, периодичен глюкозид, изовитексин, ориентин, корентин и кафеоилхинова киселина.9a Въпреки това, ефектите на Екстрактът от L. thunbergianus върху синтеза на меланин в меланоцитите все още не е изяснен.

Фигура 1. Анализ на екстракт от L. thunbergianus за (A) отстраняване на ABTS радикали, (B) анти-тирозиназа и (C) вътреклетъчни активности на отстраняване на ROS
В това изследване ние приготвихме екстракта от L. thunbergianus и неговите разтворителни фракции чрез серийно фракциониране и изследвахме инхибиторните ефекти на разтворителните фракции върху биосинтезата на меланин в B16F10 меланомни клетки. Ние идентифицирахме фракцията на бутанол (n-BuOH) като основна част, съдържаща естествения инхибитор и допълнително характеризирахме ефектите на производните на кафеоилхинова киселина, изолирани от екстрактите на L. thunbergianus върху инхибирането на биосинтезата на меланин.
преглед на cistanche: антиоксидация
РЕЗУЛТАТИ И ДИСКУСИЯ
Етанолов екстракт от L. thunbergianus премахва 2,2′-азинобис(3-етил-бензотиазолин-6-сулфонова киселина (ABTS) радикал и инхибира тирозиназната активност.
Извличането на L. thunbergianus със 70 процента етанол (EtOH) беше извършено, за да се оцени потенциалната инхибиторна активност на естествените съединения в растението. Активността на екстракта от L.thunbergianus за отстраняване на радикали се определя в диапазон на концентрация от 2-200 ug/mL. Етаноловият екстракт показа зависима от концентрацията активност на извличане на радикали с максимален ефект при 50 ug/mL, при което резултатът беше в съответствие с този на арбутина, използван като положителна контрола (Фигура 1А).
Ние също така оценихме инхибиторния ефект на екстракта върху активността на тирозиназата на гъбите чрез измерване на скоростта на синтеза на допахром, катализирана от тирозиназа. Етанолектрактът инхибира 87 процента от активността на тирозиназата при 500 ug/mL, докато арбутинът инхибира само 38 процента от активността на тирозиназата при същата концентрация (Фигура 1B). След това оценихме активността на извличане на екстракта върху вътреклетъчната ROS, повишена със 100 μM водороден пероксид. Третирането с водороден пероксид предизвиква приблизително 21-кратно увеличение на вътреклетъчното ниво на ROS на B16F10 клетки (Фигура 1C). Ние открихме, че медиираното от водороден пероксид увеличение на вътреклетъчните ROS се поглъща от екстракта по дозозависим начин: максималната почистваща активност при 100 ug/mL е 78 процента (Фигура 1C). Тези резултати предполагат, че етаноловият екстракт от L. thunbergianus съдържа биоактивни съставки, които инхибират активността на тирозиназата, както и отстраняването на ABTS радикали и вътреклетъчни ROS.
екстракт от cistanche deserticola: инхибира активността на тирозиназата.
Инхибиторен потенциал на фракции на L. thunbergianus срещу меланогенеза.
A crude EtOH extract was fractionated with various solvents including hexane (Hex), methylene chloride (CH2Cl2), ethyl acetate (EtOAc), and butanol to identify and characterize ingredients inhibiting melanogenesis. To identify which solvent fractions have the potential against melanin synthesis, we performed a comparative analysis of four different L. thunbergianus solvent fractions for the radical scavenging and anti-tyrosinase activities. First, to evaluate the antioxidant activity of the four solvent fractions of the L. thunbergianus extract, we determined the ABTS radical scavenging activities in the concentration range of 2−200 μg/ mL. All fractions showed a concentration-dependent increase in ABTS radical scavenging activity (Figure 2A). In particular, EtOAc and n-BuOH fractions completely scavenged the ABTS radical at a 50 μg/mL concentration. The ABTS radical scavenging activity was in the order of n-BuOH > EtOAc >CH2Cl2 > Hex, което е в съответствие с предишния доклад. 10b Освен това, инхибиторните ефекти на различните фракции на разтворителя върху активността на тирозиназата се увеличават в зависимост от концентрацията: максималните инхибиторни активности на n-Hex и CH2Cl2 фракциите са под 65 процента, но тези на EtOAc и Фракциите на n-BuOH са над 70 процента (Фигура 2В). Инхибиторната активност е в порядъка на n-BuOH > EtOAc > CH2Cl2 > n-Hex. Тези резултати предполагат, че повече хидрофилни фракции, включително n-BuOH и EtOAc фракции, показват по-висока радикална активност и по-добра инхибиторна активност от липофилните n-Hex и CH2Cl2 фракции .
След това, ефектите на фракциите на разтворителя на L. thunbergianus върху пролиферацията на меланомни клетки бяха изследвани чрез третиране на B16F10 клетки с 200 ug/mL всяка от различните фракции или 2 mg/mL арбутин в наличие на -меланоцит-стимулиращ хормон (-MSH), за който е добре известно, че насърчава меланогенезата чрез индукция на транскрипционен фактор, свързан с микрофталмия (MITF). Резултатите показват, че нито една от фракциите няма значителен ефект върху пролиферацията на меланомни клетки (Фигура 2C). След това изследвахме инхибиторния ефект на фракциите на разтворителя върху меланогенезата, стимулирана от -MSH в меланомни клетки. Третирането с -MSH индуцира приблизително 20-кратно увеличение на вътреклетъчното съдържание на меланин на B16F10 клетки (Фигура 2D). Установихме, че -MSH медиираната меланогенеза е напълно инхибирана от n-BuOH фракцията (p <0,01) и="" частично="" инхибирана="" от="" etoacфракцията="" (40="" процента,="" p=""><0,01), докато="" -msh-медиираната="" меланогенеза="" не="" е="" значително="" променена="" от="" n-hex="" и="" ch2cl2="" фракции="" (фигура="" 2d).="" освен="" това="" бяха="" определени="" инхибиторните="" ефекти="" на="" фракциите="" на="" разтворителя="" върху="" тирозиназното="" активиране,="" медиирано="" от="" -msh,="" тъй="" като="" тирозиназата="" играе="" ключова="" роля="" в="" меланогенезата.="" n-buoh="" (95="" процента,="" р=""><0,001) и="" etoac="" (66="" процента,="" р=""><0,001) фракции="" обърнаха="" тирозиназно="" активиране,="" медиирано="" чрез="" -msh,="" докато="" фракциите="" n-hex="" и="" ch2cl2="" не,="" както="" е="" показано="" на="" фигура="" 2e.="" освен="" това,="" ефектът="" на="" почистване="" на="" различни="" фракции="" на="" разтворителя="" върху="" вътреклетъчното="" увеличение="" на="" ros="" се="" стимулира="" от="" водороден="" пероксид.="" всички="" фракции="" на="" разтворителя="" обръщат="" вътреклетъчното="" увеличение="" на="" ros,="" медиирано="" от="" водороден="" пероксид,="" както="" е="" показано="" на="" фигура="" 2f.="" тези="" резултати="" показват,="" че="" buoh="" фракцията="" на="" l.="" thunbergianus="" инхибира="" -msh-индуцирана="" меланинсинтеза="" чрез="" инхибиране="" на="" вътреклетъчната="" тирозиназна="" активност="" в="" b16f10="" клетки.="" освен="" това,="" тези="" резултати="" предполагат,="" че="" биоактивните="" съставки,="" инхибиращи="" синтеза="" на="" меланин,="" са="" хидрофилни="" и="" се="" намират="" главно="" във="" фракцията="" на="">

Фигура 2. Ефекти на фракциите на разтворителя върху ABTS радикално отстраняване, антитирозиназни и антимеланогенезни дейности.
Идентифициране и характеризиране на биоактивни съединения на екстракт от L. thunbergianus.
За идентифициране и характеризиране на съставките, инхибиращи меланогенезата, беше извършен анализ с високоефективна течна хроматография (HPLC) за фракции с всички разтворители. HPLC анализът на фракциите на разтворителя разкри, че всички фракции съдържат три основни съединения при времена на задържане от 21, 28 и 29 минути съответно за съединения 1, 2 и 3 (Фигура 3A-D). Тези три основни съединения бяха допълнително изолирани чрез препаративно HPLC пречистване. Количествата на трите основни съединения във фракцията n-BuOH са определени с помощта на търговски производни на кафеоилхинова киселина като вътрешни стандартни молекули, съгласно предишния доклад.12
След това изолираните съединения бяха идентифицирани чрез сравнение на техните 1H и 13C NMR данни с литературата и беше установено, че са в съответствие с предложените структури (Фигура 4).13 Фигура 3E показва молекулната структура на трите съединения. Съединение 1 (добив, 3.2 ± 0.1 mg/100 mg n BuOH фракция) се получава като бледожълт прах. 'HNMR (400 MHz, DMSO-d6) 5 9.66 (1H, brs), 9.20 (1H, brs), 7.49 (1H, d, J=15.9 Hz), 7.04 (1H, s), 6.99 ( 1H, d, J=8.2Hz), 6.78 (1H, d, J=8.1 Hz), 6.23 (1H, d, J=15.9 Hz), 5.20( 1H, m), 5.08 (1H, brs), 4.89 (1H, brs) 4.13 (1H, m), 3.84 (1H, m), 3.56 (1H, s), 3.35 (1H, s), 1.99 (1H, m), 1.92 (1H,m), 1.89 (1H,m), 1.79 (1H,m). 13C{1H} NMR (100 MHz, DMSO-d6) 5 (176.42, 168.10, 148.14, 145.53, 144.75, 125.65, 121.07, 115.75, 114.71, 114.22, 72.88, 71.01, 369.85, 359.85, Съединение 1 беше идентифицирано като 3-кафеоилхинова киселина чрез NMR анализ и чрез сравнение с предишната литература.13b
Съединение 2 (добив, 14.1 ± 0.1 mg/100 mg n-BuOH фракция) се получава като бледожълт прах. 'Н NMR (400 MHz, DMSO-d6) 5 9.64 (1Н, brs), 9.20 (1Н, brs), 7.52 (1Н, d, J=15.9 Hz), 7.06 (1Н, s), 7.02 ( 1H, d, J=8.1 Hz) 6.79 (1H, d, J=7.9 Hz), 6.30 (1H, d, J=15.9 Hz), 4.85 ( 1H, brs), 4.70 (1H, d, J=4.9 Hz), 4.12 (1H, brs), 3.95 (1H, m), 1.97 (2H, m), 1.88 (1H, m), 1,83 (1Н, т). 13C{1H} NMR (100 MHz, DMSO-d6) 5 (176.02, 166.27, 148.28, 145.55, 144.77, 125.54, 121.19, 115.76, 114.68, 114.57, 76.66, 73.92, 348.52, 648.57, Съединение 2 беше идентифицирано като 5-кафеоилхинова киселина чрез NMR анализ и чрез сравнение с предишната литература. 13c
Съединение 3 (добив, 3.9 ± 0.2 mg/100 mg n-BuOH фракция) се получава като бледожълт прах. 'Н NMR (400 MHz, DMSO-d6) 5 9.64 (1Н, brs), 9.20 (1Н, brs), 7.52 (1Н, d, J=15.9 Hz), 7.06 (1Н, s), 7.02 ( 1H, d, J=8.1 Hz) 6.79 (1H, d, J=7.9 Hz), 6.30 (1H, d, J=15.9 Hz), 4.85 ( 1H, brs), 4.70 (1H, d, J=4.9 Hz), 4.12 (1H, brs), 3.95 (1H, m), 1.97 (2H, m), 1.88 (1H, m), 1,83 (1Н, т). 13C{1H} NMR (100 MHz, DMSO-d6) 5 (176.02, 166.27, 148.28, 145.55, 144.77, 125.54, 121.19, 115.76, 114.68, 114.57, 76.66, 73.92, 348.52, 648.57, Съединение 3 беше идентифицирано като 4-кафеоилхинова киселина чрез NMR анализ и чрез сравнение с предишната литература.13a

Фигура 3. HPLC хроматограми на (A) n-Hex, (B) CH2Cl2, (C) EtOAc и (D) n-BuOH фракции на L. thunbergianus и (E) структура на трите основни съединения.
Инхибиторен потенциал на производни на кафеоилхинова киселина, изолирани от L. thunbergianus срещу меланогенеза.
След това, за да идентифицираме биологично активната съставка, лежаща в основата на мощната антимеланогенеза, ние определихме инхибиторната активност на трите производни на кафеоилхинова киселина, изолирани от L. thunbergianus срещу синтеза на меланин в меланомни клетки. Първо, бяха изследвани ефектите на трите производни върху отстраняването на радикали от ABTS. Резултатите показват, че трите производни имат сходни ABTS дейности по отстраняване на радикали (Фигура 5А). След това изследвахме инхибиторния ефект на трите производни, изолирани от онтирозиназната активност на L. thunbergianus. Трите производни показаха зависимо от концентрацията инхибиране на активността на тирозиназата, с максимално инхибиране при концентрация от 200 μM (Фигура 5B). Освен това, ние изследвахме инхибиторния ефект на трите производни върху -MSH-индуцираната синтеза на меланин в B16F10 клетки. Третирането с -MSH индуцира приблизително 2{11}}кратно увеличение на вътреклетъчното съдържание на меланин в клетките B16F10 (Фигура 5C). Интересното е, че съединения 1 (3-caffeoylquinicacid) и 3 (4-caffeoylquinic acid) значително повишават синтеза на меланин съответно с 25 и 23 процента (Фигура 5C, p< 0.001),="" while="" compound="" 2="" (5-caffeoylquinic="" acid)="" completely="" reversed="" α-msh-induced="" melanogenesis="" (p="" <="" 0.001).="" these="" results="" suggest="" that="" the="" three="" caffeoylquinic="" acid="" derivatives="" with="" similar="" structures="" but="" different="" substitution="" sites="" have="" different="" biological="" activities="" on="" melanogenesis.="" furthermore,="" 5-caffeoylquinic="" acid="" has="" potent="" inhibitory="" activity="" against="">
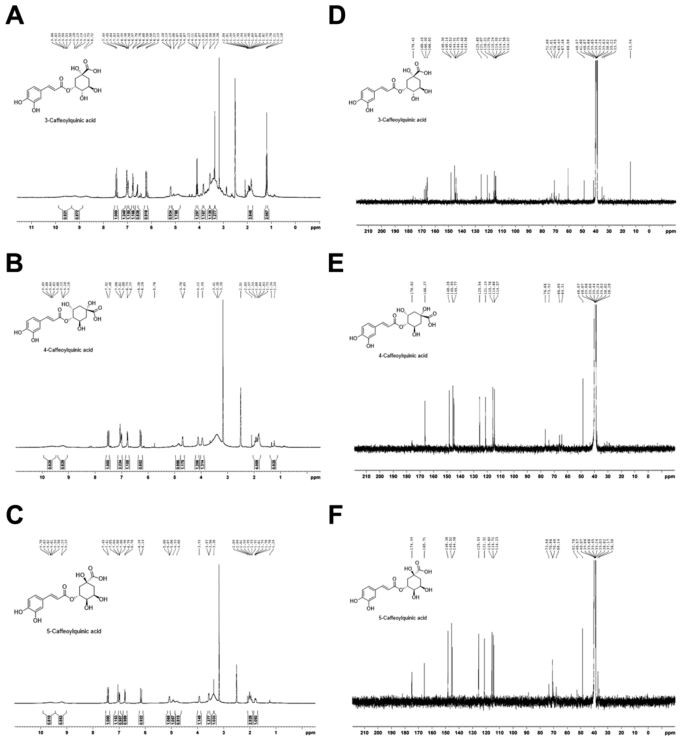
Фигура 4. 1Н NMR спектри на (A) 3-кафеоилхинова киселина, (B) 4-кафеоилхининова киселина и (C) 5-кафеоилхининова киселина и 13C NMR спектри на (D) {{ 6}}кафеоилхинова киселина, (E) 4-кафеоилхининова киселина и (F) 5-кафеоилхининова киселина
Проверка на антимеланогенезната ефикасност на 5-кафеоилхинова киселина.
За да проверим инхибиторния ефект на {{0}}кафеоилхинова киселина срещу меланогенезата, ние определихме инхибиторния ефект на търговската 5-кафеоилхининова киселина върху синтеза на меланин, медииран от -MSH. Третирането с по-ниски концентрации от 0.1 и 0.2 mM 5-caffeoylquinicacid леко повишава синтеза на меланин и вътреклетъчната тирозиназна активност, докато по-високите концентрации от 0,5 и 1 mm от съединението обръщат -MSH-медиираната меланогенеза и вътреклетъчна тирозиназна активност (Фигура 6A, B), при което резултатите са в съответствие с предишния доклад.14
Кафеоилхинова киселина е фенолно съединение, образувано от теестерна връзка между кафеена киселина и L-хининова киселина. Известно е, че производните на кафеоилхинова киселина имат анти-меланогенезни и анти-тирозиназни активности, както и ROS изчистваща активност. Тирозиназата е многофункционален съдържащ мед метален ензим с двувалентни медни катиони.1 Производните на кафеоилхинова киселина могат да инхибират активността на тирозиназата чрез хелатиране на меден катион, отговорен за поддържане на активното състояние на тирозиназата. За да се предвиди взаимодействието между 5-кафеоилхинова киселина и тирозиназа, беше извършено изчислително молекулярно докинг изследване с помощта на Maestroprogram. Най-добрата поза за съединението, докингирана тотирозиназа, е изобразена на Фигура 6C, D. Изследването за молекулярно докинг разкри, че 5-кафеоилхинова киселина взаимодейства с меден ион на разстояние 2,43 Å и установява серия от π−π подреждане с His 259, Asn 260, His 85 и His 263 остатъци и Н-връзка с Arg 268. Освен това, енергията на свързване между тирозиназата и 5-кафеоилхинова киселина беше −4,425 kJ/mol. Тези резултати показват, че 5-кафеоилхинова киселина може да инхибира активността на тирозиназата чрез медно хелиране. За да проверим инхибиторния механизъм на меланогенезата от 5-caffeoylquinicad, ние определихме способността за хелатиране на медта на 5-caffeoylquinic acid. Способността за хелатиране на мед на 5-кафеоилхинова киселина се повишава в зависимост от концентрацията (Фигура 6E). Този резултат предполага, че 5-caffeoylquinicacid инхибира синтеза на меланин чрез хелатиране на меден катион, взаимодействащ с тирозиназа.

Фигура 5. Ефекти на трите производни на кафеоилхинова киселина върху отстраняването на радикалите, in vitro анти-тирозиназната и анти-меланогенезната активност в B16F10 клетки.
МАТЕРИАЛИ И МЕТОДИ
Материали
L. thunbergianus е закупен от онлайн пазара www.jirisangol.com (Корея) и е изсушен при атмосферни условия преди употреба в това изследване. Реагенти, като 2,2′-цинк бис(3-етил-бензотиазолин-6-сулфонова киселина (ABTS) и 3-(4,5-диметилтиазол-2- yl)-2,5-дифенилтетразолиев бромид (MTT), -меланоцит-стимулиращ хормон (-MSH), и ензими, като тирозиназа от гъби, са получени от Sigma-Aldrich (Сейнт Луис, Мисури, САЩ).Калиевперсулфат (K2S2O8), пирокатехол виолет и 3,4-дихидрокси-L фенилаланин (L-DOPA) са закупени от Alfa Aesar (Haverhill, MA, USA).
Екстракция и фракциониране на L. thunbergianus.
Изсушен L. thunbergianus (80 g) се пулверизира с помощта на пулверизатор (HBL-3500S, Samyang Electronics, Корея) и се екстрахира със 70 процента EtOH три пъти (800 mL, всеки път ) при 70 градуса за 3 дни. Полученият екстракт се филтрира под вакуум с помощта на хартия Advantecfilter no. 1 и 2 (Toyo Roshi Kaisha, Ltd., Токио, Япония) и се концентрират с помощта на ротационен изпарител Hei-Vap Advantage (Heidolph, Германия), за да се получат 17,2 g от EtOH суровия екстракт. Този суров екстракт се суспендира в dH2O (180 mL) и последователно се фракционира с Hex, CH2Cl2, EtOAc и n-BuOH, за да се получи Hex (1,51 g, 8,8 процента), CH2Cl2 (0,88 g, 5,1 процента), EtOAc (3,95 g, 23,0 процента). %), и n-BuOH (3,02 g, 17,6 процента), както е описано по-рано.15 Получените екстракти и фракции се сушат чрез замразяване и се съхраняват при -80 градуса преди употреба.
Определяне на активността на ABTS за отстраняване на свободни радикали.
За да се оцени антиоксидантната активност на екстрактите от L.thunbergianus и неговите фракции на разтворителя, беше определена активността за отстраняване на ABTSрадикали, както беше описано по-горе.16 За генериране на ABTS радикала, 10 mL от 7 mMABTS беше смесен със 176 μL от 140 mM калиев перокси дисулфат в dH2O и се инкубира на тъмно при стайна температура (RT) в продължение на 16 часа преди употреба. Разтворът на ABTS радикала се разрежда с абсолютен метанол, за да се получи анаабсорбция от близо 0,7 при 734 nm. Аликвоти от 100 μL от всеки екстракт или фракции в посочения диапазон на концентрация от 2-200 ug/mL се добавят към 100 μL от разредения разтвор на ABTS радикали и се инкубират за 10 минути на тъмно при RT. След това абсорбцията беше измерена при 732 nm с помощта на многомодов четец на микроплаки SpectraMaxM5 (Molecular Devices, Sunnyvale, CA, USA). Активността на ABTS отстраняване на радикали се изчислява, както следва
ABTS радикална активност (проценти) =1−(като проба/контрола)×100 (1)
Ин витро инхибиране на тирозиназа.
Инхибиторният ефект на екстрактите от L.thunbergianus и неговите фракции на разтворителя върху активността на тирозиназата беше оценен чрез количеството допахром, синтезирано от каталитичната реакция на тирозиназа. 2a, 17 Накратко, 50 μL от всеки екстракт или фракция в посочения диапазон на концентрация се смесват с 50 μL от 50 U/mL гъбена тирозиназа в 50 mM фосфатно буфериран физиологичен разтвор (PBS; 8,1 mM Na2HPO4, 1,2 mM KH2PO4, pH 6,8, 2,7 mMKCl и 138 mM NaCl) в 96-ямкова плака и се инкубира за 30 минути при RT. След това се добавят 100 μL от 1 mM L-DOPA към всяка ямка, последвано от инкубиране за допълнителни 10 минути при 37 градуса. Абсорбцията на получения разтвор се измерва при 475 nm с помощта на многомодов микроплатерен четец SpectraMax M5.
Клетъчна култура.
Миши меланомни клетки B16F10 се култивират в модифицирана на Dulbecco среда на Eagle (DMEM) (Gibco, Gaithersburg, USA), допълнена с 10 процента инактивиран от топлина фетален говежди серум (Gibco), 100 единици/mL пеницилин и 100 ug/mL стрептомицин (Gibco) при 37 градуса под овлажнен 5 процента CO2.
Клетъчна жизнеспособност.
Жизнеспособността на B16F10 клетките се определя с помощта на МТТ анализ, както е описано по-горе.18 Накратко, B16F10 клетките се посяват в 24-плаки с ямки при плътност от 1 × 104 клетки на ямка. След 24 часа клетките бяха третирани с посочените концентрации на екстракти или фракции от L. thunbergianus за 48 часа. След това клетките бяха инкубирани с МТТ разтвор за 4 часа и редуцираните формазанови кристали бяха разтворени в DMSO. Полученият разтвор се прехвърля в 96-плаки с гнезда и абсорбцията се измерва при 540 nm с помощта на многомодов четец на микроплаки SpectraMax M5.
Определяне на вътреклетъчни реактивни кислородни видове (ROS).
Вътреклетъчното ниво на ROS се измерва, като се използва DCF/H2DCFDA клетъчен комплект за анализ на ROS (ab113851, Abcam), съгласно инструкциите на производителя. Накратко, B16F10 клетки бяха посяти в 48-плаки с ямки при плътност от 2 × 104 клетки на ямка. След 24-часово култивиране, клетките бяха третирани в продължение на 1 час с посочените концентрации на екстракти от L. thunbergianus или фракции на разтворителя в 0,1 процента говежди серумен албумин (BSA), съдържащ културална среда без фенолно червено. След това клетките се инкубират със 100 μM водороден пероксид за 30 минути. След промиване с PBS, клетките се третират с 25 μMH2DCFDA в PBS за 45 минути. Нивото на ROS се анализира от четец на микроплаки (Synergy H1, Biotek, Vermont, USA), оборудван с флуоресцентен филтър при 485/545 nm (дължина на вълната на възбуждане/емисия). Средният относителен интензитет на флуоресценция на контролата беше приравнен към 100 процента, като условията на лечение бяха изчислени пропорционално.
Определяне на съдържанието на меланин.
Съдържанието на меланин се определя, както е описано по-горе, с някои модификации.19 Клетките на меланома се култивират в плака с шест ямки за 24 часа. Те бяха третирани с посочените концентрации на екстракт от L. thunbergianus или негови фракции от разтворител за още 48 часа в присъствието на 100 nM -MSH. След два пъти промиване с охладен фосфатно буфериран физиологичен разтвор на Dulbecco, допълнен с калциев хлорид и магнезиев хлорид (D-PBS, Gibco), получените клетки бяха отделени чрез инкубиране с разтвор на трипсин-EDTA. След центрофугиране при 1000 rpm за 3 минути, клетъчната пелета се разтваря в 150 μL 1 М NaOH, съдържащ 10 процента DMSO за 1 час при 60 градуса за 1 час. Съдържанието на меланин се определя чрез абсорбцията при 405 nm, като се използва четец на микроплаки.

Екстрактът от цистанче инхибира меланина.
Определяне на активността на клетъчната тирозиназа в меланомни клетки.
Тирозиназната активност в B16F10 клетки беше изследвана на базата на количеството допахром, произведен от каталитичната реакция на вътреклетъчната тирозиназа.20 Накратко, меланомните клетки бяха култивирани в шестямкова плака за 24 часа, последвано от третиране с различни концентрации на екстракт от L.thunbergianus или негов разтворител фракции за още 48 ин в присъствието на 100 nM -MSH. След двукратно промиване с леденостуден D-PBS, клетките се лизират в 200 μL буфер за радиоимунопреципитационен анализ (RIPA) (Sigma-Aldrich), съдържащ протеазни и фосфатазни инхибитори. След центрофугиране на клетъчния лизат, събран от всяка ямка при 15, 000 g за 15 минути, 100 μL от супернатантата се смесват със 100 μL 1 mM L-DOPA в PBS (рН 6,8), последвано от инкубиране за 30 минути при 37 градуса . Абсорбцията на допахром се измерва при 475 nm с помощта на четеца на микроплаки. Данните се нормализират с протеинова концентрация, определена чрез анализ на бицинхонинова киселина.
Изолиране и характеризиране на биоактивни съединения с помощта на HPLC.
HPLC се извършва на YL{{0}}(Young Lin Instrument, Корея), оборудван с колона TC-C18 (4,6 mm, 250 mm и 5 μm, Agilent, САЩ), в конюнкция с градиентна система, съставена от разтворител А (0.2 процента мравчена киселина) и разтворител В (МеОН). Наклонът на съотношението на разтворителя беше зададен на 0-5 min, 15 процента B; 5−10 min, 15−20 процента B; 10-15 минути, 20-30 процента B; 15-30 минути, 30-40 процента B; 30-37 минути, 40-60 процента B; 37-40 минути, 60-100 процента B; 40-45 минути, 100 процента B; 45−50 минути, 100−15 процента B; и 50-55 min, 15 процента B. За да се идентифицират съставките във фракциите на разтворителя, подвижната фаза се доставя при скорост на потока от 1 mL/min и откриването на елуиране се извършва при 330 nm. За да се съберат неразтворимите фракции на биоактивните съставки, подвижната фаза се доставя при скорост на потока от 15,0 mL/min и откриването на елуиране се извършва при 330 nm с помощта на подготвителна HPLC (YL-9100 s, Young Lin Instrument, Корея ), оборудвана с колона prep-C18 (4,6 mm, 212 mm, 10 μm, Agilent, САЩ), във връзка с градиентна система, съставена от разтворител A (0,2 процента мравчена киселина) и разтворител B (MeOH). Съотношението на наклона на разтворителя беше зададено на 0-10 минути, 10 процента B; 10-20 минути, 10-15 процента B; 20-40 минути, 15 процента B; 40-60 минути, 15-20 процента B; и 60-70 минути, 30 процента B.
Молекулярно моделиране.
Кристалната структура на гъбната тирозиназа за молекулярно моделиране е агарикустирозиназа (PDB: 2Y9X), получена от Protein DataBank (PDB). Ензимът беше приготвен чрез използване на работния поток за подготовка на proteinwizard, вграден в Maestroprogram (Maestro, версия 11.9.011, Schrödinger, LLC, NewYork, NY, USA, 2019). Водата и всички други молекули, присъстващи в PDB файловете, бяха премахнати. Молекулярното докинг беше извършено с помощта на протокола за индуцирано прилягане (IFD) (Schrödinger Suite 2019 Induced Fit Docking protocol), както беше докладвано по-рано.21
Способност за хелатиране на мед.
Способността за хелатиране на медта на съединенията, изолирани от L. thunbergianus, е определена съгласно предишния доклад.22 Всяко производно на кафеоилхинова киселина (10 μL) в посочената концентрация се смесва с 280 μL 50 mM натриев ацетатен буфер (рН 6,0), 6 μL от 4 mM разтвор на пирокатехол виолетов, приготвен в същия буфер, и 10 μL от 1 ug/μL CuSO4·5H2O. Изчезването на синия цвят се наблюдава чрез измерване на абсорбцията при 632 nm, като се използва многомодов четец на микроплаки SpectraMax M5. Водата се използва като контрола вместо проба. Процентът мед хелатна активност се изчислява от абсорбцията при 632 nm, която е както следва
способност за хелатиране на мед (проценти)=1− (Проба/контрола)×100 (2)
Статистически анализ.
Всички данни в това изследване са изразени като средно ± стандартно отклонение (SD) от три независими експеримента. Статистическите анализи бяха извършени с помощта на GraphPad Prism 8.0 (GraphPad Software Inc., La Jolla, Калифорния, САЩ). Разликите между средните стойности на контролната и експонираната групи бяха анализирани с помощта на еднопосочен анализ на дисперсията (ANOVA), последван от post hoctest на Dunnett. Прагът за статистическа значимост за всички анализи беше p < 0.05="">
ИЗВОДИ
В това проучване ние демонстрирахме, че екстрактът от L. thunbergianus извлича ABTS радикалите и проявява мощен инхибиторен ефект върху биосинтезата на меланин без значителна цитотоксичност. Небиоактивна съставка, съществуваща в L. thunbergianus и инхибираща меланогенезата, беше изолирана във фракцията на n-BuOH. Освен това открихме, че трите производни на кафеоилхинова киселина са основни съединения, които съществуват във фракцията на n-BuOH и че 5-кафеоилхиновата киселина е важна съставка за потискане на меланогенезата в клетките на меланома чрез инхибиране на активността на клетъчната тирозиназа. Тук изолирахме инхибитора на естественото съединение 5-кафеоилхинова киселина от екстракта на L.thunbergianus за предотвратяване на хиперпигментация и разкрихме неговия инхибиращ механизъм, който е в основата на меланогенезата. По този начин, нашите открития предполагат, че 5-кафеоилхинова киселина и n-BuOH фракцията, изолирана от L. thunbergianus, може да са полезни в козметиката като агенти за избелване на кожата.
филийки цистанче



