Изчерпателен анализ на регулатори на пироптоза и туморна имунна микросреда при светлоклетъчен бъбречноклетъчен карцином
May 23, 2022
За повече информация. контактtina.xiang@wecistanche.com
Резюме
Заден план: Все повече доказателства сочат, че пироптозата може да регулиратуморна имунна микросреда(TIME), за да повлияе на развитието на тумора. Като силно имуногенен тумор, светлоклетъчният бъбречноклетъчен карцином (ccRCC) може да се възползва от имунотерапията, но свързаните с него изследвания върху пироптозата във ВРЕМЕТО на ccRCC все още са недостатъчни.
Методи: Наличните данни, получени от бази данни TCGA и GEO, бяха анализирани, за да се идентифицират различните профили на експресия на пироптоза в ccRCC и нормални тъкани, и корелацията на регулаторите на пироптоза с TIME беше оценена в cCRCC.
Резултати: Съгласно консенсусния клъстерен анализ, две диференциални нива на експресия на подтипове бяха идентифицирани, за да повлияят на прогнозата на пациента и бяха свързани със стадия и степента на хистологичния тумор. Имунните клетки се изчисляват чрез алгоритъма CIBERSORT. По-високи инфилтрирани нива на наивни В клетки, Т клетки CD4 памет в покой, NK клетки в покой, моноцити и макрофаги бяха наблюдавани в Клъстер 1, докато по-високи инфилтрирани нива на CD8 плюс Т клетки, Т фоликуларни помощни клетки и Tregs бяха наблюдавани в Клъстер 2 Анализът на обогатяване на набор от гени показва, че клъстер 2 е обогатен с множество имуно-свързани пътища, включително JAK-STAT сигнален път. Освен това, свръхекспресията на осем имунни контролни точки е свързана с развитието на ccRCC, особено в клъстер 2. Като четири потенциално ключови регулатора на пироптоза, AIM2, CASP5, NOD2 и GZMB беше потвърдено, че са регулирани нагоре в ccRCC чрез RT-qPCR анализ и допълнително проверени от HPA база данни. Допълнителен анализ на панрак предполага, че тези четири регулатора на пироптоза са диференциално експресирани и свързани с ВРЕМЕТО при множество видове рак.
Заключение: Настоящото проучване предостави цялостен поглед върху регулаторите на пироптоза във ВРЕМЕТО на ccRCC, което може да осигури потенциална стойност за имунотерапията.
Ключови думи: светлоклетъчен бъбречноклетъчен карцином, пироптоза, туморна имунна микросреда, имунни контролни точки, имунотерапия

Кликнете, за да научите, че herba cistanches лекува бъбречната функция
Заден план
Бъбречноклетъчен карцином(RCC) е най-честият злокачествен солиден тумор на бъбрека при възрастни, представляващ приблизително 3 процента от всички злокачествени заболявания при възрастни и 90 процента от злокачествените бъбречни заболявания[1]. Понастоящем броят на смъртните случаи, дължащи се на RCC всяка година в световен мащаб, е надхвърлил 1,00,000, а нивата на заболеваемост и смъртност нарастват със скорост от 2-3 процента на всеки 10 години [2]. Според версията от 2004 г. на патологичната класификация на RCC на СЗО, честотата на ясноклетъчен бъбречноклетъчен карцином (ccRCC) е приблизително 70 процента [3]. Въпреки че хирургичната резекция все още е най-доброто лечение за ccRCC, понастоящем няма ефективно постоперативно адювантно лечение и ccRCC не е чувствителен към лъчетерапия и химиотерапия. Според литературата, 20-40 процента от пациентите получават рецидив след операция [4]. Като силно имуногенен тумор, ccRCC може да се възползва от имунотерапията.
Пироптозата е вид програмирана клетъчна смърт, придружена отвъзпалениепредизвикани от инфекция с патогенни микроорганизми или други вредни сигнали [5]. Пироптозата се характеризира главно с клетъчно подуване, лизис и освобождаване на цитоплазмено съдържание. Подходящата пироптоза е важен механизъм за приемника да устои на инфекция от чужди патогенни микроорганизми. Прекомерната пироптоза обаче е вредна или дори фатална за гостоприемника. Все повече проучвания показват, че пироптозата също играе важна роля в развитието на тумори [6]. Пироптозата създава среда, инхибираща тумора, чрез освобождаване на възпалителни фактори. Въпреки това, пироптозата може също да отслаби имунната функция на тялото срещу туморните клетки и да ускори растежа на тумори при различни видове рак. Някои проучвания показват, че ефективният провъзпалителен ефект на пироптозата е свързан с регулирането на туморната имунна микросреда [7]. Тези открития предполагат, че пироптозата играе важна роля в развитието на тумора и антитуморния процес. Ефектът на пироптозата върху прогнозата на ccRCC обаче е неясен. Все още липсва цялостно разбиране на пироптозата в ccRCC, включително кръстосаното взаимодействие между регулаторите на пироптоза и туморната имунна микросреда.
В настоящото проучване извършихме цялостен ретроспективен анализ, базиран на базата данни на Атласа на генома на рака (TCGA) и Омнибусната база данни на генната експресия (GEO), за да оценим влиянието на пироптозата върху TIME и допълнително проучихме основните механизми между пироптозата и индивидуалното TIME характеристики, базирани на консенсусния клъстерен анализ. В допълнение, настоящото проучване също потвърди връзката между пироптозата и експресията на имунната гореща контролна точка.
Материали и методи
Събиране на данни и идентифициране на диференциално изразяване
Данните за секвениране на РНК (RNA-seq) на 539 ccRCC тъкани и 72 нормалнибъбректъкани, както и съответните клинични характеристики от базата данни на TCGA (https://portal.gdc.cancer.gov/). Данните GSE46699 и GSE53757 от базата данни GEO (https://www.ncbi.nlm.nih.gov/geo/) бяха събрани и използвани за оценка на експресията на регулатора на пироптоза. Освен това, данни за експресия на ген за пан-рак на TCGA за 33 вида злокачествени тумори и съответната клинична информация, като резултати за стволовост, базирани на иРНК (RNAss) и ДНК-метилиране (DNAss), както и имунни подтипове, са получени от университета Калифорния Санта Круз база данни (UCSC Xena, http://xena.ucsc.edu/). 37-те регулатора на пироптозата са представени в Допълнителен файл 4: Таблица S1 и са извлечени от предишни изследвания [8, 9]. Чрез използване на пакета "limma", повече от двукратни промени и процент на фалшиви открития (FDR, коригирана p-стойност)<0.05 is="" considered="" differential="" gene="" expression.="" the="" immunohistochemistry="" (ihc)="" staining="" images="" of="" pyroptosis="" regulators="" in="" normal="" kidney="" and="" tumor="" tissues="" were="" analyzed="" and="" obtained="" from="" the="" hpa="" database="" (http://www.proteinatlas.org/).to="" compare="" the="" expression="" between="" normal="" and="" tumor="" samples,="" all="" tissues="" were="" selected="" using="" the="" same="">
Консенсусно групиране
Унивариантният регресионен анализ на Кокс беше използван за извличане на регулатори на пироптоза чрез р-стойността на R пакета "оцеляване"<0.05). consensus="" clustering="" was="" performed="" to="" explore="" the="" potential="" molecular="" subtype="" between="" the="" bca="" patients="" using="" the="" r="" package"consensus="" cluster="" plus".="" the="" cluster="" count="" (k)="" was="" set="" from="" 1="" to="" 9,="" and="" the="" best="" optimal="" k="" value="" was="" selected="" for="" further="">
Оценка на туморната имунна микросреда
CIBERSORT, инструмент за анализ, базиран на сигнатурата на имунния ген LM22, беше използван за оценка на нивата на туморна имунна инфилтрация на ccRCC. Алгоритъмът беше изпълнен за 1000 пермутации и ccRCC проби с изход P<0.05 were="" selected="" for="" further="" analysis.="" the="" "estimate"="" package="" in="" r="" was="" used="" to="" evaluate="" the="" immune="" score="" and="" the="" stromal="" score.="" moreover,="" 8="" com-mon="" immune="" checkpoint="" genes,="" including="" pd-1,="" pd-l1,="" pd-l2,="" ctla4,="" siglec15,="" tigit,="" tim3,="" and="" lad3,="" were="" extracted="" and="" evaluated="" for="" their="" correlations="" with="" pyroptosis="" regulators="" in="">
Анализ на функционалното обогатяване
Анализът на генната онтология (GO) и анализът на сигналния път на Киото Енциклопедия на гените и геномите (KEGG) бяха извършени с помощта на пакета "cluster Profiler" в R. Освен това беше извършен анализ на обогатяване на генен набор (GSEA), за да се идентифицират разликите в набора от гени, експресирани между двата клъстера в обогатяването на пътя на KEGG. Броят на пермутациите е извършен 1000 пъти за
всеки анализ и пътищата с коригирана p-стойност<0.05 and="" q="" values=""><0.05 were="" considered="" statistically="">
Прогноза за лекарствения отговор
Въз основа на информацията, извлечена от базата данни на Genomics of Drug Sensitivity in Cancer (GDSC) (https://www.cancerrxgene.org/), бяха изчислени химиотерапевтичните чувствителност за ccRCC. Бяха избрани три общи клинични лекарства за прогнозиране на химиотерапевтичния отговор и R пакетът "pRRophetic" беше използван за оценка на химиотерапевтичния отговор, определен от полумаксималната инхибиторна концентрация (IC50).
Клетъчни линии и RT-qPCR анализ
Човешките ccRCC клетъчни линии, 786-O и Caki-1, са предоставени от Haixiang Shen, а нормалната клетъчна линия от човешки бъбречен кортекс, HK-2, е предоставена от Yanhong Ma.RPMI 1640 среда (Gibco), допълнена с 10 процента фетален говежди серум (FBS, Gibco), се използва за култивиране на клетките. И всички клетки бяха култивирани при 37 градуса с 5 процента въглероден диоксид. Общите РНК се екстрахират от клетките с Trizol Kit (Invitrogen, Карлсбад, Калифорния, САЩ) съгласно инструкциите на производителя. Първата верига (cDNA) беше обратно транскрибирана и използвана като шаблон за qPCR анализ, както е описано по-горе [10]. Нивата на експресия на регулаторите на пироптоза (AIM2, NOD2, GZMB и CASP5) бяха измерени с помощта на SYBR Green qPCR Kit (Takara, Япония). Името на гена и последователностите на праймера са изброени в Допълнителен файл 5: Таблица S2. Нивата на тРНК на всички гени бяха нормализирани до GAPDH (ендогенна нормализираща референция).
Статистически анализ
Статистическият анализ беше извършен с помощта на софтуер R (http://www.R-project.org, версия 4.0.3), език за програмиране PERL (версия 5.32.1.1, https://www.perl. org /) и GraphPad Prism 8.0. Коефициентите на корелация бяха изчислени чрез Spearmen и корелационни анализи на разстояние. Бяха начертани кривите на Kaplan-Meier и беше използван логаритмичен тест за изчисляване на значителната разлика в оцеляването. Тестът за знаков ранг на Wilcoxon беше използван за анализ на непрекъснати променливи, докато тестът хи-квадрат беше използван за анализ на категоричните данни. Резултатите от RT-qPCR бяха изразени като средна стойност ± SEM. Разликите между групите бяха оценени чрез еднопосочен ANOVA, последван от ad hoc теста за множество сравнения на Dunnett за сравнение с нормални бъбречни клетки. P-стойност по-малка от 0.05 се счита за статистически значима за всички анализи.

Резултати
Идентифициране и класификация на диференциално свързаните с пироптоза регулатори
Експресията на 37 свързани с пироптоза гени беше сравнена в кохортата TCGA-KIRC и 11 гена бяха идентифицирани като диференциално експресирани гени (Фиг. 1А). След като два независими набора от данни от базата данни GEO бяха използвани за външно илюстриране на експресията на тези 11 гена в ccRCC, шест свързани с пироптоза регулатори (AIM2, CASP5, NLRP3, NOD2, GZMA и GZMB) показаха, че са силно експресирани в ccRCC (фиг. .1B). Комбинирана с прогностична информация за пациента, изтеглена от набори от данни на TCGA, след това беше приложена едномерна регресия на Кокс за скрининг на гени от тези 6 регулатора и четири от тях (AIM2, CASP5, NOD2 и GZMB) бяха значително свързани с прогнозата на пациента с ccRCC (фиг. 1C) . За по-нататъшно изследване на връзката между експресията на тези 4 регулатора и подтипове ccRCC, беше извършен консенсусен клъстерен анализ с кохортни пациенти на TCGA-KIRC. Консенсусният клъстерен анализ беше извършен с пациенти с ccRCC въз основа на тези четири регулатора на пироптоза и резултатът показа, че клъстерната променлива (k) =2 е идентифицирана като най-високата клъстерна стабилност от k =1 до 9, което показва, че че пациентите с ccRCC могат да бъдат разделени на два клъстера с най-високи вътрешногрупови корелации и най-ниски междугрупови корелации (фиг. 1D). Освен това, пациентите в Клъстер 1 са имали благоприятна обща преживяемост (OS) в сравнение с тези в Клъстер 2 (Фигура 1E).

ВРЕМЕВ анализ на клъстерите според регулаторите на пироптозата
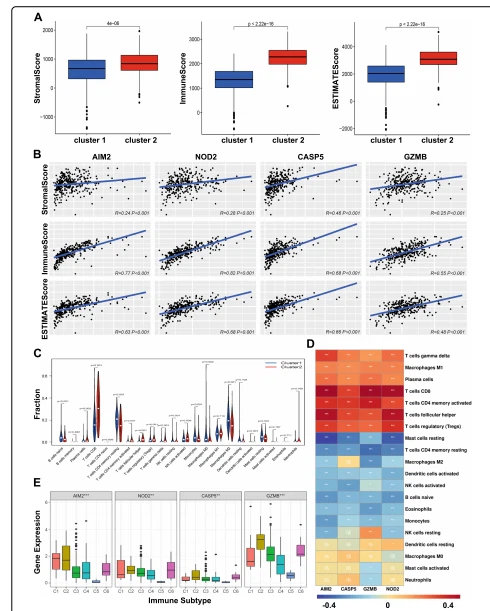
За да се проучи кои пътища са обогатени в клъстерите, беше извършен GSEA анализ, за да се идентифицират значимите KEGG пътища, свързани с двата клъстера. Резултатите показват, че взаимодействието на цитокиновите рецептори, сигнализиращият път на Т-клетъчния рецептор, обработката и представянето на антигена, сигналният път на хемокините, медиираната от естествените клетки-убийци цитотоксичност, сигнализиращият път на Toll-подобния рецептор, сигнализиращият път на В-клетъчния рецептор и JAK-STAT сигнализирането пътят са значително свързани с клъстер 2 (допълнителен файл 1: фигура S1), което показва, че клъстерите, съдържащи регулатори на пироптоза, са свързани с туморна имунна микросреда. Следователно, за да се проучи разликата в имунната функция между двата клъстера, бяха изчислени ESTIMATE резултати и се демонстрира, че Клъстер 2 има значително по-високи ESTIMATE, стромални и имунни резултати в сравнение с Клъстер 1 (фиг. 2A), а четирите регулатора на пироптоза са положителни свързани с тези резултати (фиг. 2B). Освен това, двата клъстера разкриват значителни разлики в инфилтрацията на имунните клетки (фиг. 2C). Клъстер 1 притежаваше по-високи инфилтрирани нива на неактивни В клетки, Т клетки CD4 в покой, NK клетки в покой, моноцити, макрофаги M0, макрофаги M2, активирани дендритни клетки и мастоцити в покой, докато Клъстер 2 беше по-висок свързани с плазмени клетки, Т клетки CD8, Т клетки с активирана памет, Т клетки фоликуларен помощник, Т клетки регулаторни (Tregs), Т клетки гама делта и активирани NK клетки. Анализът на корелацията между четирите регулатора и типа имунни клетки показа, че четирите регулатора имат положителна или отрицателна корелация с повечето типове имунни клетки (Фигура 2D). Интересно е, че по-нататъшно изследване на диференциалната експресия на имунни гени между два клъстера разкрива, че маса от имунни гени е регулирана нагоре в Клъстер 2, докато само 5 гена са регулирани надолу (Допълнителен файл 2: Фигура S2A). 10-те най-регулирани нагоре и надолу гени бяха избрани за анализ на корелацията и резултатът е показан в Допълнителен файл 2: Фигура S2B. GO анализът на биологичните процеси показа, че диференциалната експресия на имунните гени между клъстерите е обогатена чрез активиране на сигналния път на рецептора на клетъчната повърхност и сигналната трансдукция наимунен отговор. Анализът на клетъчните компоненти показва, че диференциално експресираните имунни гени са изобилни в имуноглобулиновия комплекс. Анализът на молекулярната функция показва, че диференциално експресираните имунни гени включват свързване на антиген. KEGG анализът показа, че диференциално експресираните имунни гени са обогатени с взаимодействия цитокин-цитокинов рецептор (Допълнителен файл 2: Фигура S2C, D). Тези резултати показват, че Клъстер 2 и четирите регулатора са замесени в туморната имунна микросреда.
Асоциация на регулаторите на пироптозата с инхибиторите на имунната контролна точка и таргетната лекарствена чувствителност Терапиите с инхибитор на имунната контролна точка (ICI) са установени като мощна възможност за лечение на множество видове тумори, докато само част от пациентите се възползват от такава терапия. Следователно диференциалното изразяване на ICI в различни подтипове беше допълнително проучено. Осем гена на гореща имунна контролна точка (SIGLEC15, TIGIT, PD-L1, TIM3, PD-1, CTLA4, LAG3 и PD-L2) бяха положително свързани с клъстер 2 (Фигура 3A, B). Интересното е, че четири регулатора бяха тясно свързани с повечето ICI, докато нямаше значителна връзка между GZMB и SIGLEC15 (фиг. 3C). Освен това, като се има предвид стойността на клиничното лечение в чувствителността на целевите лекарства, сунитиниб и темсиролимус показват по-голяма чувствителност в клъстер 1, докато акситиниб е тясно свързан с клъстер 2 (фиг. 3D-F). Тези резултати показват, че тази класификация може да осигури определена референтна стойност за клиничното лечение на различни пациенти с ccRCC.

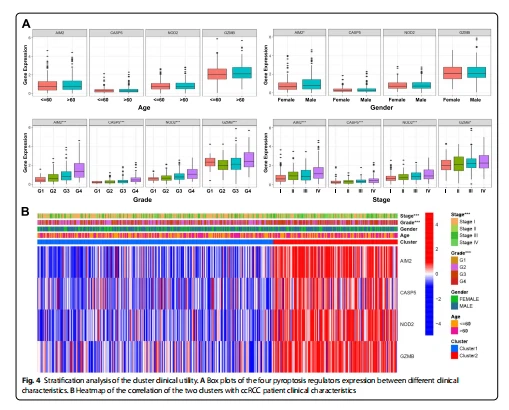
Стратификационен анализ на клъстерната клинична полезност За по-нататъшно изследване на клиничната стойност на връзката между тази класификация и различните клинични характеристики, пациентите с ccRCC бяха разделени на различни групи според възрастта на пациента, пола, степента и стадия на заболяването. Струва си да се отбележи, че по-високият стадий на заболяването е по-свързан с пациентите в Клъстер 2, както и с патологичната степен (Таблица 1; Фиг.4B). Допълнителен анализ на връзката между регулаторите на пироптозата и клиничните характеристики показа, че нивото на експресия на четирите регулатора се повишава с увеличаването на стадия на заболяването и патологичната степен, докато само AIM2 е по-силно експресиран при мъжете, отколкото при жените. Няма значителна разлика между експресията на четирите регулатора и възрастта на пациента (Фигура 4А).

Експериментална проверка на експресията на четирите регулатора Въз основа на биоинформационния анализ на експресията на тези четири регулатора, ние анализирахме нивата на експресия на иРНК и протеина. В сравнение с нормалните клетки, нивата на експресия на тези 4 гена бяха регулирани нагоре в различна степен в двете ccRCC клетъчни линии (фиг. 5А). Съответно, моделите на протеинова експресия на AIM2, NOD2 и GZMB от базата данни на HPA разкриха, че регулаторите също са свръхекспресирани в ccRCC тъкан в сравнение с нормалната тъкан (фиг. 5B).

Четири модела на експресия на регулатор на пироптоза при множество ракови заболявания
По-нататъшно изследване на модела на експресия на тези четири регулатора на пироптоза при пан-рак показа, че четири регулатора на пироптоза са диференциално експресирани в множество ракови заболявания (Фигура 6A). AIM2 е диференциално експресиран в множество ракови заболявания, включително рак на пикочния мехур, гърдата, хранопровода, бъбреците, черния дроб , белия дроб, стомаха и ендометриума, както и CASP5, NOD2 и GZMB (фиг.6A). По-нататъшен анализ установи, че AIM2 е най-положително свързан с HNSC, докато CASP5 е отрицателно свързан с COAD (Фигура 6B). А AIM2 и GZMB бяха двата гена с най-значима положителна асоциация (коефициент на корелация =0.59, фиг.6C).
По време на прогресирането на рака туморните клетки могат постепенно да загубят диференциран фенотип и да придобият характеристики, подобни на прогениторни и стволови клетки[11]. Като цяло, RNAss и DNAss могат да се използват за оценка на стволовостта на раковите стволови клетки [12]. Следователно, беше изследвана корелацията между регулаторите на пироптоза с стволовостта на тумора, измерена чрез RNAss и DNAss. Четирите регулатора са значително положително или отрицателно корелирани с RNAss и DNAss в повечето пан-ракови заболявания (Фигура 6D). По-специално, в KIRC, AIM2 и GZMB бяха положително или отрицателно свързани с РНК, съответно, докато NOD2 беше отрицателно свързан с DNAss (Допълнителен файл 3: Фигура S3).

Асоциация на четирите регулатора на пироптоза с туморна имунна микросреда при пан-рак
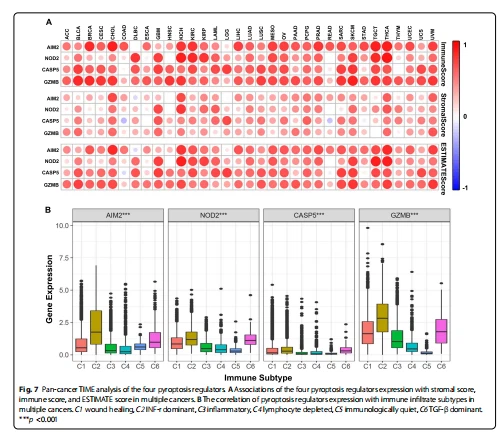
Въз основа на важния регулаторен ефект на гените на пироптозата върху различни типове имунни клетки, четирите регулатора бяха допълнително изследвани в панраковата микросреда. Интересното е, че освен AIM2 беше отрицателно свързан с DLBC и CASP5 беше отрицателно свързан с COAD и READ в резултата ESTIMATE и стромалния резултат, други бяха положително свързани с ракови заболявания в имунния резултат, стромалния резултат и ESTI-MATE резултата (Фиг.7A ). За да се изследва експресията на четирите регулатора на пироптоза в различни имунни подтипове при пан-рак, имунните инфилтрати бяха разделени на шест типа за анализ, които съответстват съответно от стимулиращи тумора до туморно супресивни, включително заздравяване на рани, IFN-y доминиращ, възпалителни, лимфоцитни изчерпан, имунологично тих и TGF- доминиращ. Интересното е, че четирите регулатора на пироптоза бяха значително свързани с имунните подтипове и четирите регулатора на пироптоза бяха най-силно експресирани в IFN-y доминиращ, последван от TGF- доминиращ (Фигура 7B). В KIRC, обаче, експресията на четирите регулатора на пироптоза е най-висока в C2, както при анализа на панрак. AIM2, който има втората най-висока експресия в имунните подтипове, е свързан с Cl, докато NOD2, CASP5 и GZMB са свързани с C6 (фиг. 2E).

Дискусия
Хирургичната резекция е първото лечение на бъбречноклетъчен карцином в нашата клинична практика. Въпреки това, все още е трудно да се отстранят метастазите на бъбречноклетъчния карцином. Метастатичният бъбречноклетъчен карцином е резистентен на лъчетерапия и системна терапия, включително хормонална терапия и химиотерапия [13]. Клинично изпитване на nivolumab, анти-PD-L1 инхибитор на имунната контролна точка, за лечение на метастатичен ccRCC (CheckMate-025) показа, че nivolumab има значително по-добро OS, коефициент на риск, ORR и общ процент на отговор [ 14]. Тези проучвания показват, че приложението на имунотерапията при лечението на ccRCC има големи перспективи. Един задълбочен анализ на хетерогенността на ccRCC TIME може да помогне да се осигури прецизно и индивидуализирано управление на имунотерапията за подобряване на ефекта от лечението и качеството на прогнозата за преживяемост на пациента. Тук пациентите с ccRCC бяха разделени на два независими молекулярни подтипа с различни клинични характеристики, експресия на имунен ген и TIME чрез консенсусно групиране за четири основни регулатора на пироптоза. Според настоящото проучване Клъстер 2 има по-лоша прогноза от Клъстер 1, но Клъстер 2 е по-чувствителен към имунотерапия.
Сред присъщите механизми на смърт на клетките, пироптозата получава все по-голямо внимание. Пироптозата е новоразпознат тип програмирана възпалителна клетъчна смърт, която се активира чрез пътища, медиирани от класическа каспаза-1 инфламазоми или некласическа каспаза-4, каспаза-5 и каспаза{{4} } [15]. Наскоро появиха се доказателства за важната роля на пироптозата в туморогенезата на човешки злокачествени заболявания [16,17]. Пироптозата инхибира туморния растеж при колоректален рак, рак на черния дроб и рак на кожата, но има двупосочен ефект върху рака на гърдата [18-20]. В ccRCC остава неизвестно как взаимодействат свързаните с пироптоза гени и дали те са свързани с времето за оцеляване на пациента. Експресията на повечето регулаторни гени на пироптоза е положително корелирана и играе важна прогностична роля при ccRCC. Тези открития предполагат, че регулаторите на пироптоза могат да играят ключова роля в регулирането на туморогенезата и развитието на ccRCC. В настоящото проучване бяха идентифицирани четири регулатора на пироптоза, които са силно изразени при рак на бъбреците и причиняват лоша прогноза. AIM2 е цитозолен вроден имунен рецептор, който разпознава двойноверижна ДНК (dsDNA), освободена по време на клетъчно смущение и патогенно нападение. Активираният AIM2 активира класическия път на пироптоза чрез каспаза-1 [21]. AIM2 може да играе уникална роля при различни видове рак [22-25] и настоящото проучване показа, че AIM2 играе роля, насърчаваща рака при ccRCC. Каспаза-5(CASP5), подобно на каспаза-4 и каспаза-1l, е изпълнителен протеин на каспаза-1-независима пироптоза [26]. GZMB се използва от цитотоксичните лимфоцити като молекулярно оръжие за защита срещу инфектирани с вируси и злокачествено трансформирани клетки гостоприемници[27]. Ниската експресия на GZMB е свързана с ранни метастази при колоректален рак, което предполага инфилтрация на кръвоносни съдове и нерви [28]. Интересното е, че нашият анализ установи, че GZMB е положително корелиран ген при рак на бъбреците. NOD2 е рецептор за разпознаване на образи, който може да регулира вродения имунен отговор на гостоприемника и да предотврати възпаление, стеатоза и затлъстяване [29]. Извънклетъчният хистон H3, индуциран от LPS, може да причини пироптоза по време на сепсис чрез пътища NOD2 и VSIG4/NLRP3 [30]. Остава неизвестно как тези гени взаимодействат помежду си по време на клетъчна пироптоза в ccRCC.
В нашата клинична практика тирозин киназните инхибитори на рецептора на съдовия ендотелен растежен фактор (VEGFR-TKIs) се превърнаха в стандарт за лечение на mRCC [31]. Сунитиниб, широкоспектърен инхибитор на рецепторни тирозин кинази, е широко използван като стандарт за лечение на първа линия терапия на напреднал ccRCC [32]. Въпреки това, не всички пациенти с RCC са чувствителни към лечението със сунитиниб и повечето пациенти ще развият резистентност към сунитиниб след няколко месеца лечение. Следователно, ключът към избора на сунитиниб за лечение е да се изберат пациенти, които са чувствителни към сунитиниб. Настоящото проучване показа, че клъстер 1 е по-чувствителен към сунитиниб, докато клъстер 2 е по-чувствителен към акситиниб.
Разбирането на експресията на регулаторите на пироптоза в ccRCC преди лечението може да помогне за проектиране на по-оптимизирани целеви възможности за лечение в полза на пациентите. Някои проучвания показват, че ефективният провъзпалителен ефект на пироптозата е свързан с регулирането на туморната имунна микросреда [33]. Въпреки това, потенциалната роля на пироптозата в имунната микросреда на ccRCC все още е неуловима. Въз основа на характеристиките на експресията на регулаторите на пироптоза, настоящото проучване показва, че пациентите в различни клъстери имат различни корелации с различни имунни инфилтрации. В клъстер 1 се наблюдават по-високи инфилтрирани нива на неактивни В клетки, Т клетки CD4 в покой, NK клетки в покой, моноцити, макрофаги M0 и макрофаги M2. От друга страна, клъстер 2 е по-високо свързан с CD8 плюс Т клетки, Tregs и Т фоликуларни помощни клетки. Tregs могат да секретират различни имуносупресивни цитокини, водещи до имунно бягство на туморните клетки. Проучванията показват, че Tregs ефективно инхибират пролиферацията на ефекторни Т клетки и високото ниво на инфилтрация на CD8+ Т клетки е неблагоприятен прогностичен фактор за ccRCC [34,35]. Лошата прогноза на клъстер 2 и заключенията от тези две заключения са взаимно съгласувани. Клъстер 2 е в положителна корелация с осем горещи ICI (SIGLEC15, TIGIT, PD-L1, T IM3, PD-1, CTLA4, L AG3 и PD-L2). Въз основа на тези констатации, лошите резултати за оцеляване на Клъстер 2 може да са причинени от намаленото ниво на антитуморен имунитет и Клъстер 2 може да бъде по-полезен при имунотерапията. Резултатите от GSEA показват, че клъстер 2 е свързан с различни имунорегулаторни сигнални пътища. Важно е, че сигналният път на JAK-STAT е свързан с канцерогенезата и имунната инфилтрация на ccRCC. По този начин спекулирахме, че пироптозата може да регулира състава на туморната имунна микросреда. Нашето проучване предполага, че ccRCC с висока експресия на тези 4 гена може да бъде по-чувствителен към имунотерапия.
Нивото на експресия на четирите регулатора се повишава с увеличаване на стадия на заболяването и степента на патология и няма значителна разлика между експресията на четирите регулатора и възрастта на пациента, което е в съответствие с по-лошата прогноза на клъстер 2.
Като се има предвид, че пироптозата е широко включена в различни биологични процеси, ние изследвахме дали тези четири регулатора на пироптоза в клъстер 2 също играят важна роля при други видове рак. Впоследствие беше извършен анализ на панрак и резултатите показаха, че тези четири регулатора на пироптоза са тясно свързани със стромалния резултат, имунния резултат и резултата ESTIMATE при множество видове рак. Тези резултати показват, че тези четири регулатора на пироптоза са потенциални мишени за различни имунотерапии на рак и не се ограничават до ccRCC.
В бъдеще е необходим допълнителен надежден анализ за проверка в по-голяма кохорта. Освен това са необходими допълнителни in vitro и in vivo експерименти за изясняване на регулаторния механизъм между регулаторите на пироптозата и туморната имунна микросреда.
Изводи
В обобщение, това проучване систематично анализира профила на експресия на регулаторите на пироптоза в ccRCC и неговата корелация с имунните контролни точки и ролята в туморната имунна микросреда. Експресията на регулаторите на пироптоза е значително свързана с имунните контролни точки като PD-L1 и CTLA4. Два независими подтипа също бяха установени чрез последователното групиране на регулатори на пироптоза. Туморна хетерогенност и разлики в експресията на имунната контролна точка и туморната имунна микросреда са наблюдавани между двата подтипа, което ще помогне за стратификация на риска и прецизно лечение на пациенти с ccRCC. Едноетапен панраков анализ показа, че тези регулатори на пироптоза са тясно свързани със стромалния резултат, имунния резултат и резултата ESTIMATE при много видове рак. Важно е, че бъдещи клинични изпитвания и основни изследвания ще помогнат за определяне на целите за подобряване на ефикасността на имунотерапията срещу рак.
