Експресия на имуноглобулин G в човешки проксимални тубулни епителни клетки
Mar 18, 2022
Контакт: Audrey Hu Whatsapp/hp: 0086 13880143964 Имейл:audrey.hu@wecistanche.com
ZHENLING DENG и др
Резюме. Проксималентръбенепителни клетки (PTECs) имат вродени имунни характеристики и произвеждат провъзпалителни фактори, хемокини и компоненти на комплемента, които управляват епителен-мезенхимален преход (EMT). Нашите предишни проучвания разкриха, че човешките мезангиални клетки и подоцити са способни да синтезират и секретират съответно имуноглобулин (Ig) A и IgG. Целта на настоящото изследване беше да се оцени експресията на Igs в PTECs. Първо, IgG се открива в цитоплазмата, клетъчната мембрана и лумена наPTECsв нормалната бъбречна кора отимунохистохимия. Второ, транскрипция на Ig ген и V(D)J рекомбинация бяха открити в единични PTEC чрез вложена PCR и Sanger секвениране. Трето, Ig, Igκ и Igλ бяха ясно открити в обезсмъртена PTEC линия (HK-2) чрез имунооцветяване и Western blotting, в които беше използван RP215 (антитяло, което се свързва предимно с не-В клетъчен IgG). В допълнение, Ig , Igκ и Igλ генни транскрипти, консервативна V(D)J рекомбинация в Ig променливата област, рекомбинация, активираща ген 1/2 и индуцирана от активиране цитидин деаминаза, всички бяха открити в HK-2 клетки. Тези данни предполагат, че PTEC могат да експресират IgG по начин, подобен на В клетките. Освен това експресията на IgG се регулира нагоре от TGF‑1 и може да бъде включена в ЕМТ.
Ключови думи:проксималентръбенепителни клетки, едноклетъчни, HK‑2, IgG, епителен-мезенхимален преход

Cistanche tubulosa предотвратява бъбречни заболявания, щракнете тук, за да получите пробата
Въведение
Проксималентръбенепителни клетки (PTECs) са най-разпространеният тип клетки вбъбреки имат важна роля в възстановяването на бъбреците и/или прогресирането на хронични бъбречни заболявания. PTEC упражняват имунологични функции чрез експресиране на множество Toll-подобни рецептори (TLR), като TLR 1, 2, 3, 4 и 9 (1,2), и молекули, свързани с антиген-представящата клетъчна функция, включително MHCII, CD74, CD80 и CD86 (3). Тези вродени имунни характеристики на PTECs им позволяват да действат като имунни отговори на широк спектър от стимули, с последващо производство и освобождаване на биоактивни медиатори, включително провъзпалителни цитокини, хемокини и компоненти на комплемента, които стимулират интерстициално възпаление и фиброза (4). PTEC също експресират неонатални Fc рецептори и запазват капацитета на специфично рН-зависимо свързване и трансцитоза на имуноглобулин (Ig)G (5). Въпреки това, доколкото ни е известно, остава неизвестно дали PTEC експресират Igs.
По-рано се предполагаше, че Ig се произвеждат единствено от зрели В клетки и плазмени клетки и че Ig действат като антитела за разпознаване и неутрализиране на различни патогени. Въпреки това, тази теория беше оспорена през последните десетилетия, тъй като все повече доказателства съобщават, че Ig, включително IgA, IgG и IgM, могат да бъдат произведени и секретирани от не-В клетки, като човешки епителни ракови клетки (6,7) и нормални не-В клетки (8, 9), както и в имуно-привилегировани места, като очите (10), централните неврони (11, 12), плацентата (13) и тестисите и епидидима (14)
Подобно на Igs, получени от В клетки (B-Igs), не-B-Igs също са продукти на транскрипция и пренареждане на Ig ген и показват класически модели на V(D)J рекомбинация с нуклеотидни добавки в кръстовищата и соматични хипермутации (7, 11,14). За разлика от B-Igs, не-B-Igs показват ограничени модели на V(D)J рекомбинация и по-малко разнообразие (7). Функционално, не-B-Igs не само упражняват активност на естествени антитела в кожата и лигавицата (8), но могат също така да действат като растежни фактори за насърчаване на клетъчната пролиферация и адхезия и могат да подобрят инициирането и метастазите на рак чрез свързване с интегрини ( 15-17). Например, разпознатият от RP215 раков IgG изпълнява своята онкогенна функция, като взаимодейства с комплекса интегрин 6 4 и активира FAK и Src пътищата (15).
Предишното ни проучване показа, че мезангиалните клетки (18) и подоцитите (19) могат да синтезират и секретират IgA и IgG и да участват в клетъчния растеж и клетъчната адхезия in vitro. Настоящото проучване имаше за цел да оцени нивата на експресия на Igs в PTECs и да изследва потенциалната му роля в епителен-мезенхимния преход (EMT).

Ефекти на цистанхе: благоприятства бъбреците
Материали и методи
Клетъчна култура и лечение.Увековечена PTEC линия HK‑2 беше закупена от American Type Culture Collection. HK-2 клетки се култивират в DMEM/F12, допълнен с 100 U/ml пеницилин, 0,1 mg/ml стрептомицин (всички Gibco; Thermo Fisher Scientific, Inc.) и 10 процента фетален говежди серум (FBS; Австралийски произход; Biological Industries USA, Inc.) при 37˚C в атмосфера, съдържаща 95 процента въздух и 5 процента CO2. За да се избегне намесата на Ig в FBS, средата беше заменена със среда без серум 24-48 часа преди събирането на клетките. HK-2 клетки бяха третирани с различни концентрации (2, 5 и 10 ng/ml) на TGF-1 (Sigma-Aldrich; Merck KGaA).
Единична PTEC изолация и cDNA синтез.Проба от човешки бъбрек от макроскопски нормална кортикална тъкан е получена от пациент (мъж, 31 години), подложен на нефректомия в резултат на бъбречен карцином без очевидна бъбречна дисфункция. Едноклетъчна суспензия се приготвя чрез смилане на бъбречната кора с 1 mg/ml колагеназа I (Sigma-Aldrich; Merck KGaA) при 37˚C за 20 минути. PTEC бяха сортирани с помощта на фикоеритрин (РЕ)-конюгиран анти-CD10 (кат. № 312203) и алофикоцианин (APC)-конюгиран анти-CD13 (кат. № 301705; и двете BioLegend, Inc.) чрез флуоресцентно-активирано клетъчно сортиране ( BD FACSAria II Special Order System), както е описано по-горе (20). Съответните изотипни контролни антитела (кат. № 400111 и 400119; и двете BioLegend, Inc.) бяха използвани за изключване на неспецифично оцветяване. Двойно положително белязани живи клетки бяха изолирани като PTECs. Единичен PTEC беше избран ръчно под обърнат светлинен микроскоп с помощта на капилярна пипета и след това беше прехвърлен в 0,2-ml тънкостенна PCR епруветка, съдържаща лизисен буфер (21). Екстракцията на единична PTEC РНК и синтезът на cDNA се извършват съгласно описаните по-рано методи (21). Общо пет единични PTEC бяха използвани за откриване на транскрипция и пренареждане на Ig ген.
PCR амплификация.Общата РНК се екстрахира от HK-2 клетки, периферни кръвни мононуклеарни клетки [PBMCs, изолирани от 31-годишна здрава донорка с помощта на Ficoll (кат. № 7111011; Dakewe Biotech., Ltd.) ] и бъбречна кора (от същия пациент, използван при единична PTEC изолация) с помощта на реагент TRIzol® (Invitrogen; Thermo Fisher Scientific, Inc.), а концентрацията на РНК беше оценена с помощта на NanoDrop спектрофотометър (NanoDrop; Thermo Fisher Scientific, Inc.) . Впоследствие, 2 µg обща РНК се транскрибира обратно към сДНК, като се използва RevertAid First Strand cDNA Synthesis kit (кат. № K1622; Thermo Fisher Scientific, Inc.). PCR се извършва с помощта на праймери, насочени към постоянните региони на Ig, Igκ, Igλ и индуцирана от активиране цитидин деаминаза (AID). Беше извършена вложена PCR за амплифициране на променливата област на Ig, протеин 2, свързан с рецептора на липопротеин с ниска плътност (LRP2) и ген, активиращ рекомбинация (RAG)1 и RAG2. PCR продуктите се разделят чрез електрофореза върху 1.0% агарозен гел и се визуализират с помощта на GelRed (кат. № 41003; Biotium, Inc.). Праймерите на AID, RAG1/2 и постоянните региони на Ig, Igκ, Igλ, използвани в това изследване, се отнасят до праймерите, използвани от Jing et al (19). Праймерите на Ig променливата област се отнасят до праймерите, използвани от van Dongen et al (22). Другите праймери, използвани за PCR, са изброени в таблица SI. Условията на термоциклиране са изброени в Таблица SII.
Секвениране на Sanger и анализи на данни за секвениране.PCR продуктите на Ig променливия регион, получени от единични PTECs, HK-2 клетки и PBMCs бяха съответно клонирани в pGEM-T Easy Vector System I (кат. № A1360; Promega Corporation), която беше трансформирана в ТОП10 компетентни клетки (CB104; Tiangen Biotech Co., Ltd.). Накратко, 5 µl продукти на лигиране бяха добавени към 30 µl TOP10 компетентни клетки, инкубирани върху лед за 30 минути, подложени на топлинен шок при 42˚C за 90 секунди и инкубирани върху лед за 5 минути. След това се добавят 500 µl LB и се оставят да престоят при 37˚C в продължение на 40 минути преди да се инокулира част от бактериалната течност върху петриеви панички, покрити с 0,1 mmol/l IPTG и 20 µg/ml X-Gal. Съдовете се обръщат при 37˚C за една нощ. Общо 5-16 бели колонии на проба бяха избрани на случаен принцип и секвенирани с помощта на ABI 3730XL генетичен анализатор (Applied Biosystems; Thermo Fisher Scientific, Inc.). Пренаредените V(D)J последователности бяха сравнени с тези в основния инструмент за търсене на локално подравняване (https://www.ncbi.nlm.nih.gov/igblast/), за да се идентифицират най-добре съвпадащите генни сегменти и връзки на зародишна линия след изрязване на праймера .
Western blot анализ.HK-2 клетките бяха лизирани в TSD лизисен буфер [1 процент SDS, 50 mM Tris-HCl (рН 7,5), 50 mM DTT], съдържащ протеазен инхибиторен коктейл (Applygen Technologies Inc.), обработен с ултразвук в ледена вода за 1 минута ( работа 5 секунди и почивка 15 секунди; 3 пъти) и лизирани за 30 минути при стайна температура. След центрофугиране при 12,000 xg за 10 минути при 4˚C, протеиновата концентрация на клетъчния лизат се определя с помощта на BCA комплект (Applygen Technologies Inc.). Впоследствие към лизата се добавя 5X редуциращ зареждащ буфер, който се вари при 100˚C в продължение на 10 минути и пробите веднага се използват за Western blot анализ. Серумът, използван като положителна контрола за Ig, се изолира от здрав донор (същият донор, използван в PBMC) чрез центрофугиране при 2,103 xg за 10 минути при стайна температура.

Ефекти на цистанхе: благоприятства бъбреците
Уестърн блотинг се извършва съгласно стандартни процедури. Накратко, 3{{40}} µg протеини бяха разделени чрез SDS-PAGE върху 10% гелове и бяха прехвърлени върху нитроцелулозна мембрана. Впоследствие мембраната се блокира в 5 процента обезмаслено мляко при стайна температура за 1 час и се инкубира с първични антитела при 4˚C за една нощ, включително заешки античовешки Ig (кат. № ab109489; 1:1,{{8} }), заешки античовешки Ig 4 (кат. № ab109493; 1:1, 000), анти-Igκ (кат. № ab124727; 1:10, 000), анти- Igλ (кат. № ab124719; 1:20, 000), заешки античовешки ‑актин (кат. № ab8227; 1:2, 000) (всички от Abcam) и RP215 моноклонално антитяло (mAb) (дарено от професор Xiaoyan Qiu, Пекински университет, Пекин, Китай; 1:1, 000), което идентифицира специфично свързан с въглехидрати епитоп върху не-B-Ig. След това мембраната се инкубира с кози анти-заешки (кат. № 926-32211) или анти-миши (кат. № 926-32210) IgG-IRDyeTM680CW вторични антитела (и двете 1:10, 000; и двете LI‑COR Biosciences) при стайна температура за 1 час. Сигналът беше открит с помощта на системата Odyssey Imaging и софтуера Odyssey V3.0 (и двата LI‑COR Biosciences). Софтуерът ImageJ (версия 1.8.0; Национални здравни институти) беше използван за полу-количествено определяне.
Пречистване на IgG и масспектрометрия.След като клетките HK-2 са култивирани в DMEM/F12 без FBS в продължение на 48 часа, супернатантът на културата се събира след центрофугиране при 2,103 xg за 10 минути при 4°C. Клетъчният супернатант се пречиства чрез афинитетна хроматография, като се използва протеин G Sepharose, съгласно инструкциите на производителя (кат. № 17-0618-02; Thermo Fisher Scientific, Inc.). Елуентът беше ултра-филтриран, за да се замени елуиращият буфер (0,1 М глицин; рН 2,4) с PBS. Пречистените протеини бяха разделени чрез SDS-PAGE върху 10% гелове, открити чрез Western blotting и допълнително анализирани чрез масова спектрометрия, извършена от Beijing Protein Innovation Co., Ltd.
Имунофлуоресценция.HK-2 клетки се култивират върху покривни стъкла, които се фиксират в студен неразреден ацетон за 5 минути при стайна температура. Впоследствие предметните стъкла се промиват два пъти в PBS и се блокират с 5 процента FBS/PBS при стайна температура за 20 минути, след което се инкубират с първични антитела при 4˚C за една нощ. Антителата бяха същите като тези, използвани при Western blotting: заешки античовешки Ig (1:150), античовешки Igκ (1:250), античовешки Igλ (1:250) и RP215 mAb (1:200 ); PBS се използва като отрицателна контрола. След промиване в PBS предметните стъкла се инкубират с маркирани с флуоресцеин изотиоцианат кози анти-заешки (кат. № A11008) или кози анти-миши (кат. № A11001) IgG антитела (1:1,000); Invitrogen; Thermo Fisher Scientific, Inc.) при стайна температура за 1 час. Ядрата се оцветяват с DAPI. Изображенията бяха заснети под флуоресцентен микроскоп Leica DFC300 FX (Leica Microsystems GmbH).
Имунохистохимично оцветяване.Параканцерозните бъбречни корти са събрани от четирима пациенти от мъжки пол (на възраст 38-49 години) с бъбречен карцином. Нормалните параканцерозни бъбречни кори след нефректомия се фиксират с 10 процента формалин за 48 часа при стайна температура и след това се поставят в парафин. Вградени в парафин проби от човешки бъбрек бяха нарязани на 3-µm секции и депарафинизирани и рехидратирани чрез серия от степенувани концентрации на етанол. Извличането на антиген се извършва чрез кипене в 0.05 M Tris-EDTA (рН 9,0) в тенджера под налягане за 3 минути. След това срезовете се инкубират с 3 процента разтвор на H2O2 в продължение на 10 минути при стайна температура, за да се елиминира ендогенната пероксидаза и се инкубират с нормален кози серум (кат. № ZLI-9022, ZSGB-BIO, Китай) в продължение на 30 минути при стайна температура, за да се блокират неспецифичните места за свързване на антитяло при стайна температура. Впоследствие беше извършено индиректно имунохистохимично оцветяване с първични антитела при 4˚C за една нощ, включително RP215 mAb (1:200; 5 µg/ml), заешки античовешки Ig (1:2, 000), античовешки Igκ (1:1, 000), античовешки Igλ (1:1, 000) (същите антитела, използвани при Western blotting). Секции без първични антитела бяха използвани като отрицателни контроли. След това слайдовете се инкубират с неразредени вторични антитела, маркирани с пероксидаза от хрян (кат. номера PV-6001 и PV-6002; и двете OriGene Technologies, Inc.) при стайна температура за 30 минути. Свързаните антитела се откриват с помощта на диаминобензидин. Накрая предметните стъкла бяха оцветени с хематоксилин. Изображенията са заснети с помощта на светлинен микроскоп (x200 увеличение). Статистически анализ. Данните са представени като средна стойност ± стандартно отклонение и са анализирани с помощта на SPSS 20.0 за Windows (IBM Corp.). Всички експерименти се повтарят 3 пъти. Разликите между множество групи бяха анализирани с помощта на еднопосочен ANOVA и posthoc тест на Tukey. П<0.05 was="" considered="" to="" indicate="" a="" statistically="" significant="">

Ефекти на цистанхе: благоприятства бъбреците
Резултати
Експресия на IgG в бъбречни тубулни епителни клетки на бъбречната кора.Нормални бъбречни кори, които са събрани от донори, подложени на нефректомия в резултат на бъбречноклетъчен карцином, са използвани за определяне на IgG експресията в бъбречните тубулни епителни клетки чрез имунохистохимия, като се използват антитела срещу човешки Ig, Igκ, Igλ и RP215 (антитяло, което предимно се свързва с не-B-IgG). Положително оцветяване на IgG тежки и леки вериги не беше открито само в PTECs, но също и в дисталните извити тубулни епителни клетки, или в цитоплазмата, клетъчната мембрана или тубуларния лумен (фиг. 1).
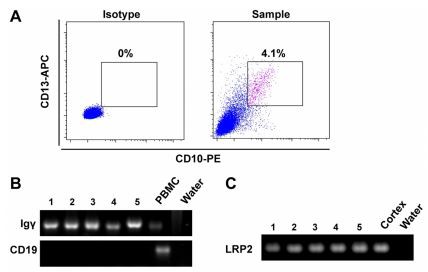
Транскрипция и V(D)J рекомбинация на IgG в единични PTECs. За да се избегне намесата на остатъчната кръв, свързването и трансцитозата на IgG от PTECs в бъбречната кора и за да се получат директни доказателства за IgG експресия в PTECs, единични PTECs бяха сортирани от човешката бъбречна кора с помощта на CD10 и CD13 съвместно маркиране чрез поток цитометрия (20). Както е показано на Фиг. 2A, CD10/CD13 двойно положителни PTEC представляват 4,1 процента от жизнеспособните клетки в пробата. Изолираните PTEC бяха допълнително потвърдени с помощта на специфичния маркерен ген LRP2 и замърсяването на B-клетките беше елиминирано от CD19. Транскриптите на Ig променлива област бяха амплифицирани в пет единични PTECs чрез вложена PCR (фиг. 2B и C). Резултатите от секвенирането на Sanger разкриха, че PTEC показват функционална и консервативна VDJ рекомбинация на IgG тежка верига (Таблица I), което показва, че експресията на IgG може да възникне в PTEC.
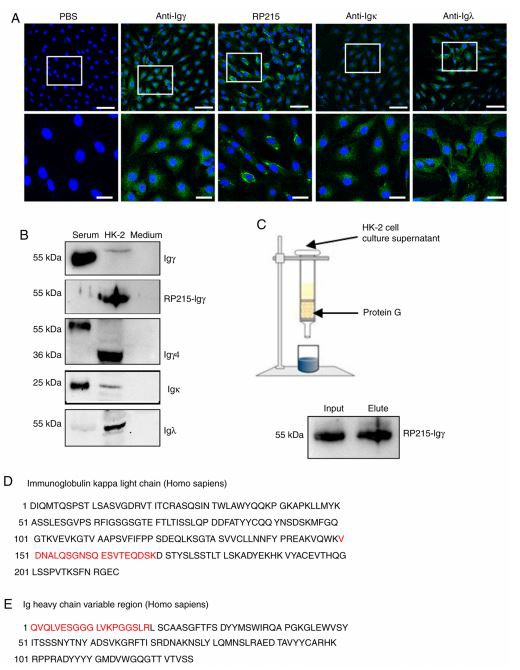
Експресия на тежка и лека верига на IgG в HK-2 клетки. Тъй като беше трудно да се открие експресия на IgG протеин в един PTEC и да се получат достатъчно PTECs за Western blotting, клетъчната линия HK-2, която се състои от обезсмъртени PTECs, беше избрана за по-нататъшно потвърждаване на експресията на IgG протеин. Имунофлуоресцентният анализ демонстрира положително оцветяване на Ig, Igκ и Igλ в цитоплазмата и по-силно положително оцветяване на RP215 предимно в цитоплазмата и клетъчната мембрана (Фиг. 3A).
Впоследствие, експресията на IgG тежки и леки вериги в HK-2 клетки беше открита чрез Western blotting при редуциращи условия. За да се елиминира намесата на FBS в културалната среда, средата, съдържаща FBS, се попива със съответните антитела и се оцветява отрицателно. Търговско IgG антитяло успя да открие IgG, получен от серум, но не и IgG, получен от HK-2. Обратно, RP215 може да открие IgG, получен от HK-2, но не и серумен IgG. И търговското IgG антитяло, и RP215 успяха да открият Ig при 55 kDa. Ивица Ig 4 (36 kDa) беше открита в HK-2 клетки, в съответствие с прогнозираното молекулно тегло. Освен това, експресии на Igκ (25 kDa) и Igλ (50 kDa, димер) се наблюдават в клетъчните лизати (Фиг. 3В). Впоследствие, IgG в клетъчния супернатант беше пречистен от протеин G, потвърден чрез Western blotting и секвениран чрез масспектрометрия, което демонстрира, че 55-kDa лентата съдържа фрагменти от Igκ веригата и променливата област на тежката верига на Ig, според Националния център за База данни за биотехнологична информация (NCBI) (фиг. 3C‑E). Тези данни предполагат, че HK-2 клетки произвеждат и секретират IgG протеин.

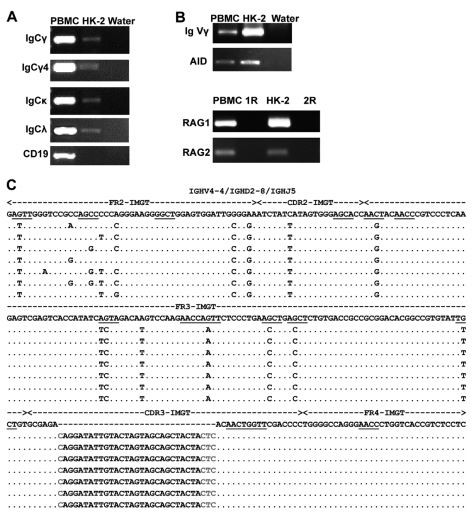
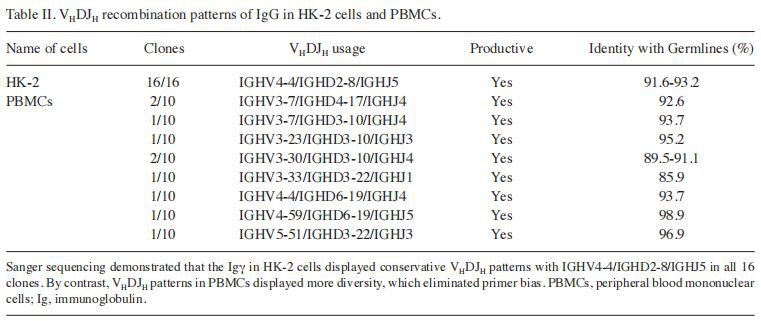
Транскрипция и V(D)J рекомбинация на IgG тежки и леки вериги в HK-2 клетки. Транскрипцията на Ig ген и функционалната V(D)J рекомбинация е предпоставка за Ig експресия. За да се потвърди експресията на IgG в HK-2 клетки, Ig , Igκ и Igλ транскриптите бяха оценени чрез амплифициране на постоянните и променливи региони в HK-2 клетките (фиг. 4A и B). Секвенирането на постоянните PCR продукти показва висока хомология с публикуваната последователност в базата данни на NCBI. T-A клонирането и секвенирането на Sanger показаха, че Ig в HK-2 клетки показва консервативна V(D)J рекомбинация с VH4-4/D2-8/JH5. Обратно, разнообразието на V(D)J рекомбинация се наблюдава в PBMCs, което елиминира отклонението на праймера (Таблица II). Подобно на В клетките, получените от HK-2 IgG показват типична продуктивна V(D)J рекомбинация с V-D и D-J връзките (фиг. 4C). Освен това, соматичните хипермутации бяха открити в Ig, получен от HK-2 (диапазон, 6,8-8,4 процента) със 7 от 15 мотива на горещи точки (RGYW/WRCY, W=A/T, R= A/G, Y=C/T) с мутации.
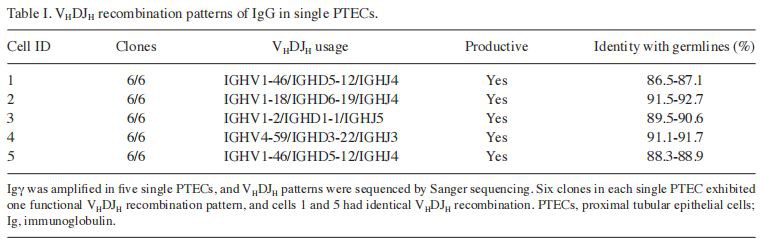
В допълнение, AID транскрипти (основен елемент за соматична хипермутация и рекомбинация на клас превключвател в В клетки) и RAG1 и RAG2 [необходими за V(D)J рекомбинация] бяха открити в HK-2 клетки (фиг. 4B), което показва, че механизмът, лежащ в основата на синтеза на Ig в HK-2 клетките, може да бъде подобен на този в В клетките.
TGF‑1 повишава експресията на IgG в HK‑2 клетки. HK-2 клетките бяха стимулирани с различни концентрации на TGF-1 в продължение на 48 часа. Имунофлуоресцентното оцветяване разкрива, че цитоплазменият IgG показва засилено положително оцветяване в сравнение с контролната група (фиг. 5А). Western blotting потвърди, че IgG е значително повишен от TGF-1 (P<0.05; fig.="" 5b="" and="">

Ефекти на цистанхе: благоприятства бъбреците
Дискусия
Настоящото проучване демонстрира, че PTECs експресират IgG с генна транскрипция и функционална консервативна V(D)J рекомбинация, която е подобна на не-B-IgG. TGF‑ 1 повишава експресията на IgG в HK2 клетки.
За да се изследва дали PTEC експресират IgG, IgG първо се открива в цитоплазмата, клетъчната мембрана и лумена на PTEC в нормалния човешки бъбречен кортекс чрез имунохистохимия; резултатите показват, че PTEC произвеждат и секретират IgG. Това е в контраст с нашето рутинно патологично изследване, при което не е открит очевиден IgG в PTECs. Това може да се дължи на много слабо PTEC оцветяване, което е било твърде ниско, за да бъде открито, особено при имуносвързани гломерулни заболявания, при които Igs са силно положителни в гломерулите и PTEC оцветяването може да бъде неволно, но изкуствено загубено. Трансцитозата на IgG от циркулацията от PTECs чрез Fc рецептора беше частично изключена, тъй като беше наблюдавано ясно оцветяване на IgG от RP215 в клетъчната мембрана и цитоплазмата. Тези констатации предполагат, че IgG, получен от PTEC, е подобен на други не-B-IgG и може да има уникални гликозилирани епитопи, които могат да бъдат специфично разпознати от RP215 вместо търговско анти-IgG антитяло (15). Констатацията, че само част от тубулните епителни клетки експресират IgG, може да се обясни с динамична експресия при различни клетъчни цикли, която е подобна на модела на експресия на IgA, получен от мезангиални клетки (18). Съвместното оцветяване на IgG с тубулни маркери (като аквапорин 1 и аквапорин 3) би било полезно за по-нататъшни изследвания за подобряване на резултатите от настоящото изследване.
Едноклетъчното РНК секвениране може ясно да покаже транскрипцията на специфичен ген в дадена клетка. Транскрипти на Ig веригата и V(D)J рекомбинация бяха открити в единични PTECs. Въпреки че бяха използвани само пет единични PTEC, процесът беше строг, тъй като бъбречната кора беше събрана далеч от тумора и всяка отделна клетка беше сортирана чрез поточна цитометрия с два PTEC-специфични маркерни гена, потвърдени отново с помощта на трети специфичен маркерен ген (LRP2) и замърсяването с B-клетки беше елиминирано. Резултатите разкриха, че PTECs не само представят IgG генни транскрипти, но и класическата V(D)J рекомбинация в променливата област като В клетки, като продуктивната V(D)J рекомбинация с V-D и D-J връзки (Фиг. 4), което показва, че PTECs имат потенциала да произвеждат IgG. В допълнение, по-консервативната V(D)J рекомбинация илюстрира, че PTECs присъстват с IgG генни транскрипти и V(D)J рекомбинация, които са подобни на други не-В клетки.
HK‑2, увековечена линия PTEC, е лесна за култивиране в големи количества. Настоящото проучване потвърди експресията на IgG протеин в култивирани HK-2 клетки; IgG се открива в HK-2 клетки както чрез имунофлуоресценция, така и чрез Western blotting. Ig 4, подклас на Ig, също беше открит при размер на лентата, съответстващ на предвиденото молекулно тегло. Масспектрометрията разкри, че протеинът, пречистен от клетъчния супернатант с помощта на протеин G, съдържа фрагменти от вариабилния регион на тежката верига на Ig и веригата Igκ, предоставяйки доказателство за секреция на IgG от PTECs. Транскрипцията на IgG в HK-2 клетки допълнително подкрепи IgG експресията в PTECs, а консервативната V(D)J рекомбинация с IGHV4-4/IGHD2-8/IGHJ5 в HK-2 клетки допълнително подкрепи наличието на IgG в HK-2 клетки, подобни към други не-В клетки.
Настоящото проучване също така изследва основния механизъм на производството на IgG в PTEC чрез изследване на транскрипцията на RAG1, RAG2 и AID в HK-2 клетки. Беше разкрито, че RAG1, RAG2 и AID са транскрибирани в HK-2 клетки. Освен това, RAG1, RAG2 или AID транскрипти преди това са били открити в множество други не-В клетки, като подоцити (19) и няколко ракови клетъчни линии (23). Тези резултати предполагат, че не-В клетките, включително PTEC, може да имат сходни механизми на синтез на Ig с В клетките. Въпреки това, дали AID и/или RAG1/2 са необходими гени за IgG, получени от PTEC, изисква допълнително изследване. В допълнение, фоликуларните хелперни CD4 Т клетки са важни за регулиране на В-клетъчната диференциация на зародишния център в плазмени клетки и подпомагане на производството на Igs (24). Нашите непубликувани данни разкриха, че не-B-Ig все още се откриват в мишки NOD-SCID с дефицит на Т и В клетки, което показва, че не-B-Ig не са изцяло зависими от Т хелперни клетки. Дали Т-хелперните клетки са необходими за PTECs да експресират IgG, изисква допълнителни изследвания.
TGF‑1 има ключова имуномодулираща роля в производството на Ig. Например, TGF‑1 индуцира превключване и секреция на клас IgA в стимулирани В клетки в далака на мишка (25) и В клетките на човешки сливици (26). McIntyre et al (27) показаха, че TGF‑1 селективно стимулира секрецията на IgG2b от липополизахарид-активирани В клетки, най-вероятно чрез индуциране на превключване на клас IgM към IgG2b. Duan et al (28) демонстрира, че TGF‑1 повишава експресията на IgA чрез регулиране на транскрипционния фактор Ets‑1 в епителните ракови клетки. Настоящото проучване демонстрира, че TGF‑1 повишава експресията на IgG в HK‑2 клетки. Като се има предвид, че само IgG се открива в HK-2 клетки, се предполага, че TGF-1 индуцира експресия на IgG независимо от превключването на Ig клас. Регулаторният механизъм на производството на IgG от TGF‑1 изисква допълнително изследване.
PTECs играят важна роля в тубулната интерстициална фиброза чрез EMT и TGF‑1 действа като основен профибротичен медиатор. В настоящото проучване добавянето на TGF-1 към култивирани HK-2 клетки повишава експресията на IgG, което показва, че IgG, получен от HK-2, може да бъде положително свързан с EMT. Предишни проучвания съобщават, че ракът-IgG е свързан с метастази и насърчава ЕМТ чрез намаляване на Е-кадхерина при слюнчен аденоиден кистичен карцином (29) и рак на белия дроб (30). Струва си да се проучи дали IgG, получен от PTEC, може да играе роля в ЕМТ на бъбречните тубули и интерстициална фиброза при болестни състояния, като исхемия/реперфузионно увреждане илихронично бъбречно заболяване.
В заключение, доколкото ни е известно, настоящото изследване беше първото, което демонстрира, че PTEC могат да експресират и секретират IgG, а TGF-1 може да регулира експресията на IgG в HK-2 клетки. Въпреки това, потенциалната роля на PTEC-получен IgG в тубулоинтерстициалната фиброза изисква допълнително изследване.

Ефекти на цистанхе: благоприятства бъбреците
Финансиране
Това проучване беше подкрепено от безвъзмездни средства от Националната фондация за природни науки на Китай (безвъзмездни средства № 82070736, 91642109 и 81870488), Фондацията за естествени науки на Хайнан (безвъзмездна помощ № 819QN355), Фондацията за научни изследвания на медицинския университет в Хайнан (грант № HYPY201926) и ключовите проекти за подкрепа на основната изследователска програма на Националната природонаучна фондация (грант № 91642206).
Наличие на данни и материали
Наборите от данни, използвани и/или анализирани по време на настоящото проучване, са достъпни от съответния автор при разумно искане.
Авторски принос
Като съответни автори, YW и XQ замислиха и проектираха изследването. ZD участва в дизайна на изследването, извърши хистологични и едноклетъчни експерименти, подготви проби за масова спектрометрия, анализира данни и написа ръкописа. ZJ участва в дизайна на изследването, повечето експерименти относно експресията на IgG в HK‑2 клетки и съответния анализ на данни. YG, JM, HD и YL извършиха експерименти с частични клетъчни линии. ZC и YP избраха подходящи случаи за експерименти с една клетка според клиничните характеристики. HY и ZS участваха в експерименти с една клетка. SW участва в имунохистохимично оцветяване, анализира данни за оцветяване на тъкани и състави и ревизира ръкописа. YW, ZD и ZJ потвърдиха автентичността на всички необработени данни. Всички автори прегледаха ръкописа и ревизираха данните. Всички автори прочетоха и одобриха окончателния ръкопис.
Етично одобрение и съгласие за участие
Настоящото проучване е в съответствие с принципите на Декларацията от Хелзинки и е одобрено от Комитета по медицинска етика на трета болница на Пекинския университет (одобрение № S2020121) и е проведено в съответствие с протокола. Всички донори доброволно дариха бъбречна кора и предоставиха писмено информирано съгласие преди даряването на бъбречната кора за изследването. Всички методи бяха проведени в съответствие със съответните насоки и разпоредби. Тези проби бяха строго анонимни. Човешки серум и PBMCs, използвани като положителни контроли при Western blotting или PCR с обратна транскрипция в настоящото изследване, са получени от кръвта на здрав доброволец, който е предоставил писмено информирано съгласие за вземане на проба.
Ефекти на цистанхе: благоприятства бъбреците
Препратки
1. Schlondorff DO: Преглед на факторите, допринасящи за патофизиологията на прогресивното бъбречно заболяване. Kidney Int 74: 860-866, 2008 г.
2. Donadio ME, Loiacono E, Peruzzi L, Amore A, Camilla R, Chile F, Vergano L, Boido A, Corrieri M, Bianciotto M,et ал: Toll-подобни рецептори, имунопротеазома и регулаторни Т клетки при деца с пурпура на Henoch-Schonlein и първична IgA нефропатия. Pediatr Nephrol 29: 1545-1551, 2014 г.
3. Breda PC, Wiech T, Meyer-Schwesinger C, Grahammer F, Huber T, Panzer U, Tiegs G и Neumann K: Бъбречните проксимални тубуларни епителни клетки упражняват имуномодулираща функция чрез стимулиране на възпалителни CD4 плюс Т клетъчни отговори. Am J Physiol Renal Physiol 317: F77-F89, 2019.
4. Liu BC, Tang TT, Lv LL и Lan HY: Увреждане на бъбречните тубули: Движеща сила към хронично бъбречно заболяване. Kidney Int 93: 568-579, 2018 г.
5. Kobayashi N, Suzuki Y, Tsuge T, Okumura K, Ra C и Tomino Y: FcRn-медиирана трансцитоза на имуноглобулин G в човешки бъбречни проксимални тубулни епителни клетки. Am J Physiol Renal Physiol 282: F358-F365, 2002.
6. Qiu X, Zhu X, Zhang L, Mao Y, Zhang J, Hao P, Li G, Lv P, Li Z, Sun X,et ал: Човешките епителни ракови заболявания секретират имуноглобулин g с неустановена специфичност за насърчаване на растежа и оцеляването на туморните клетки. Cancer Res 63: 6488-6495, 2003 г.
7. Zheng J, Huang J, Mao Y, Liu S, Sun X, Zhu X, Ma T, Zhang L, Ji J, Zhang Y,et ал: Генните транскрипти на имуноглобулин имат различни характеристики на рекомбинация на VHDJH в човешки епителни ракови клетки. J Biol Chem 284: 13610-13619, 2009 г.
8. Jiang D, Ge J, Liao Q, Ma J, Liu Y, Huang J, Wang C, Xu W, Zheng J, Shao W,et ал: IgG и IgA с потенциална активност за свързване на микроби се експресират от нормални епидермални клетки на човешка кожа. Int J Mol Sci 16: 2574-2590, 2015 г.
9. Zhu Z, Zhang M, Shao W, Wang P, Gong X, Ma J, Qiu X и Wang B: Имуноглобулин М, нова молекула от миокардни клетки на мишки. Int J Biochem Cell Biol 88: 172-180, 2017 г.
10. Niu N, Zhang J, Sun Y, Wang S, Sun Y, Korteweg C, Gao W и Gu J: Експресия и разпределение на имуноглобулин G и неговите рецептори в имуно-привилегировано място: Окото. Cell Mol Life Sci 68: 2481-2492, 2011 г.
11. Huang J, Sun X, Mao Y, Zhu X, Zhang P, Zhang L, Du J и Qiu XY: Експресия на имуноглобулинов ген с класическо V-(D)-J пренареждане в миши мозъчни неврони. Int J Biochem Cell Biol 40: 1604-1615, 2008 г.
12. Niu N, Zhang J, Guo Y, Zhao Y, Korteweg C и Gu J: Експресия и разпространение на имуноглобулин G и неговите рецептори в човешката нервна система. Int J Biochem Cell Biol 43: 556-563, 2011.
13. Li J, Korteweg C, Qiu Y, Luo J, Chen Z, Huang G, Li W и Gu J: Два модела на ултраструктурно разпределение на имуноглобулин G в човешката плацента и функционални последици. Biol Reprod 91: 128, 2014 г.
14. Huang J, Zhang L, Ma T, Zhang P и Qiu X: Експресия на имуноглобулинов ген с класическо V-(D)-J пренареждане в миши тестис и епидидим. J Histochem Cytochem 57: 339-349, 2009 г.
15. Tang J, Zhang J, Liu Y, Liao Q, Huang J, Geng Z, Xu W, Sheng Z, Lee G, Zhang Y,et ал: Клетките на белодробния плоскоклетъчен карцином експресират неканонично гликозилиран IgG, който активира интегрин-FAK сигнализация. Cancer Lett 430: 148-159, 2018 г.
16. Cui M, You L, Zheng B, Huang X, Liu QF, Huang J, Pan B, Qiu X, Liao Q и Zhao Y: Високата експресия на получен от рак гликозилиран имуноглобулин G предсказва лоша прогноза при дуктален аденокарцином на панкреаса. J Рак 11: 2213-2221, 2020 г
17. Cui M, Hu Y, Zheng B, Zhang S, Zhang X, Wang M, Qiu XY, Liao Q и Zhao YP: Имуноглобулин G, получен от рак: нов маркер за диференциална диагноза и прогнозиране на рецидив при паратироиден карцином. Clin Endocrinol (Oxf) 92: 461-467, 2020 г.
18. Deng H, Ma J, Jing Z, Deng Z, Liang Y, AL, Liu Y, Qiu X и Wang Y: Експресия на имуноглобулин А в човешки мезангиални клетки и неговите ефекти върху клетъчната апоптоза и адхезия. Mol Med Rep 17: 5272-5282, 2018 г.
19. Jing Z, Deng H, Ma J, Guo Y, Liang Y, Wu R, AL, Geng Z, Qiu X и Wang Y: Експресия на имуноглобулин G в човешки подоцити и неговата роля в клетъчната жизнеспособност и адхезия. Int J Mol Med 41: 3296-3306, 2018 г.
20. Van der Hauwaert C, Savary G, Gnemmi V, Glowacki F, Pottier N, Bouillez A, Maboudou P, Zini L, Leroy X, Cauffiez C,et ал: Изолиране и характеризиране на първичен проксимален тубуларен епителен клетъчен модел от човешки бъбрек чрез CD10/CD13 двойно маркиране. PLoS One 8: e66750, 2013 г.
