Таурин: източник и приложение за облекчаване на зрителната умора, част 2
Sep 27, 2023
3.2.1. Намаляване на увреждането на ретината от стрес: окисление, възпаление, апоптоза
Основната причина за зрителната умора е продължителната работа на окото или излагането на окото на силна светлина и кислород. Тази ситуация насърчава засилен очен метаболизъм, последван от увеличаване на пероксидите и следователно уязвимост към окислително увреждане, което започва да се появява [78]. Текущи проучвания показват, че един от най-съществените защитни ефекти на таурина върху клетките е неговият антиоксидантен ефект, медииран от три различни процеса: Първо, тауринът неутрализира неутрофилния оксидант хипохлориста киселина и полученият реакционен продукт, хлорамин таурат, също е по-добър при възпрепятстване на появата на възпаление [79,80]. Второ, тауринът намалява производството на супероксид чрез митохондриалния метаболизъм [81,82]. Трето, ROS, произведени от клетъчния метаболизъм или външни стимули от околната среда, са склонни да атакуват антиоксидантните ензими, което води до повишено окислително увреждане [82,83], докато тауринът може ефективно да защити тези антиоксидантни ензими от ROS атака, като по този начин противодейства на оксидативния стрес [33,84]. Добре известно е, че излагането на светлина има тенденция да води до увреждане на ретината от стрес и увреждане или загуба на фоторецептори и хранителните добавки с таурин могат да повишат концентрацията на таурин в ретината, която се намалява от излагане на светлина, да намали индуцираното от излагане на светлина свръхпроизводство на MDA в ретината и да увеличи активност на ретинална супероксид дисмутаза (SOD) и глутатион пероксидаза (GSH-Px) в ретината.
Cistanche може да действа като средство против умора и подобрител на издръжливостта, а експериментални проучвания показват, че отварата от Cistanche tubulosa може ефективно да защити чернодробните хепатоцити и ендотелните клетки, увредени при носещи тежести плуващи мишки, да регулира експресията на NOS3 и да стимулира чернодробния гликоген синтез, като по този начин упражнява ефикасност против умора. Богатият на фенилетаноидни гликозиди екстракт от Cistanche tubulosa може значително да намали нивата на серумната креатин киназа, лактат дехидрогеназа и лактат и да повиши нивата на хемоглобина (HB) и глюкозата при ICR мишки и това може да играе роля против умората чрез намаляване на мускулните увреждания и забавяне на обогатяването на млечна киселина за съхранение на енергия при мишки. Таблетките Compound Cistanche Tubulosa значително удължават времето за плуване с натоварване, повишават чернодробния гликогенов резерв и намаляват нивото на серумната урея след тренировка при мишки, показвайки своя ефект против умора. Отварата от Cistanchis може да подобри издръжливостта и да ускори премахването на умората при трениращи мишки, а също така може да намали повишаването на серумната креатин киназа след физическо натоварване и да поддържа ултраструктурата на скелетните мускули на мишки нормална след тренировка, което показва, че има ефектите за повишаване на физическата сила и против умора. Cistanchis също значително удължава времето за оцеляване на отровени с нитрити мишки и повишава толерантността към хипоксия и умора.

Кликнете върху причините за умората
【За повече информация:george.deng@wecistanche.com / WhatsApp:8613632399501】
В същото време тауринът също инхибира експресията на каспаза-1 в апоптотичния сигнален път на фоторецепторните клетки, което предполага, че хранителният таурин може да намали индуцираното от фотохимичен стрес увреждане на ретината чрез медииране на ретиналните антиоксидантни и антиапоптотични механизми, което също предполага, че тауринът има незаменима и важна физиологична роля в структурното и функционално развитие на ретината [85]. В проучване на Diego et al. [86], отново беше потвърдено, че тауринът е основно хранително вещество за поддържане на редовна физиологична активност на клетките на ретината, особено при наличие на индуцирано от светлина увреждане на фоторецепторите, и че ретината има по-високи изисквания за таурин . Нещо повече, тауринът значително подобрява нивата на таурин и преживяемостта на фоторецепторите при плъхове с дистрофия на ретината, намалява освобождаването на провъзпалителни фактори и увреждането от оксидативен стрес в ретината и ефективно поправя и намалява увреждането на RPE клетките [87]. Това предполага, че тауринът може да намали увреждането на функцията на ретината чрез противовъзпалителни и антиоксидантни пътища [88]. В допълнение, тауринът може също така да предотврати морфологичните промени на ретината и зрителния нерв чрез намаляване на пътя на оксидативния стрес на ретината и инхибиране на ендотелин-1 (мощен вазоконстриктор, участващ в глаукоматозна съдова дисрегулация на ретината и оксидативен стрес)-индуцирана апоптоза на клетките на ретината [89] .
Проучванията показват, че зрителната функция на окото намалява с възрастта. Увреждането на ретината при някои животински модели на стареене също може да бъде тясно свързано с дефицита на таурин [90]. Wang и др. използва целева метаболомика, за да анализира и сравни метаболитите в очите на 6-седмични C57 BL6/J млади мишки с тези на 73-седмични мишки. Резултатите от анализа показват, че стареещите мишки имат намалени електроретинограмни отговори и намален брой фоторецептори в сравнение с млади мишки и се наблюдава нарушен метаболизъм на таурин [91]. In vivo и ex vivo експериментални проучвания показват, че тауринът подобрява увреждането на AMD чрез намаляване на апоптотичния път на ретината [92].
Горните проучвания показват, че тауринът има жизненоважна роля за поддържане на нормални зрителни и фоторецепторни функции. Тауринът може ефективно да подобри уврежданията от стрес, особено уврежданията от оксидативен стрес, възникващи в ретината. В допълнение, тауринът може също да играе роля в защитата на функцията на ретината от увреждане на стреса чрез противовъзпалителни и антиапоптотични ефекти, като по този начин облекчава зрителната умора.
3.2.2. Намаляване на екситотоксичното увреждане на ретината и осигуряване на невропротекция
Биполярните клетки, фоторецепторите и ганглиозните клетки на окото съдържат високи концентрации на глутамат, важен невротрансмитер, който, когато е претоварен, предизвиква ексцитотоксичност и апоптотично сигнализиране, което води до дисфункция на ретината [93]. Освен това, екситотоксичното увреждане на ретината също е в основата на загуба на зрителна функция [94,95]. Това възбуждащо токсично увреждане на ретината също включва свръхстимулация на глутаматните рецептори, особено подтипа на N-метил-D-аспарагинова киселина (NMDA) на глутаматните рецептори, което причинява входящ поток на калций и нарушава вътреклетъчната екологична хомеостаза, задействайки проапоптотични пътища [96]. Следователно, индуцирането на увреждане на ретината при плъхове чрез интравитреално инжектиране на NMDA е използвано като представителен животински модел на ексцитотоксично увреждане на ретината [97]. За разлика от това, доказано е, че тауринът осигурява неврозащита чрез път, който намалява вътреклетъчния свободен калций, като по този начин проявява резистентност към индуцирана от глутамат екситотоксичност [98]. Освен това тауринът е потенциален невромодулатор на предаването на глутамат [99]. Тауринът може ефективно да инхибира индуцираната от глутамат екситотоксичност и да предпази функцията на ретината от увреждане чрез дългосрочна хранителна добавка на тауриновия път [100]. В допълнение, експериментални данни показват, че тауринът е ефективен при пречистването на широк спектър от реактивни кислородни и азотни видове при различни физиологични концентрации [101]. Следователно, редуциращият ефект на хранителния таурин върху оксидативния стрес на ретината може да се дължи не само на способността му да възстановява и укрепва антиоксидантната защита на ретината, но и на способността на таурина да засилва разрушаването на свободните радикали и по този начин да предотвратява индуцираното от NMDA увреждане на ретината чрез намаляване на ретината. оксидативен стрес [102].
Плъхът на Royal College of Surgeons (RCS) е често използван животински модел за пигментен ретинит. Основните прояви на този плъх са нарушена фагоцитоза на RPE клетки [103–106] с прогресивна фоторецепторна дегенерация [107–110], повишена пролиферация на ретинални глиални клетки, променен ретрограден аксонален транспорт на ганглийни клетки на ретината (RGC) и загуба на RGC [111–113]. Едно проучване твърди, че първият признак на дегенерация на ретината при RCS плъхове е значително намаляване на нивата на таурин. Данните показват, че ретиналния таурин се доставя от RPE клетки и клетки на Мюлер [91,114]. В същото време изчерпването на таурин също увеличава пролиферацията на глиалните клетки на ретината и нарушава фагоцитозата на RPE клетките [35]. Това предполага, че тауринът е незаменим за поддържане на нормална функция на RPE и че подобряването на вредното увреждане на RPE клетките чрез добавяне на таурин може да бъде потенциална стратегия за диетична интервенция. Наистина, добавянето на 0,2 М таурин към питейната вода на RCS плъхове разкри значително намаляване на броя на микроглиите във външния слой на ретината, ефективно намаляване на съдържанието на глиален фибриларен кисел протеин (GFAP) в клетките на Мюлер, значително намаляване на оксидативен стрес във външното и вътрешното ядро на ретината, както и подобрено поддържане на синаптичните връзки на ретината. Това предполага, че диетичният таурин може да действа за подобряване на увреждането на фоторецепторите и увеличаване на електрическите реакции на ретината чрез медииране на различни невропротективни механизми [88].
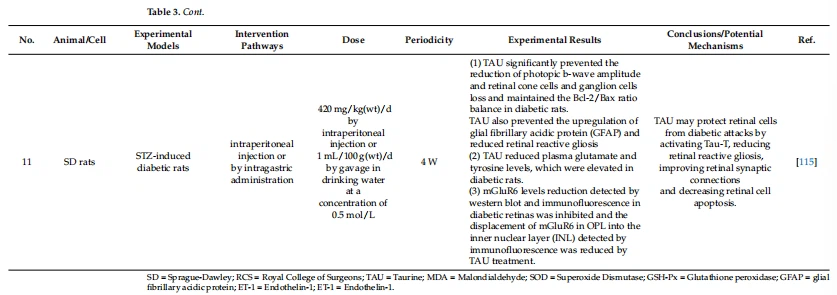
В допълнение, тауринът може също да играе роля за подобряване на увреждането на ретината чрез подобряване на синаптичните връзки на ретината, поддържане на баланса на съотношението Bcl-2/Bax (което определя апоптозата) и намаляване на реактивната глиална пролиферация в клетките на Мюлер на ретината [115]. ]. В заключение, горните проучвания показват, че тауринът може да играе роля в подобряването на нормалната функция и морфологията на увредените RPE, RGC и фоторецепторите чрез намаляване на възбудителната токсичност в ретината, както и различни невропротективни механизми, като по този начин облекчава зрителната умора.
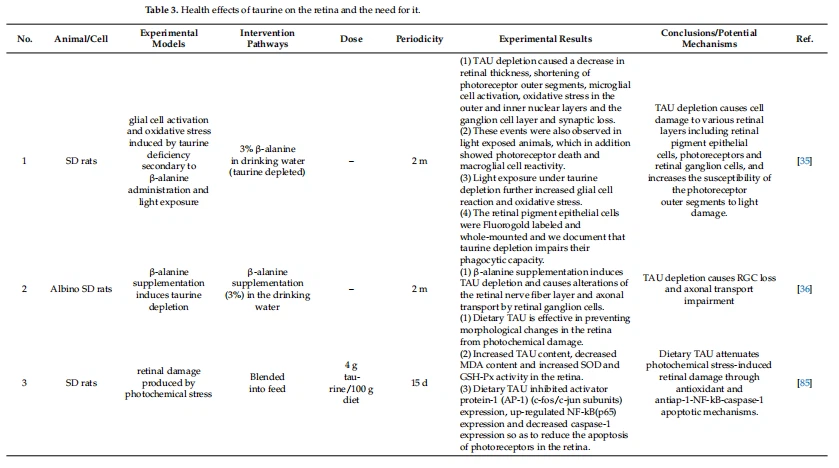
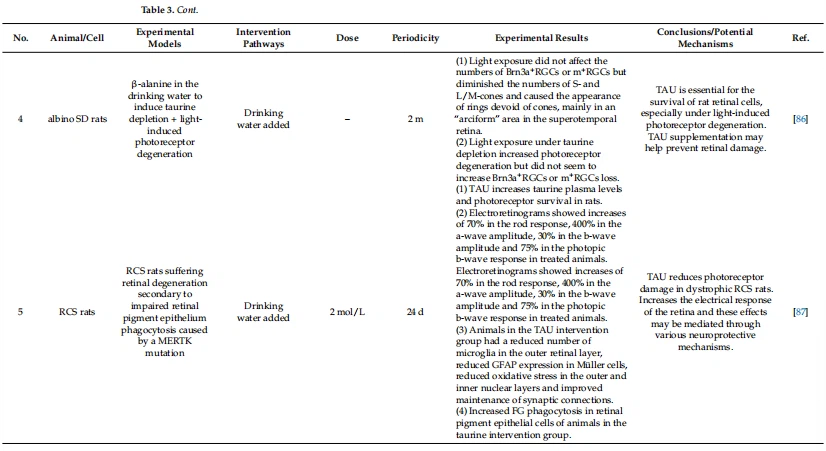
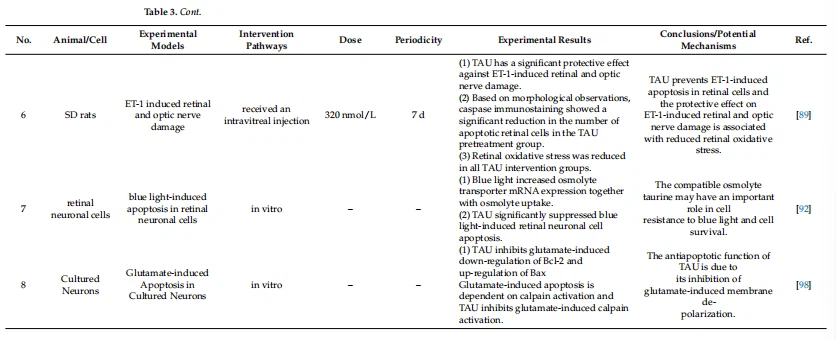
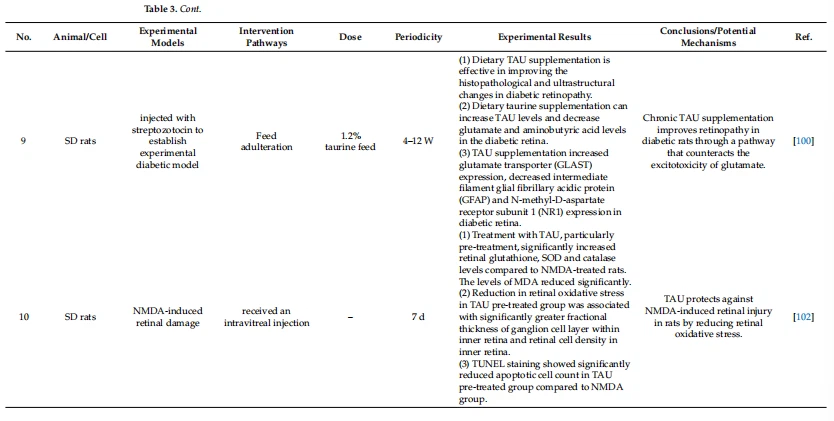
Здравните ефекти на таурина върху ретината и необходимостта от него са описани подробно в таблица 3.
4. Изводи
Зрителната умора се причинява главно от спад или увреждане на функцията на ретината, особено когато продължителното използване на очите води до прекомерно натрупване на метаболитни отпадъци в окото, които не могат да бъдат изчистени, причинявайки различни наранявания от стрес. Тауринът се счита за основен хранителен елемент за функцията и оцеляването на фоторецепторите на ретината, RGCs и RPE клетките [36,87,116] и неговото изчерпване увеличава чувствителността на ретината към увреждане на излагането на светлина [35,36] и също така увеличава пролиферацията на глиални клетки и оксидативен стрес в ретината, нарушавайки нормалния фагоцитен капацитет на RPE [35]. В допълнение, множество клинични [117,118] и проучвания върху животни [33,119,120] показват, че изчерпването на таурин може да предизвика нарушена функция на ретината и дори патологично заболяване на очите. Добавянето на таурин е ефективно за подобряване на фоторецепторната дегенерация на ретината [88,121] и увреждането на ретината и зрителния нерв [33,90]. Въпреки това, настоящите изследвания върху защитния ефект на таурина върху ретината са фокусирани главно върху неговия антиоксидантен ефект. Изследванията върху неантиоксидантните пътища за подобряване на увреждането на ретината може да са важна посока за бъдещи изследвания. В допълнение, тауринът, като естествена аминокиселина, има висок профил на безопасност и е разрешено да се добавя към функционални напитки и други хранителни продукти в много страни. Поради важната защитна роля на таурина в ретината и неговата висока хранителна безопасност, приложението му при разработването на функционални храни за облекчаване на зрителната умора е много обещаващо. Следователно, при бъдещото разработване на функционални храни за облекчаване на зрителната умора, изследванията върху синергичния ефект на таурина в комбинация с други функционални съставки могат да бъдат подобрени, за да се изясни оптималното съотношение на формулировката между таурин и други функционални съставки, за да се увеличи максимално зрителната умора релефна функция на продуктите.
Рационалният подбор и изследване на екстракцията на суровините е едно от необходимите и ефективни средства за максимизиране на тяхната функция във формулировката. Следователно, тази статия систематично прави преглед на пътищата на ендогенния синтез и екзогенното диетично разпределение на таурин в човешкото тяло, както и неговото извличане и промишлено производство. Методите за химичен синтез и биоферментация са подходящи за промишленото производство на таурин с висока чистота, но всеки има определени недостатъци. Методите за екстракция, от друга страна, не са подходящи за промишлено производство на таурин с по-висока чистота, но са от голямо значение за разработването на функционални хранителни съставки. Това е така, защото тялото получава таурин чрез екзогенни средства, като консумира определена доза богата на таурин храна, която след това се смила, абсорбира и метаболизира от тялото, за да попълни тялото наистина с необходимото количество таурин. Този процес подчертава не само нивото на съдържание на таурин в храната, но и връзката между дозата и ефикасността. Изборът на подходящи суровини и методи за екстракция може ефективно да повиши съдържанието на таурин в суровините и да намали дозировката на самите суровини, което подобрява използването на суровините, обогатява гамата от налични суровини за формулиране на функционални храни за облекчаване на зрителната умора, подобрява новостта на продуктовите формулировки и също така улеснява изследователите да диверсифицират дизайна на функционални лекарствени форми за храни според характеристиките на населението. Също така е много подходящ за изследване и разработване на нови хранителни съставки, както и функционални хранителни съставки.
В заключение, тауринът има важен защитен ефект върху функцията на ретината, главно поради своите антиоксидантни и невропротективни ефекти, и е от съществено значение за функцията и оцеляването на фоторецепторите на ретината, RGC и RPE клетките. Въпреки това, тъй като количеството таурин, синтезирано от човешкото тяло, не е достатъчно, за да отговори на здравните нужди на тялото, той трябва да бъде набавен чрез хранителни добавки. Това предполага важността и необходимостта от хранителни добавки с таурин за насърчаване на здравето на очите. Ето защо тази статия предоставя систематичен преглед на източниците на таурин, включително ендогенните метаболитни и екзогенни диетични пътища, както и подробен преглед на разпространението и производството на екзогенен таурин. Физиологичните механизми, лежащи в основата на производството на зрителна умора, са обобщени и е прегледан напредъкът на изследванията на таурина за облекчаване на зрителната умора, включително безопасността на консумация и механизма на действие при облекчаване на зрителната умора, за да се предостави известна справка и вдъхновение за разработването и приложението таурин във функционални храни за облекчаване на зрителната умора.
Авторски принос:Концептуализация, HD; методика, HD; софтуер, JG; валидиране, WS; формален анализ, HD; разследване, HD; ресурси, WS; куриране на данни, JG; писане—изготвяне на оригинална чернова, HD и WS; писане - преглед и редактиране, WY; визуализация, HD; надзор, WY; администрация на проекта, WY; придобиване на финансиране, WY Всички автори са прочели и са съгласни с публикуваната версия на ръкописа.
Финансиране:Това изследване е финансирано от Националната природонаучна фондация на Китай, безвъзмездна помощ номер 32172244, и академичните изследователски проекти на Пекинския съюзен университет, безвъзмездни номера XP202006 и ZK70202004.
Изявление на институционалния съвет за преглед:Не е приложимо.
Декларация за информирано съгласие:Не е приложимо.
Декларация за наличност на данни:Не е приложимо.
Благодарности:Авторите биха искали да благодарят на Wenjie Yan за неговите насоки и финансова помощ.
Конфликти на интереси:Авторите декларират липса на конфликт на интереси.

Препратки
1. Ле, З.; Антонов, Е.; Мао, Q.; Петров, В.; Wang, Y.; Wang, W.; Шевколенко, М.; Dong, W. Очила против умора, базирани на микропризми за предотвратяване на напрежението на очите. Сензори 2022, 22, 1933. [CrossRef] [PubMed]
2. Джън, Ф.; Hou, F.; Чен, Р.; Mei, J.; Хуанг, П.; Чен, Б.; Wang, Y. Изследване на връзката между субективните симптоми на зрителната умора и зрителните функции. Преден. Neurosci. 2021, 15, 686740. [CrossRef] [PubMed]
3. Вилела, MA; Pellanda, LC; Fassa, AG; Castagno, VD „Разпространение на астенопия при деца: систематичен преглед с мета-анализ. J. Pediatr. 2015, 91, 320–325. [CrossRef] [PubMed]
4. Тода, И.; Фуджишима, Х.; Tsubota, K. Очната умора е основният симптом на сухото око. Акта Офталмол. 1993, 71, 347–352. [CrossRef] [PubMed]
5. Шепърд, Алабама; Wolffsohn, JS Дигитално напрежение на очите: разпространение, измерване и подобряване. BMJ Open Ophthalmol. 2018, 3, e000146. [CrossRef]
6. Абди, С.; Ридберг, А. Астенопия при ученици, ортоптични и офталмологични находки и лечение. Док. офталмол. 2005, 111, 65–72. [CrossRef]
7. Портело, JK; Rosenfield, M.; Бабабекова, Ю.; Естрада, JM; Леон, А. Свързани с компютър зрителни симптоми при офис работници. Офталмологичен физиол. Избирам. 2012, 32, 375–382. [CrossRef]
8. Реди, SC; Ниска, CK; Lim, YP; Ниска, LL; Мардина, Ф.; Нурсалеха, MP Синдром на компютърното зрение: Проучване на знанията и практиките при студенти. Непал. J. Ophthalmol. 2013, 5, 161–168. [CrossRef]
9. Фан, Б.; Zhang, C.; Chi, J.; Liang, Y.; Бао, X.; Cong, Y.; Ю, Б.; Ли, X.; Li, G.-Y. Молекулярният механизъм на светлинно нараняване на ретината, фокусирано върху увреждане от светлина с къса дължина на вълната. Oxidative Med. Cell Longev. 2022, 2022, 8482149. [CrossRef]
10. Аяки, М.; Кузе, М.; Кондо, М.; Цубота, К.; Negishi, K. Асоциация между дебелината на слоя на нервните влакна на ретината и умората на очите. BioMed Res. Вътр. 2019, 2019, 3014567-8. [CrossRef]
11. Янг, С.; Zhou, J.; Li, D. Функции и заболявания на пигментния епител на ретината. Преден. Pharmacol. 2021, 12, 727870. [CrossRef] [PubMed]
12. Упадхяй, М.; Milliner, C.; Бел, бакалавърска степен; Bonilha, VL Оксидативен стрес в ретината и пигментния епител на ретината (RPE): Роля на стареенето и DJ-1. Redox Biol. 2020, 37, 101623. [CrossRef] [PubMed]
13. Субраманиам, доктор по медицина; Айер, М.; Nair, AP; Венкатесан, Д.; Mathavan, S.; Eruppakotte, N.; Kizhakkillach, S.; Chandran, MK; Рой, А.; Гопалакришнан, AV; et al. Оксидативен стрес и митохондриален трансфер: Ново измерение към очните заболявания. Genes Dis. 2022, 9, 610–637. [CrossRef] [PubMed]
14. Руис-Пастор, MJ; Куцир, О.; Лакс, П.; Cuenca, N. Намаляването на DHA и други мастни киселини корелира с дегенерацията на фоторецепторите при пигментния ретинит. Exp. Eye Res. 2021, 209, 108667. [CrossRef]
15. Сузумура, А.; Терао, Р.; Kaneko, H. Защитни ефекти и молекулярно сигнализиране на n-3 мастни киселини върху оксидативен стрес и възпаление при заболявания на ретината. Антиоксиданти 2020, 9, 920. [CrossRef]
16. Ким, MJ; Ким, DH; Kwak, HS; Ю, И.-С.; Хм, МОЯТ защитен ефект на екстракти от цветя на Chrysanthemum boreale срещу A2E-индуцирано увреждане на ретината в ARPE{4}} клетка. Антиоксиданти 2022, 11, 669. [CrossRef]
17. Ди Пиердоменико, Дж.; Гарсия-Аюсо, Д.; Пинила, И.; Куенка, Н.; Видал-Санс, М.; Agudo-Barriuso, М.; Villegas-Pérez, MP Ранни събития при дегенерация на ретината, причинена от мутация на родопсин или неизправност на пигментния епител: разлики и прилики. Преден. Невроанат. 2017, 11, 14. [CrossRef]
18. Куенка, Н.; Фернандес-Санчес, Л.; Campello, L.; Maneu, V.; Де ла Вила, П.; Лакс, П.; Pinilla, I. Клетъчни реакции след наранявания на ретината и терапевтични подходи за невродегенеративни заболявания. Прог. ретина. Eye Res. 2014, 43, 17–75. [CrossRef]
19. de Hoz, R.; Рохас, Б.; Рамирес, AI; Салазар, JJ; Gallego, BI; Тривиньо, А.; Ramírez, JM Макроглиални реакции на ретината при здраве и болести. BioMed Res. Вътр. 2016, 2016, 2954721. [CrossRef]
20. Лю, Б.; Хънтър, DJ; Смит, АА; Чен, С.; Helms, JA Капацитетът на стволови клетки, получени от нервния гребен, за възстановяване на очите. Вродени дефекти Res. Част C Embryo Today Rev. 2014, 102, 299–308. [CrossRef]
21. Пенг, Л.; Парпура, В.; Verkhratsky, A. РЕДАКЦИЯ Невроглията като централен елемент на неврологичните заболявания: недооценена цел за терапевтична интервенция. Curr. Неврофармакол. 2014, 12, 303–307. [CrossRef] [PubMed]
22. Джан, X.; Ченг, М.; Chintala, SK Медиирана от каинова киселина регулация на матриксната металопротеиназа-9 насърчава дегенерацията на ретината. разследване. офталмол. Vis. Sci. 2004, 45, 2374–2383. [CrossRef] [PubMed]
23. Roche, SL; Ruiz-Lopez, AM; Moloney, JN; Бърн, AM; Cotter, TG Микроглиално-индуцирана клетъчна глиоза на Мюлер се отслабва от прогестерон в миши модел на ретинит пигментоза. Glia 2018, 66, 295–310. [CrossRef] [PubMed]
24. Ди Пиердоменико, Дж.; Гарсия-Аюсо, Д.; Agudo-Barriuso, М.; Видал-Санс, М.; Villegas-Perez, MP Роля на микроглиалните клетки в дегенерацията на фоторецепторите. Невронна регенерация. Рез. 2019, 14, 1186–1190. [CrossRef]
25. Калониатис, М.; Napper, GA Ретинални неврохимични промени след прилагане на глутамат като метаболитен субстрат. Clin. Exp. Optom. 2002, 85, 27–36. [CrossRef]
26. Барабас, П.; Ковач, И.; Kardos, J.; Schousboe, A. Екзогенният глутамат и тауринът упражняват различни действия върху индуцираното от светлина освобождаване на две ендогенни аминокиселини в изолирана ретина на плъх. J. Neurosci. Рез. 2003, 73, 731–736. [CrossRef]
27. Payet, O.; Maurin, L.; Bonne, C.; Muller, A. Hypoxia стимулира усвояването на глутамат в клетките на ретината на цели плъхове in vitro. Neurosci. Lett. 2004, 356, 148–150. [CrossRef]
28. Джао, Л.; Zabel, MK; Уанг, X.; Ма, В.; Шах, П.; Фарис, RN; Qian, H.; Паркхърст, CN; Gan, WB; Wong, WT Микроглиалната фагоцитоза на живи фоторецептори допринася за наследената ретина. EMBO Mol. Med. 2015, 7, 1179–1197. [CrossRef]
29. Чен, Ф.; Ми, М.; Джан, К.; Wei, N.; Чен, К.; Xu, H.; Юан, Дж.; Zhou, Y.; Lang, H.; Ю, X.; et al. Тауринът буферира глутаматната хомеостаза в клетките на ретината in vitro при хипоксични условия. Ophthalmic Res. 2010, 44, 105–112. [CrossRef]
30. Рипс, Х.; Shen, W. Преглед: Таурин: „много важна“ аминокиселина. Mol. Vis. 2012, 18, 2673–2686.
31. Wójcik, OP; Koenig, KL; Zeleniuch-Jacquotte, A.; Коста, М.; Chen, Y. Потенциалните защитни ефекти на таурина върху коронарната болест на сърцето. Атеросклероза 2010, 208, 19–25. [CrossRef] [PubMed]
32. Група на EFSA по добавките и продуктите или веществата, използвани в храните за животни (FEEDAP). Научно становище относно безопасността и ефикасността на таурина като фуражна добавка за всички животински видове. EFSA J. 2012, 10, 2736.
33. Фрогер, Н.; Кадети, Л.; Lorach, H.; Martins, J.; Bemelmans, A.; Дъбъс, Е.; Degardin, J.; Болка, Д.; Форстър, В.; Chicaud, L.; et al. Тауринът осигурява неврозащита срещу дегенерация на ганглийните клетки на ретината. PLoS ONE 2012, 7, e42017. [CrossRef]
34. Хейс, KC; Грижа, Р.; Schmidt, SY Дегенерация на ретината, свързана с дефицит на таурин при котка. Science 1976, 188, 949–953. [CrossRef] [PubMed]
35. Мартинес-Вакас, А.; Ди Пиердоменико, Дж.; Валиенте-Сориано, FJ; Видал-Санс, М.; Picaud, S.; Villegas-Pérez, MP; García-Ayuso, D. Активиране на глиални клетки и оксидативен стрес при дегенерация на ретината, предизвикана от -аланин, причинено от изчерпване на таурин и излагане на светлина. Вътр. J. Mol. Sci. 2021, 23, 346. [CrossRef] [PubMed]
36. Хадж-Саид, В.; Froger, N.; Ивкович, И.; Хименес-Лопес, М.; Дъбюс, Е.; Dégardin-Chicaud, J.; Simonutti, M.; Quénol, C.; Neveux, N.; Villegas-Pérez, MP; et al. Количествен и топографски анализ на загубите на конусовидни фоторецептори и ганглиозни клетки на ретината при изчерпване на таурин. разследване. офталмол. Vis. Sci. 2016, 57, 4692–4703. [CrossRef]
37. Зенг, К.; Xu, H.; Ми, М.; Джан, К.; Джан, Й.; Чен, К.; Чен, Ф.; Zhu, J.; Yu, X. Хранителната добавка с таурин предотвратява глиалните промени в ретината на диабетни плъхове. Neurochem. Рез. 2009, 34, 244–254. [CrossRef]
38. Ву, Д.; Песен, Л.; Zhu, C.; Джан, X.; Guo, H.; Yang, C. Разтворимост на таурин и приложението му за подобряване на процеса на кристализация. J. Mol. Liq. 2017, 241, 326–333. [CrossRef]
39. Wang, LW Ефект на добавката на таурин върху атлетичните постижения на спортистите. Food Res. Dev. 2022, 43, 231–232.
40. Теватия, Р.; Алън, Дж.; Rudrappa, D.; Уайт, Д.; Clemente, TE; Cerutti, H.; Демирел, Ю.; Blum, P. Биосинтетичният път на таурин на микроводорасли. Algal Res. 2015, 9, 21–26. [CrossRef]
41. Витвицки, В.; Гарг, SK; Banerjee, R. Биосинтеза на таурин от неврони и астроцити. J. Biol. Chem. 2011, 286, 32002–32010. [CrossRef] [PubMed]
42. Lund, EK Ползи за здравето от морски дарове; Само мастните киселини ли са? Food Chem. 2013, 140, 413–420. [CrossRef]
43. Wang, F. Извличане, изолиране и пречистване на таурин от Zea mays. Магистърска теза, Nanjing Agricultural University, Nanjing, Китай, 2014 г.
44. Сие, З.; Яо, Й.; Лиу, Б.; Чен, X.; Fang, T. Изследователски напредък на методите за извличане и откриване на таурин. Food Ind. Sci. техн. 2019, 40, 323–331. [CrossRef]
45. Хуанг, X.; Hou, S.; Li, G.; Кай, Дания; Su, Z. Преглед на таурина като активна съставка в китайската медицина. Брадичка. Народна. Средства за защита 2005, 9, 64–65. [CrossRef]
46. Учида, М.; Kurushima, H.; Ишихара, К.; Мурата, Й.; Тойота, К.; Ишида, Н.; Niwa, K.; Араки, Т. Характеризиране на ферментирал сос от морски водорасли, приготвен от нори (Pyropia yezoensis). J. Biosci. Bioeng. 2017, 123, 327–332. [CrossRef]
47. Лв, Р.; Чен, Р.; Чен, X.; Fang, T. Напредък на изследванията върху извличането на естествен таурин от карантии от охлюви. Анхуей Агрик. Бик. 2019, 25, 14–16+83. [CrossRef]
48. Джан, MD; Зан, Н.; Li, SR; Zhou, YJ Напредъкът на изследванията върху технологията за обработка и откриване на таурин и неговото приложение. Agric. произв. Процес. 2019, 19, 68–72+74. [CrossRef]
49. Wang, C.; Li, J.; Cao, Y.; Huang, J.; Лин, Х.; Джао, Т.; Лиу, Л.; Шен, П.; McClements, DJ; Чен, Дж.; et al. Екстракция и характеризиране на пектинови полизахариди от кори на Choerospondias axillaris: Сравнение на методи за екстракция с гореща вода и ултразвук. Food Chem. 2023, 401, 134156. [CrossRef]
50. Vinatoru, M. Ултразвуково подпомогнато извличане (ОАЕ) на природни продукти някои насоки за добра практика и докладване. Ултразвук. Sonochem. 2015, 25, 94–95. [CrossRef]
51. Мартин-Гарсия, Б.; Pasini, F.; Верардо, В.; Диас-Де-Серио, Е.; Tylewicz, U.; Gómez-Caravaca, AM; Caboni, MF Оптимизиране на Sonotrode ултразвукова-подпомогната екстракция на проантоцианидини от Brewers' отработени зърна. Антиоксиданти 2019, 8, 282. [CrossRef]
52. Джи, Л.; Лиу, Т.; Wang, Y.; Ли, X.; Li, H.; Jiang, X.; Sun, Y. Изследване на процеса на екстракция на таурин в миди kui. China Agric. Sci. техн. нея. 2017, 19, 132–138. [CrossRef]
53. Jiang, X. Изследване на процеса на извличане на таурин от изумрудена мида. Food Sci. техн. 2006, 1, 62–64.
54. Qian, A.; Ян, С.; Ю, Й.; Lin, X. Проучване на методи за предварителна обработка за определяне на таурин в морски дарове. Китай Агрон. Бик. 2006, 5, 94–97.
55. Qian, Q. Напредък в изследванията върху извличането на активни вещества като таурин, полизахариди и пептиди от морски организми. Food Ind. Sci. техн. 2013, 34, 383–387. [CrossRef]
56. Ma, C.-C.; Бътлър, Д.; Милиган, В.; Hammann, BA; Luo, H.; Бразил, JF; Лиу, Д.; Чаудхари, RV; Субраманиам, Б. Непрекъснат процес за производство на таурин от моноетаноламин. инж. инж. Chem. Рез. 2020, 59, 13007–13015. [CrossRef]
58. Буличев, Е.Ю.; Rubanyak, NY Търговски синтез на 2-аминоетансулфонова киселина (таурин). Pharm. Chem. J. 2013, 46, 740–741. [CrossRef]
58. Yeh, S.; Deng, J.; Liu, Q.-S.; Deng, B. Напредъкът на изследването на храненето с таурин и приложението му в котешка храна. Guangdong Anim. съпруг ветеринарен лекар Sci. техн. 2021, 46, 21–26+43.
59. Joo, Y.-C.; Ко, YJ; Вие, SK; Шин, SK; Hyeon, JE; Musaad, AS; Han, SO Създаване на нов път в Corynebacterium glutamicum за производството на таурин като хранителна добавка. J. Agric. Food Chem. 2018, 66, 13454–13463. [CrossRef]
60. Джени. Високоволтово импулсно електрическо ензимно разграждане на месо от миди за получаване на таурин. Магистърска теза, Университет Джилин, Чанчун, Китай, 2020 г. [CrossRef]
61. Лю, X.; Хуанг, Л.; Бай, Й.; Лиу, X.; Li, S. Извличане на биоцинк и таурин от месото на Pinctada martensii. J. Food Sci. 2020 г., 85, 1125–1131. [CrossRef]

62. Гуо, З.; Ge, X.; Хан, Л.; Янг, Л.; Yu, Q. Ултразвукова екстракция и пречистване на таурин от говежди черен дроб. J. Food Compos. анален 2020, 90. предпубл. [CrossRef]
63. Уанг, Ф.; Guo, X.-Y.; Zhang, D.-N.; Wu, Y.; Wu, T.; Чен, З.-Г. Ултразвукова екстракция и пречистване на таурин от червените водорасли Porphyra yezoensis. Ултразвук. Sonochem. 2015, 24, 36–42. [CrossRef] [PubMed]
64. Ху, К.-Л.; Gao, R.-C.; Янг, Ф.-С.; Liu, W.-T.; Янг, J.-F. Изследване на процеса на приготвяне на таурин чрез ензимно смилане на кипяща течност от филипинска мида. J. Light Ind. 2018, 33, 26–33.
65. Лиу, Й.; Джан, З.; Тонг, Х.; Сън, К.; Song, X. Оптимизиране на условията на ензимния процес на екстракция на таурин от стриди чрез неутрална протеаза, използвайки методологията на повърхността на реакцията. Food Sci. 2011, 32, 25–28.
66. Чен, Дж.; Ouyang, J.; Лиу, З.; Джоу, Л.; Хуанг, Х.; Ying, X. Напредък на изследванията върху процеса на синтез и пречистване на кристализация на таурин. мод. Chem. 2021, 41, 57–62. [CrossRef]
67. Научен комитет по храните (SCF). Становище относно кофеина, таурина и D-глюкуроно- -лактона като съставки на така наречените „енергийни“ напитки; SCF: Брюксел, Белгия, 1999 г.; стр. 1–12.
68. Sanz-Serrano, J.; Vettorazzi, A.; Мурузабал, Д.; Azqueta, A.; de Cerain, AL In Vitro оценка на генотоксичността на функционални съставки: бетаин, холин и таурин. Храни 2021, 10, 339. [CrossRef]
69. Мензи, Дж.; Prentice, H.; Wu, J.-Y. Невропротективни механизми на таурина срещу исхемичен инсулт. Brain Sci. 2013, 3, 877–907. [CrossRef]
70. Джан, М.; Bi, LF; Fang, JH; Su, XL; Da, GL; Кувамори, Т.; Kagamimori, S. Благоприятни ефекти на таурина върху серумните липиди при пациенти с наднормено тегло или затлъстяване без диабет. Аминокиселини 2004, 26, 267–271. [CrossRef]
71. Мураками, С.; Кондо, Й.; Nagata, T. Ефекти от дългосрочно лечение с таурин при мишки, хранени с диета с високо съдържание на мазнини: Подобряване на метаболизма на холестерола и натрупване на съдови липиди от таурин. адв. Exp. Med. Biol. 2000, 483, 177–186.
72. Sturman, JA; Messing, JM Ефекти на високия диетичен таурин върху концентрациите на таурин в котешките тъкани и репродуктивната производителност. J. Nutr. 1992, 122, 82–88. [CrossRef]
73. Шао, А.; Hathcock, JN Оценка на риска за аминокиселините таурин, l-глутамин и l-аргинин. Регул. Токсикол. Pharmacol. 2008, 50, 376–399. [CrossRef]
74. Уанг, X.; Chen, Y. Проучване на оценката на безопасността на таурин, витамин Е и инозитол комплекс прах. Clin. Рез. Брадичка. Med. 2020, 12, 1–5.
75. Шу, З.; Джоу, X.; Zhao, P.; Zhao, F. Токсикологична оценка на безопасността на Qili таурин витаминна напитка. Beverage Ind. 2016, 19, 5–9.
76. Джао, К.; AI, F.; Zheng, L.; Чен, X.; Lin, J. Проучване на безопасността на богати на селен дрожди и формулирани продукти с таурин. Strait J. Предишна Med. 2019, 25, 47–49.
77. Geng, KJ; Liu, X. Безопасност и функционалност на комбинирани таблетки от млечни минерални соли и таурин. J. Food Saf. 2022, 2, 86–90. [CrossRef]
78. Дуан, Х.; Yan, WJ Напредъкът на изследванията върху суровините и техните ефикасни компоненти за функцията за облекчаване на зрителната умора. Food Ind. Sci. техн. 2022, 1–13. [CrossRef]
79. Ким, К.; Ча, Й.-Н. Таурин хлорамин, произведен от таурин при възпаление, осигурява противовъзпалителни и цитопротективни ефекти. Аминокиселини 2013, 46, 89–100. [CrossRef]
80. Марцинкевич, Й.; Грабовска, А.; Берета, Дж.; Stelmaszynska, T. Таурин хлорамин, продукт на активирани неутрофили, инхибира in vitro генерирането на азотен оксид и други възпалителни медиатори на макрофаги. J. Leukoc. Biol. 1995, 58, 667–674. [CrossRef] [PubMed]
81. Шафър, С.; Kim, HW Ефекти и механизми на таурина като терапевтичен агент. Biomol. Там. 2018, 26, 225–241. [CrossRef]
82. Jong, CJ; Azuma, J.; Schaffer, S. Механизъм, който е в основата на антиоксидантната активност на таурина: Предотвратяване на производството на митохондриален оксидант. Аминокиселини 2011, 42, 2223–2232. [CrossRef]
83. Нита, М.; Grzybowski, A. Ролята на реактивните кислородни видове и оксидативния стрес в патомеханизма на свързаните с възрастта очни заболявания и други патологии на предните и задните очни сегменти при възрастни. Оксид. Med. Cell Longev. 2016, 2016, 3164734. [CrossRef]
84. Гоше, Д.; Арно, Е.; Husson, Z.; Froger, N.; Дъбъс, Е.; Гондуен, П.; Dherbécourt, D.; Degardin, J.; Simonutti, M.; Фуке, С.; et al. Дефицитът на таурин уврежда невроните на ретината: конусовидни фоторецептори и ганглийни клетки на ретината. Аминокиселини 2012, 43, 1979–1993. [CrossRef] [PubMed]
85. Ю, X.; Чен, К.; Wei, N.; Джан, К.; Liu, J.; Mi, M. Диетичният таурин намалява увреждането на ретината, причинено от фотохимичен стрес чрез антиоксидантни и антиапоптотични механизми при плъхове Sprague-Dawley. механизми при плъхове Sprague-Dawley. бр. J. Nutr. 2007, 98, 711–719. [CrossRef] [PubMed]
86. Гарсия-Аюсо, Д.; Ди Пиердоменико, Дж.; Хадж-Саид, В.; Мари, М.; Agudo-Barriuso, М.; Видал-Санс, М.; Villegas-Pérez, MP Изчерпването на таурин причинява загуба на ipRGC и увеличава индуцираната от светлина дегенерация на фоторецепторите. разследване. офталмол. Vis. Sci. 2018, 59, 1396–1409. [CrossRef] [PubMed]
87. Мартинес-Вакас, А.; Ди Пиердоменико, Дж.; Gallego-Ortega, A.; Валиенте-Сориано, FJ; Видал-Санс, М.; Picaud, S.; Villegas-Pérez, MP; García-Ayuso, D. Системното лечение с таурин осигурява функционална и морфологична невропротекция на фоторецепторите и възстановява функцията на пигментния епител на ретината при RCS плъхове. Redox Biol. 2022, 57, 102506. [CrossRef] [PubMed]
88. Кастели, В.; Паладини, А.; Д'Анджело, М.; Алегрети, М.; Мантели, Ф.; Brandolini, L.; Cocchiaro, P.; Cimini, A.; Varrassi, G. Таурин и оксидативен стрес при здравето и заболяването на ретината. Неврология на ЦНС. Там. 2021, 27, 403–412. [CrossRef]
89. Агарвал, Р.; Арфузир, NNN; Иежица, И.; Агарвал, П.; Сидек, С.; Ismail, NM Тауринът предпазва от увреждане на ретината и зрителния нерв, предизвикано от ендотелин-1 при плъхове чрез антиоксидантни ефекти. Невронна регенерация. Рез. 2018, 13, 2014–2021. [CrossRef] [PubMed]
90. Militante, J.; Lombardini, JB Свързана с възрастта дегенерация на ретината при животински модели на стареене: възможно участие на дефицит на таурин и оксидативен стрес. Neurochem. Рез. 2004, 29, 151–160. [CrossRef]
91. Wang, Y.; Гренел, А.; Zhong, F.; Ям, М.; Хауер, А.; Грегор, Е.; Жу, С.; Lohner, D.; Zhu, J.; Du, J. Метаболитен подпис на стареещото око при мишки. Neurobiol. Стареене 2018, 71, 223–233. [CrossRef]
92. Dayang, W.; Dongbo, P. Тауринът намалява индуцираната от синя светлина апоптоза на невроналните клетки на ретината in vitro. Кутан. Окул. Токсикол. 2018, 37, 240–244. [CrossRef]
93. Парк, J.-S.; Park, J.-H.; Ким, К.-Й. Невропротективни ефекти на миристаргенол А срещу индуцирана от глутамат апоптотична НТ22 клетъчна смърт. RSC Adv. 2019, 9, 31247–31254. [CrossRef]
94. Арашкевич, А.; Zozulinska-Ziolkiewicz, D. Невродегенерация на ретината в хода на диабет-патогенеза и клинична перспектива. Curr. Неврофармакол. 2016, 14, 805–809. [CrossRef] [PubMed]
95. Ishikawa, M. Аномалии в метаболизма на глутамата и екситотоксичност при заболявания на ретината. Scientifica 2013, 2013, 528940. [CrossRef] [PubMed]
96. Choi, D. Невротоксичност на глутамат и заболявания на нервната система. Neuron 1988, 1, 623–634. [CrossRef] [PubMed]
97. Агарвал, Р.; Agarwal, P. Модели на гризачи на глаукома и тяхната приложимост за откриване на лекарства. Експертно мнение. Лекарство Discov. 2017, 12, 261–270. [CrossRef] [PubMed]
98. Леон, Р.; Wu, H.; Джин, Й.; Wei, J.; Buddhala, C.; Prentice, H.; Wu, JY Защитна функция на таурина при индуцирана от глутамат апоптоза в култивирани неврони. J. Neurosci. Рез. 2009, 87, 1185–1194. [CrossRef]
99. Були, С.; Shen, W. Реципрочна регулация между отговора на таурин и глутамат чрез Са 2+- зависими пътища в неврони от трети ред на ретината. J. Biomed. Sci. 2010, 17 (Допълнение 1), S5. [CrossRef]
100. Ю, X.; Xu, Z.; Ми, М.; Xu, H.; Zhu, J.; Wei, N.; Чен, К.; Джан, К.; Zeng, K.; Wang, J.; et al. Хранителната добавка с таурин облекчава диабетната ретинопатия чрез анти-екзитотоксичност на глутамата при индуцирани от стрептозотоцин плъхове Sprague-Dawley. екситотоксичност на глутамат при индуцирани от стрептозотоцин плъхове Sprague-Dawley. Neurochem. Рез. 2007, 33, 500–507. [CrossRef]
101. Оливейра, MW; Minotto, JB; де Оливейра, MR; Zanotto-Filho, A.; Бер, Джорджия; Rocha, RF; Moreira, JC; Klamt, F. Почистващ и антиоксидантен потенциал на физиологичните концентрации на таурин срещу различни реактивни кислородни / азотни видове. Pharmacol. Rep. 2010, 62, 185–193. [CrossRef]
102. Джафри, AJA; Agarwal, R.; Иежица, И.; Агарвал, П.; Ismail, NM Тауринът предпазва от увреждане на ретината, предизвикано от NMDA, като намалява оксидативния стрес на ретината. Аминокиселини 2019, 51, 641–646. [CrossRef]
103. Аудо, И.; Mohand-Said, S.; Boulanger-Scemama, E.; Zanlonghi, X.; Condroyer, C.; Демонтант, В.; Boyard, F.; Антонио, А.; Méjécase, C.; El Shamieh, S.; et al. Актуализация на MERTK мутация при наследствени заболявания на ретината. тананикам Мутат. 2018, 39, 887–913. [CrossRef]

104. Едуардс, РБ; Szamier, RB Дефектна фагоцитоза на изолирани външни сегменти на пръчка от RCS плъх ретинален пигментен епител в култура. Наука 1977, 197, 1001–1003. [CrossRef] [PubMed]
105. Ли, Л.; Turner, JE Наследствена дистрофия на ретината при RCS плъхове: Предотвратяване на дегенерация на фоторецептори чрез трансплантация на пигментни епителни клетки. Exp. Eye Res. 1988, 47, 911–917. [CrossRef] [PubMed]
106. Валиенте-Сориано, FJ; Салинас-Наваро, М.; Ди Пиердоменико, Дж.; Гарсия-Аюсо, Д.; Лукас-Руис, Ф.; Пинила, И.; Куенка, Н.; Видал-Санс, М.; Villegas-Pérez, MP; Agudo-Barriuso, M. Проследяване на ретината за анализиране на целостта и фагоцитния капацитет на пигментния епител на ретината. Sci. Rep. 2020, 10, 7273. [CrossRef] [PubMed]
107. Гарсия-Аюсо, Д.; Ди Пиердоменико, Дж.; Видал-Санс, М.; Villegas-Pérez, MP Смъртта на ганглийните клетки на ретината като късен ремоделиращ ефект от дегенерация на фоторецепторите. Вътр. J. Mol. Sci. 2019, 20, 4649. [CrossRef] [PubMed]
108. Ди Пиердоменико, Дж.; Гарсия-Аюсо, Д.; González-Herrero, MER; Гарсия-Бернал, Д.; Бланкер, М.; Bernal-Garro, JM; Гарсия Ернандес, AM; Видал-Санс, М.; Villegas-Pérez, MP Трансплантации на мононуклеарни клетки, получени от костен мозък, намаляват глиозата на ретината при два животински модела на наследствена фоторецепторна дегенерация. Вътр. J. Mol. Sci. 2020, 21, 7252. [CrossRef]
109. Ди Пиердоменико, Дж.; Шолц, Р.; Валиенте-Сориано, FJ; Sánchez-Migallón, MC; Видал-Санс, М.; Лангман, Т.; Agudo-Barriuso, М.; Гарсия-Аюсо, Д.; Villegas-Pérez, MP Невропротективни ефекти на FGF2 и миноциклин в два животински модела на наследствена дегенерация на ретината. разследване. офталмол. Vis. Sci. 2018, 59, 4392–4403. [CrossRef]
110. Даулинг, JE; Sidman, RL Наследствена дистрофия на ретината при плъхове. J. Cell Biol. 1962, 14, 73–109. [CrossRef]
111. Гарсия-Аюсо, Д.; Ди Пиердоменико, Дж.; Agudo-Barriuso, М.; Видал-Санс, М.; Villegas-Pérez, M. Ремоделирането на ретината след дегенерация на фоторецепторите причинява смърт на ганглийните клетки на ретината. Невронна регенерация. Рез. 2018, 13, 1885–1886. [CrossRef]
112. Гарсия-Аюсо, Д.; Салинас-Наваро, М.; Надал-Никол, FM; Ортин-Мартинес, А.; Agudo-Barriuso, М.; Видал-Санс, М.; Villegas-Pérez, MP Секторна загуба на ганглийни клетки на ретината при наследена фоторецепторна дегенерация се дължи на смърт на RGC. бр. J. Ophthalmol. 2014, 98, 396–401. [CrossRef]
113. Villegas-P, MP; Лорънс, JM; Видал-Санс, М.; Lavail, MM; Lund, RD Загуба на ганглийни клетки в ретината на плъх RCS: резултат от компресия на аксони чрез свиване на интраретинални съдове, свързани с пигментния епител. J. Comp. неврол. 1998, 392, 58–77. [CrossRef]
114. Рашер, К.; Servos, G.; Berthold, G.; Hartwig, H.-G.; Warskulat, U.; Heller-Stilb, B.; Häussinger, D. Лишаването от светлина забавя, но не предотвратява загубата на фоторецептори в мишки с нокаут на таурин транспортер. Vis. Рез. 2004, 44, 2091–2100. [CrossRef] [PubMed]
115. Фан, Й.; Lai, J.; Юан, Й.; Wang, L.; Wang, Q.; Yuan, F. Тауринът защитава клетките на ретината и подобрява синаптичните връзки при плъхове с ранен диабет. Curr. Eye Res. 2019, 45, 52–63. [CrossRef] [PubMed]
116. Гарсия-Аюсо, Д.; Ди Пиердоменико, Дж.; Валиенте-Сориано, FJ; Мартинес-Вакас, А.; Agudo-Barriuso, М.; Видал-Санс, М.; Picaud, S.; Villegas-Pérez, MP -аланинова добавка предизвиква изчерпване на таурин и причинява промени в слоя нервни влакна на ретината и аксонален транспорт от ганглийните клетки на ретината. Exp. Eye Res. 2019, 188, 107781. [CrossRef] [PubMed]
117. Хорват, Г.-А.; Hukin, J.; Stockler-Ipsiroglu, S.; Aroichane, M. Очни констатации при лечение с вигабатрин и таурин при двама пациенти с дефицит на янтарна полумиалдехид дехидрогеназа. Невропедиатрия 2016, 47, 263–267. [CrossRef] [PubMed]
118. Preising, MN; Гьорг, Б.; Friedburg, C.; Qvartskhava, N.; Budde, BS; Бонус, М.; Toliat, MR; Pfleger, C.; Altmüller, J.; Еребиан, Д.; et al. Биалелната мутация на човешки SLC6A6, кодираща транспортера на таурин TAUT, е свързана с ранна дегенерация на ретината. FASEB J. 2019, 33, 11507–11527. [CrossRef]
119. Джамул, Ф.; Dégardin, J.; Болка, Д.; Гондуен, П.; Simonutti, M.; Дъбъс, Е.; Caplette, R.; Фуке, С.; Занаят, CM; Сахел, JA; et al. Дефицитът на таурин уврежда фоторецепторите и ганглиозните клетки на ретината при третирани с вигабатрин неонатални плъхове. Mol. Клетъчни неврони. 2010, 43, 414–421. [CrossRef]
120. Тао, Й.; Янг, Дж.; Ма, З.; Ян, З.; Liu, C.; Ма, Дж.; Wang, Y.; Янг, З.; Huang, YF Индуцираната от вигабатрин ретинална токсичност е свързана с фотопично излагане и дефицит на таурин: изследване in vivo. Cell Physiol. Biochem. 2016, 40, 831–846. [CrossRef]
121. Ламбук, Л.; Иежица, И.; Agarwal, R.; Бакър, NS; Агарвал, П.; Ismail, NM Антиапоптотичен ефект на таурин срещу индуцирана от NMDA ретинална екситотоксичност при плъхове. Невротоксикология 2018, 70, 62–71. [CrossRef]
Отказ от отговорност/Бележка на издателя:Твърденията, мненията и данните, съдържащи се във всички публикации, са само на отделния автор(и) и сътрудник(и), а не на MDPI и/или редактора(ите). MDPI и/или редакторът(ите) се отказват от отговорност за всякакви наранявания на хора или собственост, произтичащи от идеи, методи, инструкции или продукти, посочени в съдържанието.
【За повече информация:george.deng@wecistanche.com / WhatsApp:8613632399501】
